На рисунке показана фазовая диаграмма воды. Укажите на диаграмме точки, характеризующие равновесие жидкой и паровой фаз.
Хлор
3. Количественно процессы электролиза подчиняются законам
3)Фарадея
4. Процесс, протекающий при электролизе раствора сульфата натрия на платиновом аноде, описывается уравнением:
2)2H2O + 2ē → H2 + 2OH-
5. Процесс, протекающий при электролизе раствора сульфата никеля на никелевом аноде описывается уравнением:
3)Ni - 2 ē → Ni2+
6. Процесс, протекающий при электролизе раствора хлорида меди(II) на платиновом аноде, описывается уравнением
1)2Cl- -2 ē→ Cl2
7. При электролизе водного раствора смеси солей CuCl2, KCl, AlCl3 на катоде протекает процесс:
1)Cu2+ + 2 ē → Cu0
8. На электродах гальванического элемента Якоби-Даниэля, состоящего из цинковой и медной пластин, протекают следующие процессы:
2)A: Zn - 2 ē → Zn2+ K: Cu2+ + 2 ē → Cu
9. На электродах гальванического элемента Якоби-Даниэля, состоящего из серебряной и свинцовой пластин, протекают следующие процессы:
1)A: Pb - 2 ē → Pb2+ K: Ag+ + 1 ē →Ag
10. Гальванический элемент Вольта состоит из цинковой и медной пластин, опущенных в раствор серной кислоты. На электродах этого гальванического элемента протекают следующие процессы:
1)А: Zn – 2 ē → Zn2+ K: 2H+ + 2 ē → H2
11. На электродах гальванического элемента Якоби-Даниэля., состоящего из цинковой и железной пластин, протекают следующие процессы:
1)А: Zn – 2 ē → Zn2+ K: Fe2+ + 2 ē → Fe
12. Наибольшую э.д.с. имеет гальванический элемент:
4)Mg / Mg(NO3)2, 1M // AgNO3, 1M / Ag
13. В гальваническом элементе Якоби-Даниэля при 298 К установилось равновесие :
Zn + 2Ag+ ←→ Zn2+ + 2Ag
Концентрация ионов Zn2+ составляет 0,01моль/л, концентрация ионов Ag+ составляет 0,001 моль/л. Э.д.с. данного гальванического элемента равна:
3)1,44 В
14. Э.д.с. гальванического элемента
Zn / ZnSO4, 0,000001 M // ZnSO4, 0,01 M /Zn равна:
В
15. Краткая схема гальванического элемента Якоби-Даниэля имеет вид:
Zn / ZnSO4, 1M // CuSO4, 1M / Cu
Э.д.с. данного гальванического элемента равна:
В
16. Процессы, протекающие при контактной коррозии магния и железа в нейтральной водной среде, описываются уравнениями
1)А: Mg – 2e → Mg2+ K: 2H2O + O2 – 4e → 4OH-
17.Для протекторной защиты железа от коррозии в нейтральной водной среде применяется:
Цинк
18. Металлом, наиболее подверженным электрохимической коррозии при контакте с оловом, является:
Магний
19. Электрохимическая коррозия железа в нейтральной водной среде описывается уравнением:
1)4Fe + 3O2 + 6H2O = 4Fe(OH)3
20. Процессы, протекающие при коррозии оцинкованного железа во влажном воздухе, описываются уравнениями:
3)А: Zn – 2e → Zn2+
K: 2H2O + O2 – 4e → 4OH-
21. Уравнение, отвечающее электрохимической коррозии металла:
3)2Zn + O2 + 2H2O = 2Zn(OH)2
22. Процесс отвода электронов с катодных участков при электрохимической коррозии называется:
Деполяризацией
23. Металлом, который может служить анодным покрытием на железе, является:
Магний
24. Процесс коррозии лужёного железа в кислой среде при нарушении целостности покрытия описывается уравнениями:
2)А: Fe – 2ē→ Fe2+ K: 2H+ + 2ē → H2
25. Атмосферная коррозия лужёного железа (покрытого тонким слоем олова) описывается уравнениями:
1)А: Fe – 2ē → Fe2+ K: 2H2O + O2 +4ē → 4OH-
Тесты по разделу «Химическая связь»
1. Между атомами элементов с порядковыми номерами 3 и 9 образуется химическая связь
1) ионная
2. Наименее прочная химическая связь
2) водородная
3. При образовании молекулы хлороводорода перекрываются орбитали
3) s и р
4. При гибридизации одной одной s- и одной р-орбиталей образуются
3) две гибридные sр-орбитали
5. Между молекулами воды образуется вид связи
2) водородный
6.Между молекулами этилового спирта образуется вид связи
2) водородный
7. Последовательность заполнения молекулярных орбиталей в порядке возрастания их энергии σs<σs*<σz<πх=πу<πх*=πу*<σz* характерна для молекулы
3) O2
8. Последовательность заполнения молекулярных орбиталей в порядке возрастания их энергии σs<σs*<πх=πу<σz <πх*=πу*<σz* характерна для молекулы
4) CO
9. Кратность связи в молекуле О2 равна
2) 2
10. Кратность связи в молекуле N2 равна
3) 3
11. Кратность связи в молекуле Н2 равна
1) 1
12. В хлориде аммония отсутствуют связи
4) ковалентные неполярные
13. Ковалентную неполярную связь имеет
3) Н2
14. Ковалентную полярную связь имеет
4) НСl
15. Наибольшую склонность к образованию ионных связей проявляет элемент
5) F
16. Геометрическая форма молекулы метана СН4
2) тетраэдрическая
17. Угол 109028/ образуется между гибридными
3) sр3-орбиталями
18. Угол 1200 характерен для
4) угловой молекулы
19. Угол 109028/ характерен для
2)тетраэдрической молекулы
20. Геометрическая форма молекулы аммиака NH3
2) пирамидальная
21. Прочность и полярность связи в ряду молекул HF→HCl→НВr→HJ изменяются:
3) как прочность, так и полярность связи уменьшаются
22. π-связь образуется при перекрывании
4) р-орбиталей, оси которых параллельны
23. Две π-связи имеет молекула
2) СО2
24. Двойную связь имеет молекула
4) O2
25. Тройную связь имеет молекула
4) C2Н2
26. Трехцентровую связь имеет молекула
2) НNО3
27. Линейную форму имеет молекула
2) ВeCl2
28. Пирамидальную форму имеет молекула
1) NH3
29. Число σ-связей в три раза больше числа π-связей
4) хлористой кислоты
30 Все связи ковалентные неполярные в молекуле
5) О2
31. Парамагнитной является молекула
2) O2
32. В молекуле аммиака NH3 число связывающих электронных пар равно
2) 3
33. В молекуле аммиака NH3 число несвязывающих электронных пар равно
3) 1
34. Формулы соединений только с ковалентной связью представлены в ряду
3) H2O, СН3СООН
Тесты по разделу «Полимеры»
1.Карбоцепным является полимер:
1) (-СF2-)n –тефлон
2.Гетероцепным полимером является:
5) (-СН2-СН2О-)n-полиэтиленоксид
3.Полимерами не являются:
4) Продукты взаимодействия щелочей с минеральными кислотами
4 Наиболее устойчивым полимером является:
Тефлон ( Фторпласт-4)
5. При нагревании термопласты:
2)Переходят в вязкотекучее состояние практически без разложения
6.Природным полимером является:
1)Желатин
7.Органические ВМС содержат в своем составе:
4)Углерод, водород, азот, кислород и серу
8.При реакции поликонденсации не образуются:
4) Водород
9. К сетчатым полимерам не относятся:
3) Резина
10. Поликонденсационные ВМС могут быть получены реакциями взаимодействия:
4) Гексаметилендиамина и адипиновой кислоты
11. Степень полимеризации это:
1) Отношение среднего молекулярного веса полимера к молекулярному весу мономера
12. При полимеризации метилметакрилата - СН2=С(СН3)СООСН3 образуется:
1) Полиметилметакрилат
13. При обработке полистирола серной кислотой образуется:
2) Сульфированный полистирол
14. При гидролизе капрона образуются:
1) Капроновая кислота
15. Пенополиуретаны это:
2) Вспененные полиуретаны
16. Силиконы это:
3) Полисилоксаны
17. Натуральный каучук это:
2) Цис-полиизопрен
18. При нитровании клетчатки не образуется:
4) Целлофан
19. Лавсан (терилен) образуется при взаимодействии:
1) Диметилтерефталата с этиленгликолем
20. При нагревании термореактивных ВМС не образуются:
5) Продукты полимераналогичных превращений
21. При реакции поликонденсации формальдегида с фенолом не образуется:
3) Резина
22. При гидролизе поливинилацетата обрауется:
2) Поливиниловый спирт
23. При полном сгорании полиэтилена образуются:
1) СО2 и Н2О
24. Реакция радикальной полимеризации осуществляется под действием:
1) Инициаторов радикальной полимеризации
25. Полиамиды получаются при взаимодействии:
4) Диаминов с двухосновными кислотами
Тесты к разделу «Физикохимический анализ»
На рисунке показана фазовая диаграмма воды. Укажите на диаграмме точки, характеризующие равновесие жидкой и паровой фаз.
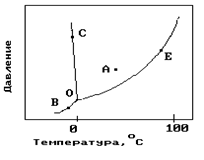 | 5) О и Е |
На рис. приведена диаграмма состояния системы компонентов M и N. Укажите на диаграмме точки, отвечающие равновесию жидкого сплава и кристаллов химического соединения MN.
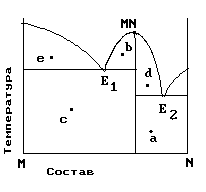 | 2) b и d |
На рис. приведена диаграмма состояния системы А-В. Укажите на диаграмме область однородного расплава.
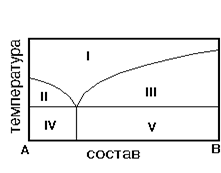
2) I
