Структура автоматизированной системы испытаний
Общие принципы
Для осуществления указанных целей необходимо эффективное массовое испытание ксенобиотиков на биологическую активность.
Проверка большого массива ксенобиотиков на один или несколько видов биологической активности получила название скрининга.
Идея скрининга возникла достаточно давно, во всяком случае в период становления химической индустрии она уже прочно завоевала себе место в умах фармакологов. В 1910 г. одна из немецких фирм испытала около 1200 производных акридина. На «сите» оказалось три препарата: трифловин (против паразитических заболеваний), риванол (антисептик), акрихин (противомалярийный). В поисках заменителя хинина в 30-е гг. было исследовано 16 000 соединений, принадлежащих к различным группам. Среди них 7618-м по счету оказался хлорохин, а 13272-м – притахин.
В 1966 г. в США в поисках противоопухолевых препаратов было испытано около 114 000 соединений, из которых было отобрано 12 потенциальных лекарств, но ни одно из них не стало достаточно выдающимся в своем классе фармакологических препаратов.
С 1928 г. в СССР на протяжении 10 лет в поисках алкалоидов под руководством А.П. Орехова было исследовано 700 растений, среди которых искомыми оказались всего 60 алкалоидов. В следующие 10 лет исследовались еще 4500 растений и было открыто еще 20 алкалоидов.
Таким образом, тотальная проверка большого массива химических соединений или природных объектов, направленная на выявление потенциальных фармакологических препаратов, получила в ХХ в. свое развитие как один из основных методов поиска новых лекарств и вообще химических соединений с заданным типом биологической активности.
Экономическая эффективность скрининга возрастает, если растет число тестируемых активностей, и скрининг становится многоцелевым, например помимо фармакологии ориентирован и на цели сельского хозяйства, микробиологической промышленности, охраны окружающей среды и т. д.
Системное определение биологической активности всего массива соединений может быть осуществлено путем создания высокопроизводительной системы их классификации по видам биологический активности. Каждый ксенобиотик обладает определенными видами и степенью биологической активности. Мы должны выявить эти свойства и предсказать возможность практического использования данного соединения или дать прогноз его возможной роли в окружающей среде.
Система тестирования ксенобиотиков по видам биологической активности может включать два взаимосвязанных подхода. Первый – уровень целевого объекта испытаний (человек, животное, растение, биогеоценоз), на который направлено действие искомого ксенобиотика, исходя из целей поиска (лекарства, ветеринарное средство, гербицид и т. д.), и второй подход – совокупность тест-объектов, базирующихся на использовании более примитивной организации живой материи, чем целевой. Использование второго подхода оправдано в тех случаях, когда первый не обеспечивает достаточной производительности и т. д.
Существует ряд особенностей, затрудняющих индустриализацию процесса биологического испытания соединений на целых организмах, в частности на животных. К ним относятся следующие:
– необходимость большого количества животных в качестве тест-объектов;
– затрата большого количества исследуемого химического соединения. Как правило, на первых порах синтезируется десятки – сотни миллиграмм вещества;
– ограниченность автоматизации процесса;
– единичный акт испытания химического соединения на животных мало управляем во времени и требует достаточно длительного срока.
Таким образом, работая со сравнительно небольшими массивами химических соединений и определяя сравнительно немного видов активности, для достижения любой из названных выше целей можно использовать животных как основной тест-объект.
Индустриальные масштабы испытаний и их промышленная организация требуют введения нового принципа, который позволил бы на порядки увеличить производительность системы и обеспечить возможность работы с малым количеством испытуемого вещества.
Поэтому возникает необходимость обратиться к исследованиям на тканевом, клеточном, молекулярных уровнях строения живого, что, в свою очередь, необходимо для выяснения механизма действия конкретного ксенобиотика.
Вот здесь вступает в право использование принципа качественного подобия – эпиморфизм тест-объекта и целевого объекта в отношении определенного биологического свойства ксенобиотика.
Принцип эпиморфизма – принцип конструктора: из небольшого количества деталей построить как можно большее количество Фигур. Возможности принципа эпиморфизма довольно велики, поскольку основные молекулярные строуктуры и субклеточные образования в большей степени единообразны у самых разнообразных живых объектов.
Главные методологические трудности при использовании эпиморфных моделей заключаются в том, чтобы определить оптимальный уровень детализации модели по отношению к моделирующему процессу, т. е. целостному организму. Этого можно достичь исходя из того, что в системе тест-объектов на клеточном уровне организации представляются все царства живого и основные типы тканей организма человека, а также из того, что у тест-объектов в совокупности определяются все основные реакции (гибель, повреждение, адаптация, проницаемость, метаболизм ксенобиотиков, синтез белка и ДНК, возбудимость и т. д.).
Когда мы говорим о биологической активности ксенобиотиков, то для ее определения, естественно, необходимы тест-объекты, на которых регистрируются определенные виды биологической реакции (гибель, изменение роста, изменение различных метаболических реакций и т. д.) при их действии; эти реакции называются тест-реакциями. В этой связи необходимо разработать принципы отбора и стандартизации тест-объектов при классификации ксенобиотиков по видам биологической активности.
Подбор тест-объектов предлагается проводить по следующим критериям: по молекулярным рецепторам, являющимся мишенями для веществ с данными видами активности; по принципу надмолекулярной организации и молекулярному составу (близость по структуре); по функциональному сходству; по органному или тканевому происхождению; по близости патологического состояния тест-объекта и реального объекта.
Первый критерий является самым сильным и надежным. Например, на этом критерии основан выбор ганглиев прудовика как модели нейронов головного мозга в отношении медиаторных и антимедиаторных видов биологической активности. Высокая гомология или даже тождество рецепторов для медиаторов у моллюсков и позвоночных служит основанием для надежности прогноза этих активностей на целевой тест-объект.
Второй (близость по структуре) и третий (близость по функции) критерии используются при выборе моделей для оценки влияния на подвижность (сперматозоиды, тетрахимена), на дыхание и гликолиз (печень, эритроциты, клетки опухолей), на фотосинтез (водоросль Nitella), на химический гомеостаз (печень – монооксигеназная система).
Давность эволюционного приобретения и консерватизм таких процессов, как жгутиковая подвижность, окислительное фосфорилирование и гликолиз, фотосинтез, монооксигеназная система, дают известную уверенность в том, что полученные на определенных тест-объектах данные можно переносить на подобные системы других видов тканей. Однако при этом следует иметь в виду, что высокая гомология надмолекулярной структуры или функции молекулярной системы не означает одинаковости молекулярного строения элементов, слагающих систему.
При рассмотренных трех критериях остается неопределенность прогноза, обусловленная необходимостью переносить результаты ответов in vitro на систему in vivo, а именно тем, что in vitro не учитывается доступность объекта-мишени, метаболизма ксенобиотика и строения реального объекта. Гибель клетки – это не значит гибель организма. Значительно большая степень неопределенности существует для тех видов активности, которым характерны системные эффекты на уровне ткани, органа или организма, т. е. в тех случаях, когда важные, определяющие особенности действия химических соединений зависят не от взаимодействия с какой-либо мишенью, а от взаимодействия с многими мишенями или всей реакцией системы на связывание с мишенью. Такие проблемы характерны для адаптогенов, витаминов, наркотиков.
В этом случае подбор биологических тест-объектов по критерию органного и тканевому происхождениям дает значительную гарантию прогноза. Однако все же гораздо надежнее строить прогноз по данным испытаний на объектах с учетом всех критериев.
И, естественно, следует учитывать последний признак – близость патологического состояния тест-объекта и реального объекта.
Классификация ксенобиотиков по видам биологической активности по-новому ставит вопрос о подборе и стандартизации тест-объектов. Система должна обеспечить возможность сопоставления результатов испытаний на биологическую активность разных соединений, проведенных в разные годы. Очевидно, этого можно достигнуть только в том случае, когда уровень стандартности тест-объектов очень высок в течение многих лет. Именно степень воспроизводимости, стандартность набора тест-объектов непосредственно определяют надежность принимаемых решений и степень автоматизации системы (возможно, в большей степени, чем ЭВМ).
И если с молекулярными тест-объектами это сделать проще, то объекты клеточно-тканевого уровня организации – «живые». Как все живое, они непрерывно развиваются, подвергаются сильному влиянию эндогенных и экзогенных факторов, физиологическое состояние тест-объектов подвержено сезонным колебаниям и т. д.
Каждый тест-объект индивидуален, что приводит к целому ряду затруднений при регистрации его характеристик, интерпретации данных, выявлении их соответствия поставленным целям и т. д.
Существует ряд методических подходов для стандартизации, подбора, приготовления тест-объектов, например: стандартизация условий содержания животных; использование контрольных карт (отбраковка животных, для которых отклонения согласно карте превышают определенную величину); выбор наиболее щадящих условий выделения и инкубации; использование дополнительных воздействий, переводящих тест-объект в заданное состояние; нормирование регистрируемых параметров (приведение к норме); выбор тест-реакций, минимальным образом зависящих от индивидуальности тест-объектов и т. д.
В конечном итоге для каждого тест-объекта клеточно-тканевой природы можно создать формализованный стандарт в виде набора количественных параметров, характеризующих стационарные и кинетические показатели тест-объектов.
Структура автоматизированной системы испытаний
С целью индустриализации процесса тестирования биологической активности ксенобиотиков необходимо иметь автоматизированную систему испытаний. Для разработки схемы испытаний ксенобиотиков на любые виды биологической активности следует вспомнить в самом общем виде путь их действия на живой объект. Попадая в организм, химическое вещество проникает в определенные ткани; в тканях взаимодействует с определенными клетками; в клетках – с определенными субклеточными структурами, а в пределах этих структур взаимодействует с биополимерами или низкомолекулярными соединениями клетки. В обратном порядке развивается реакция целостного организма – от молекулы-мишени до организма.
Как уже упоминалось, результаты воздействия ксенобиотиков зависят в первую очередь от химической структуры самого вещества, его физико-химических свойств, которые определяют тропность вещества к определенным тканям, клеткам и характер взаимодействия с молекулярными мишенями, а также зависят от структуры мишени и его функциональной роли.
Всю совокупность операций по классификации ксенобиотиков можно представить следующим образом:
1. Классификация по видам биологической активности на основании химических, физических и физико-химических свойств испытуемых соединений при отсутствии биологического тест-объекта путем расчетных операций над структурой соединения и экспериментального определения их физико-химических свойств.
2. Классификация по результатам взаимодействия соединений с моделями клетки, организма, биосферы, включающая последовательные иерархические уровни организации биологической материи:
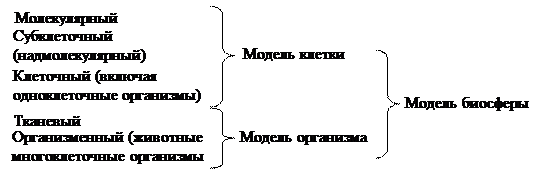 |
Моделируемые объекты (клетки, организм, биосфера) предстают в системе в виде представительных наборов тест-объектов, обладающих основными элементарными функциями, присущими целевым объектам.
В принципе, модели клетки и организма могут быть нормальными и патологическими.
Выборки тест-объектов и их расположение в системе должны отражать реальную иерархию элементов природного объекта, иерархию, обусловленную его развитием. Поэтому для организма детализацию видов биологической активности следует строить по тканевой тропности действия, опираясь на чисто генетическую классификацию типов тканей, отражающую ход онтогенеза. Представление биосферы в системе классификации должно основываться на таксономической классификации организмов, отражающей процесс эволюции.
Общий принцип организации биологических испытаний химических соединений – это многоуровневый набор тестов с повышающейся на каждом уровне сложностью биологического тест-объекта (модели) и соответственно растущей детализацией и надежностью прогноза вида биологической активности. Первый уровень – базовый, через него проходят все соединения, которые в соответствии с результатами прохождения этого первого уровня направляются затем к специализированным тестам.
Базовый уровень состоит из трех подуровней. Биологическая активность ксенобиотика уже включена в его химическую структуру. Поэтому на первом подуровне сведения о структуре и некоторых свойствах соединений вводятся в компьютер, который производит первичный анализ принадлежности соединения данной структуры к определенным уже известным классам биологической активности.
На втором подуровне эта классификация производится на основании экспериментального определения дополнительных физико-химических характеристик веществ.
На третьем подуровне в систему вводятся тест-объекты. Основным тест-объектом этого подуровня является изолированная клетка. Набор клеток (бактерии, простейшие, клетки растений, клетки высших животных) представляет собой огрубленную модель биосферы.
На этом подуровне регистрируется способность чужеродных химический соединений влиять на такие основные свойства живой клетки, как рост, дыхание, энергетика, биосинтез, способность к генетическим изменениям и т. д.
База пропускает весь массив испытуемых ксенобиотиков, выдавая для каждого из них единообразный набор характеристик – основной биологический «паспорт».
Биологический «паспорт» ксенобиотика – документ, которым должно снабжаться каждое соединение, поступившее из испытания. «Паспорт» должен содержать сведения о структуре вещества, источнике его происхождения, результаты теоретического и экспериментального изучения соединения, включая первичную оценку безопасности ксенобиотика. Биологический «паспорт» ксенобиотика – это итоговый документ.
Второй уровень, меньший по пропускной способности, – надстройка. Надстройка работает в режиме преимущественной ориентации на первые две цели: нахождение химического соединения, обладающего полезными для человеческого организма свойствами, и обнаружение вредных для человеческого организма биологических активностей испытуемых химических соединений.
Правда, при наличии технологических возможностей и в случае экономической целесообразности можно доводить производительность отдельных узлов надстройки до производительности базы и пропускать через эти узлы весь поток веществ.
Надстройка работает прежде всего ради достижения целей, связанных с организмом человека. Поэтому клетки человека и организм человека в целом берутся за основу при проектировании надстройки. Надстройка имеет дело с расчлененным потоком веществ, т. е. на отдельные испытательные блоки приходятся лишь некоторые подмножества на основе данных, получаемых в базе.
Следовательно, вся совокупность операций по классификации ксенобиотиков выглядит следующим образом:
– классификация химических соединений по видам биологической активности на основании химических, физических и физико-химических свойств испытуемых чужеродных соединений при отсутствии биологического тест-объекта: расчетных операций над структурой соединения; экспериментального определения физико-химических свойств химических соединений;
– классификация по результатам взаимодействия чужеродных соединений с моделями клетки, организма, биосферы, включающая последовательные иерархические уровни организации биологической материи.
Испытанию ксенобиотиков на множество видов биологической активности должна предшествовать операция предварительной сортировки на моделях, допускающих создание испытательных систем высокой производительности, т. е. на предварительном этапе на упрощенных (модельных) системах необходимо предсказать вид биологической активности и определить ксенобиотики, которые, по вероятным оценкам, не обладают определенными видами активности (резус) или являются токсичными (исключаются из системы испытаний).
Основная идея предыспытания состоит в том, чтобы реализовать следующий методологический подход. Заменить модели организменного уровня некоторой совокупностью моделей доорганизменного уровня. Таким образом, достигается цель более экономного расхода химического соединения на единичное испытание и реальнее становится автоматизация испытаний с технологической стороны. В этом случае при определении наиболее важных видов биологической активности и перенесении закономерностей на целостный организм подбирается совокупность адекватных моделей на основе принципа биологического эпиморфизма.
Процедура организации биологических испытаний ксенобиотиков, скажем, ориентированная на поиск лекарственных препаратов и оценку их безопасности, в общем виде сводится к следующему (рис. 3.1).
Вначале исследуются два массива ксенобиотиков: новые и известные. Это связано с тем, что среди известных соединений, не испытывавшихся ранее на биологическую активность, могут быть обнаружены искомые лекарства. Кроме того, для известных тестируемых ксенобиотиков могут быть выявлены новые виды биологической активности. Все это заставляет включить в систему испытаний как вновь синтезируемые, так и уже испытанные на отдельные виды биологической активности ксенобиотики.
На первом этапе испытаний представляется целесообразным из потока тестируемых ксенобиотиков исключить из дальнейшей проверки токсические вещества и соединения, не представляющие по каким-либо причинам в данный момент интереса.
 |
| Рис. 3.1. Блок-схема биологических испытаний ксенобиотиков (БА – биологическая активность, БАВ – биологически активные вещества) |
При дальнейших испытаниях проводится предварительная оценка безопасности отобранных ксенобиотиков. С учетом полученных результатов по фармакологической активности на более простых моделях последующая проверка ксенобиотиков проводится на животных. Ксенобиотики, у которых обнаружена нужная для практических целей активность, проходят испытания по полной программе, включая тестирование на основные и побочные виды активности, оценку острых, хронических и отдаленных форм проявления биологических активностей.
Разработка новых лекарственных средств, клинические испытания и опытное производство составляют последующие этапы в процессе создания лекарств.
Схема прохождения тестируемых ксенобиотиков через систему, включающую тесты доорганического уровня и фармакологические тесты на животных, согласно изложенным положениям представлена на рис. 3.2. Во многих случаях можно подобрать объект, ответная реакция которого будет наиболее специфической для определенного класса чужеродных соединений, несущего соответствующий вид биологической активности.
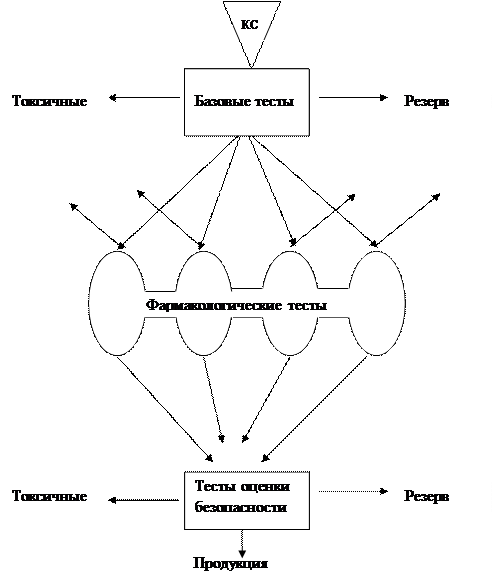 |
| Рис. 3.2. Система биологических испытаний химических соединений. КС – ксенобиотик |
Такой датчик может быть вначале обучен на определенном классе известных химических соединений, а затем использован для классификации химических соединений по степени сходства реакций биодатчика на вновь тестируемое химическое соединение и на вещества из обучающей выборки, т. е. путем обратного скрининга.
Биологический объект, используемый в качестве датчика, как мы видели, может вообще не являться моделью тех клеток, субклеточных структур и молекулярных рецепторов, на которые в организме действует химическое соединение данного вида биологической активности. Объект в этом случае выступает как чувствительный элемент прибора, осуществляющего индикацию химического соединения и индификацию вида активности.
Необходимо отметить, что следует различать специфические и неспецифические модели тест-объектов. Первые как раз и имеют четко выраженные молекулярные мишени-рецепторы (вспомним первый критерий), реагирующие на определенные химические соединения, т. е. на определенные виды биологической активности.
Однако неспецифическая модель является обязательным компонентом для классификации химических соединений. С одной стороны, оказывается возможным различать химические соединения, обладающие разными видами активности на полностью неспецифической для этих видов активности модели. Так, разработана аппаратура и методика для регистрации 16 параметров реакции эритроцитов (параметры получены из кинетических изменений светопропускания, импеданса и рН суспензии эритроцитов) на воздействия химических соединений. При испытаниях таких разных по активности и химической природе веществ, как тетрациклины, пенициллины, кортикостероиды и др., показано, что для каждого из классов этих веществ существует свой характерный портрет, выраженный в терминах 16 параметров (рис. 3.3).
В этом случае один и тот же тест-объект используется в качестве эпиморфной модели и как элемент классифицирующей системы, работающей в режиме логического конструктора.
Однако основным вариантом является, конечно, случай, когда предсказание биологической активности осуществляется через построение логической функции, элементами которой становятся реакции отдельных биодатчиков. Эти датчики являются одновременно эпиморфными моделями, позволяющими улавливать многие виды биологической активности на основе как эпиморфных соответствий, так и логических функций, полученных при обратном скрининге.
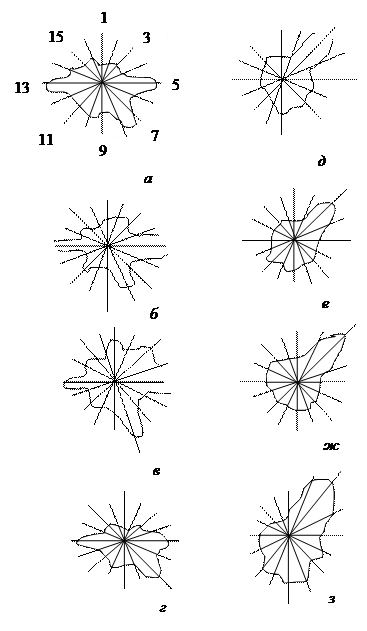 |
Рис. 3.3. Диаграммы действия чужеродных химических соединений
на суспензию эритроцитов:
а – тетрациклин; б–метациклин гидрохлорид; в – окситетрациклин;
г – морфоциклин;
д – метандростенолон; е – металандростеалон; ж – метилтестостерон;
з – феноболин
С другой стороны, использование неспецифической модели позволяет охарактеризовать дополнительный вид биологической активности химических соединений. Например, известно, что при многих заболеваниях значительная часть неспецифических общепатологических симптомов связана с появлением так называемых СМ-вторичных эндогенных токсинов пептидной природы. Для вскрытия одного из путей патологического действия СМ была выбрана модель – клетка Nitella, на которой было показано прямое неспецифическое мембранотропное действие СМ, обусловленное их поверхностной активностью.
Более того, на этой модели возможно предсказание очень широкого спектра биологической активности с классификацией веществ по их механизму действия (например, на ионную проницаемость, ионные токи, функционирование отдельных транспортных систем и т. д.).
Вещества, представляющие по своим свойствам научный и практический интерес, проходят тестирование на безопасность. Объекты испытаний по-прежнему модельные, но оценке подлежат и такие виды опасного действия, как мутагенность, канцерогенность, эмбриотоксичность и др.
