Производные солициловой кислоты
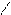 O
O

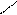

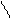
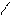
 С
С
 OH OH Обладает сильными кислотными свойствами, т.к. анион этой к-ты стабилизирован обр-ем внутримолекулярной водород.связи.
OH OH Обладает сильными кислотными свойствами, т.к. анион этой к-ты стабилизирован обр-ем внутримолекулярной водород.связи.

 O
O


 C-O-
C-O-


O-H
1) Произ-ые по –COOH:






 COOH CH3,H+ COOCH3
COOH CH3,H+ COOCH3
 -H2O OH метилсалицилат
-H2O OH метилсалицилат

 OH a)PCl5 COOC6H5
OH a)PCl5 COOC6H5
 б)С6Н5ОNa OH фенилсалицилат
б)С6Н5ОNa OH фенилсалицилат
 NaHCO3 COONa
NaHCO3 COONa

 -H2O,-CO2
-H2O,-CO2
 OH салицилатNa
OH салицилатNa
2) Ппроизв-ые по –OH:



 COOH (CH3CO)2O COOH ацетилсалециловая к-та.(аспирин)
COOH (CH3CO)2O COOH ацетилсалециловая к-та.(аспирин)

 OH –CH3COOH OCOCH3
OH –CH3COOH OCOCH3
Это анельгетич., противосп-st? жаропонижающие ср-ва.
Оксокислоты
Альдегидокислоты кетокислоты


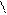 O O СН3=С-СООН
O O СН3=С-СООН
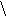 C-C О
C-C О
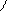 H OH
H OH
Глиаксалевая к-та.
(оксо-этановая) пировиноградная к-та. (ПВК)

 **СН3-С-СН2-COOH ацетоуксусная (АУК)
**СН3-С-СН2-COOH ацетоуксусная (АУК)
O

 ** O
** O
HOOC-C-CH2-COOH щавелевоуксусная к-та. ЩУК)

 ** HOOC-C-CH2- CH2-COOH α-кетоглутаровая
** HOOC-C-CH2- CH2-COOH α-кетоглутаровая
O
По взаимному расположению – COOHи –OHразличают: α, β, γ.
Способы получения:** Окисление гидроксикислот.


 CH3-C-COOH[O] CH3-C-COOH ПВК
CH3-C-COOH[O] CH3-C-COOH ПВК
 OH O
OH O
Молоч.к-та
** Гидролиз геминальных дигалогенопроизводных




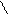
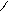
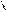
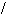


 СH3-C-COOH 3NaOH CH3-C-COONa CH3-C-COONa +HCl CH3CCOOH
СH3-C-COOH 3NaOH CH3-C-COONa CH3-C-COONa +HCl CH3CCOOH
Cl Cl -2NaCl OH HO -H2O O -NaCl O
-2H2O
Химические свойства: *по –COOH
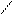
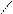 O
O
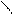 *по –С
*по –С
H
Альдегидок-ты легко окис-ся образуя дикарбоновые к-ты.
α и β оксок-ты сравнительно легко декарбоксилируются.
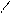
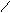 O Но сл.эфиры α/β-оксокислот сравнительно устойчивы.
O Но сл.эфиры α/β-оксокислот сравнительно устойчивы.


 СH3-C-COOH H2SO4, to CH3-C
СH3-C-COOH H2SO4, to CH3-C
 O -CO2 H
O -CO2 H
Ацетоуксусный эфир
Это этиловый эфир ацетоуксусной кислоты; получается при сложной эфирной конденсации кляйзена.(см.лекции сл.эф)
 Н О
Н О
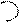




 СН3-С C®C FCH3–C=H–COOC2H5
СН3-С C®C FCH3–C=H–COOC2H5
О Н ОС2Н5 ОН
СН-кислотный центр
Кето-форма(92%) енольная форма 8%
Сравнительно большое кол-во ен.ф образованием сопряж.сист. и наличие внутримолек. Водород связи.
 СН
СН


 Н3С-СН С-ОС2Н5
Н3С-СН С-ОС2Н5
 О :О
О :О
Н…
**Реакции по кето-форме.
[H]



 СН3-С-СН2СООС2Н5 восс-ие CH3CHCH2COOC2H5
СН3-С-СН2СООС2Н5 восс-ие CH3CHCH2COOC2H5
О ОН
 СNH CN
СNH CN

 CH3–C–CH2COOC2H5
CH3–C–CH2COOC2H5
OH
SO3Na
 NaHSO3 CH3–C–CH2COOC2H5
NaHSO3 CH3–C–CH2COOC2H5

 OH
OH
** Реакциипоенольнойформе.
+Br2





 CH3C=CH–COOC2H5 CH3–C–CH–COOC2H5
CH3C=CH–COOC2H5 CH3–C–CH–COOC2H5
OH O Br
Na

 -H2 CH3–C=CHCOOC2H5
-H2 CH3–C=CHCOOC2H5
ONa
+FeCl3 окраш. вфиолет.цвет. продуктреакции.
 +CH3COH
+CH3COH
 -HCl CH3–C=CHCOOC2H5
-HCl CH3–C=CHCOOC2H5
 Ацил-ие OCOCH3
Ацил-ие OCOCH3
Алкилирование

 CH3C=CH–COOC2H5FCH3–C=CHCOOC2H5
CH3C=CH–COOC2H5FCH3–C=CHCOOC2H5
ONa O- анионацетоуксус.эфира

 CH3–C=CHCOOC2H5®CH3–C–CHCOOC2H5
CH3–C=CHCOOC2H5®CH3–C–CHCOOC2H5
О- О основной пр-кт




 CH3–C=CHCOOC2H5+RCl прод С-алкил CH3–C-CH-COOC2H5
CH3–C=CHCOOC2H5+RCl прод С-алкил CH3–C-CH-COOC2H5
 ONa O R
ONa O R

 Прод. О-алкил CH3–C=CHCOOC2H5
Прод. О-алкил CH3–C=CHCOOC2H5
OR
Проведя дальнейшие алкилир.можно заменить и второй атом водорода.
Синтез с ацетоуксусным эфиром. Ацетоуксус.эфир и его произв-ые подвергяются след.расщеплениям:
** кетонному ( при действ.разб.щелочей)


 CH3CCHCOOC2H5 Na OH(разб) CH3–C–CH2COOH to CH3–C–CH3
CH3CCHCOOC2H5 Na OH(разб) CH3–C–CH2COOH to CH3–C–CH3


 O –C2H5OH O -CO2 O
O –C2H5OH O -CO2 O
CH-C-CH2R

 O
O
Метилалкикетон
**кислотному (при дейст.конц.р-р щелочей)
 O
O


 CH3-C-CH-C 2CH3COOK + C2H5OH
CH3-C-CH-C 2CH3COOK + C2H5OH
O R OC2H5 +HCl +RCH2COOK
 KO-H KOH CH3COOH +HCl
KO-H KOH CH3COOH +HCl
RCH2COOH
Аминокислоты
Содержит в своем составе амминогруппу и карбоксильную группу.
Сульфониловая к-та.
 NH2
NH2

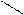
 SO3H
SO3H



 Получение:NH2 N+H3:HSO-4 :NH-SO3H NH
Получение:NH2 N+H3:HSO-4 :NH-SO3H NH
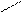
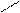
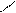






 +H2SO4(k) 180oC
+H2SO4(k) 180oC

 -H2O
-H2O

 H SO3H
H SO3H
N-фенилсульфаминовая к-та.
Основный центр
 |  |


 H2N -S-OHFH3+C SO3-
H2N -S-OHFH3+C SO3-

 Кисл.центр биполярный ион(внутри соль)
Кисл.центр биполярный ион(внутри соль)
Это сильная к-та и образует соли с щелочами.
 | |||
 | |||
 H3N+ - - SO-3 +NaOH H2N - - SO3Na
H3N+ - - SO-3 +NaOH H2N - - SO3Na

 -H2O
-H2O
Из-за биполяр.структуры не об-ет соли с минер.к-ми.
Сульфонил.кислота исп-ся в пр-ве красителей и лекарств.средств,т.е. входит в структуру сульфанид амидов, а именно антибакт.препар.


 NH2 NHCOCH3 NHCOCH3 NHCOCH3 NH2
NH2 NHCOCH3 NHCOCH3 NHCOCH3 NH2







 (CH3CO)2O HOSO2Cl +NH3 +H2O
(CH3CO)2O HOSO2Cl +NH3 +H2O

 ац-ие для сульфохл. Амидирование гидролиз
ац-ие для сульфохл. Амидирование гидролиз



 защиты NH2гр. ацтанилид SO2Cl O=S=O с целью снятия O=S=Oстрептоцид.
защиты NH2гр. ацтанилид SO2Cl O=S=O с целью снятия O=S=Oстрептоцид.
хлорсульфоновая к-та. NH2 защиты NH2
n-ацетамидобензол- это амфотерное соед-е
сульфохлорид.



 Основ.центр
Основ.центр

 H2N- -SO2NHNa +NaOH H2N - - SO2NH2 +HCl H3N+- -SO2NH2 Cl-
H2N- -SO2NHNa +NaOH H2N - - SO2NH2 +HCl H3N+- -SO2NH2 Cl-




 -H2O NH-кисл.центр.
-H2O NH-кисл.центр.
Общие формулы сульфанидамидных препаратов:
NH2


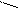

 O=S=O
O=S=O
NH-R
NH2+COOH
**алифатические ( α-, β-,γ)
**ароматические
 - COOH исполь-ся в пр-ве красителей и лек.ср-в
- COOH исполь-ся в пр-ве красителей и лек.ср-в
_ NH2
Онтрониловая к-та.
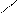

 - COOH
- COOH
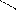 ПАБК
ПАБК
NH2
Способы получения:**действие аммиака на Hal– карб.к-ты.
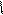
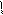


 R-CH-COOH +NH3 R-CHCOONH4 +HCl R-CH-COOH
R-CH-COOH +NH3 R-CHCOONH4 +HCl R-CH-COOH
CH -NH4Cl NH4 NH2
**Восстановительное аминирование оксо к-т.


 R-C-COOH NH3,H2 R-C-COOH R-C-COOH
R-C-COOH NH3,H2 R-C-COOH R-C-COOH



 O NH NH2
O NH NH2
Иминокислота
**Присоед. NH3к α ,β-ненасыщ.к-ам.
β
 R–CH=CH–COOH+NH3®R-CH-CH2COOH
R–CH=CH–COOH+NH3®R-CH-CH2COOH
NH2
**Ароматические получают восстановлением по Зинину соотв. нитробензойных к-т.
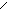
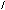 COOH COOH
COOH COOH
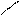



 [H] +H2O
[H] +H2O
 | |||||
 |  | ||||

 NO2 NH2
NO2 NH2
Химические свойства: *Все реакции по –COOH
*Реакции по NH2гр.
Аминокисл –это амф.соед.об-ют соли как с щелочами, так и с к-ми.
*Отнош. к нагрев.позволяют различить α,β,γ-алиф.аминок-ты.
а) α –АК при t-ре межмолек.дегидратируются с образованием дикетопиперазина.
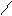
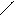 O
O
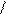
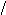
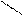
 R-CH-C O
R-CH-C O
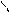
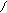 HNH OH R-CH-C
HNH OH R-CH-C
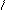
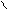 + to HN NH
+ to HN NH
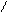

 HNH -2H2O C-CH-R
HNH -2H2O C-CH-R
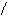
 HO O
HO O
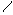 C-CH-R
C-CH-R
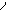 O
O
б) β-АК подвергаются дезаминированию
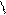
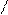 R-CH-CH-COOH to R-CH=CH-COOH
R-CH-CH-COOH to R-CH=CH-COOH
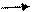 NH2 H -NH3 непред.карб.кислота
NH2 H -NH3 непред.карб.кислота
в) γ-АК дегитратируются внутримолек с об-ем лактама.

 СН2-CH2 CH2-CH
СН2-CH2 CH2-CH
R-CH C=O to R-CH C=O

 HNH OH -H2O NH лактам.
HNH OH -H2O NH лактам.
γ-аминомаслян.к-та(ГАМК)
α-аминомаслян.к-та.(аминолон)
ПАБК входит в состав фолиевой к-ты.
Ее эфиры:этиловый эфир ПАБК(анестезин)
 O
O
 H2N- -C
H2N- -C
 OC2H5
OC2H5
 O
O
 H2N- -C
H2N- -C
 OCH2CH2N(C2H5)2 новокаин
OCH2CH2N(C2H5)2 новокаин

 O
O
H2N- -C

 NHCH2CH2N(C2H5)2 новокаинамид
NHCH2CH2N(C2H5)2 новокаинамид
