Ориентировочная основа действия (ООД) для проведения самостоятельной работы студентов в учебное время
Лабораторная работа«Скорость реакции и энергия активации кислотного гидролиза этилацетата».
Цель работы:определение константы скорости, порядка и энергии активации кислотного гидролиза этилацетата.
Приборы, оборудование:погружной термостат, термометр на 1500С, цифровой термометр, секундомер, магнитная мешалка, штатив, бюретка на 25 мл, мерный цилиндр на 100 мл, пипетки на 5 мл (2 шт.) и 100 мл (1 шт.), коническая колба Эрленмейера на 250 мл с широким горлом (2 шт.), коническая колба Эрленмейера на 250 мл с узким горлом (2 шт.), резиновые пробки 17/22 (2 шт.), короткий стеклянный стакан на 250 мл, воронка.
Реактивы:этилацетат, раствор соляной кислоты С=1моль/л, раствор гидроксида натрия С=0,5моль/л, раствор фенолфталеина ω=1%, дистиллированная вода, лёд.
Выполнение эксперимента
Кислотный гидролиз сложного эфира происходит по уравнению
СН3СООС2Н5+Н2О↔СН3СООН+С2Н5ОН, которое может быть описано кинетическим уравнением реакции I порядка:
(1) 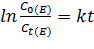 , где С0(Е) – концентрация эфира в момент времени t0
, где С0(Е) – концентрация эфира в момент времени t0
Ct (E) - концентрация эфира в момент времени t. Концентрации эфира могут быть заменены объёмами растворов NaOH, необходимыми для нейтрализации образцов в начале (V0(NaOH) ), во время реакции (V(NaOH) )и после полного превращения (V 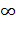 (NaOH) ).
(NaOH) ).
Тогда уравнение (1) принимает вид:
(2) 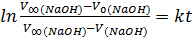 .
.
I группа.
Определение V0(NaOH).
Оттитровать 5 мл раствора соляной кислоты С=1моль/л, отмеренного пипеткой в колбу для титрования, раствором NaOH C=0,5моль/л в присутствии фенолфталеина до бледно - розовой окраски.
V0(NaOH)=V0экс(NaOH) · 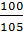
Определение k при комнатной температуре.
В коническую колбу с узким горлом внести пипеткой 100 мл раствора соляной кислоты С=1моль/л, добавить в колбу пипеткой 5 мл этилацетата. Закрыть колбу пробкой, встряхнуть содержимое, засечь время начала реакции и оставить на 10 минут. После этого отобрать пипеткой образец 5 мл и перенести в коническую колбу с широким горлом, в которую налито
100 мл предварительно охлаждённой на ледяной бане дистиллированной воды. Полученную смесь выдержать~2 минуты. Заполнить бюретку раствором гидроксида натрия С=0,5 моль/л и оттитровать содержимое колбы, используя в качестве индикатора фенолфталеин (2 капли), до появления устойчивого (~30 сек.) бледно – розового окрашивания.
Операцию отбора образца в количестве 5 мл повторить с интервалом 10 минут и оттитровывать по вышеописанной методике. Завершить серию измерений через 40 минут после начала реакции.
II группа.
Определение V0(NaOH).
Оттитровать 5 мл раствора соляной кислоты С=1моль/л, отмеренного пипеткой в колбу для титрования, раствором NaOH C=0,5моль/л в присутствии фенолфталеина до бледно - розовой окраски.
V0(NaOH)=V0экс(NaOH) · 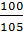
Определение k при t=450С.
В коническую колбу с узким горлом внести пипеткой 100 мл раствора соляной кислоты С=1моль/л. Закрыть колбу пробкой, поместить в термостат, нагреть до t=450С, выдержать 10 минут при этой температуре. Добавить в колбу пипеткой 5 мл этилацетата, засечь время начала реакции и оставить на 10 минут. После этого отобрать пипеткой образец 5 мл и перенести в коническую колбу с широким горлом, в которую налито 100мл предварительно охлаждённой на ледяной бане дистиллированной воды. Полученную смесь выдержать ~ 2 минуты. Заполнить бюретку раствором гидроксида натрия С=0,5 моль/л и оттитровать содержимое колбы, используя в качестве индикатора фенолфталеин (2 капли), до появления устойчивого (~30 сек.) бледно – розового окрашивания.
Операцию отбора образца в количестве 5 мл повторить с интервалом 10 минут и оттитровывать по вышеописанной методике. Завершить серию измерений через 40 минут после начала реакции.
I группа.
II группа.
Определение V 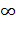 (NaOH).
(NaOH).
Температуру в термостате довести до 700С и тёплый раствор этилацетата с соляной кислотой выдержать при этой температуре в течение 15 минут. Затем отобрать пипеткой 5 мл образца, перенести в колбу с широким горлом, в которую налито 100 мл предварительно охлаждённой на ледяной бане дистиллированной воды, и выдержать ~2 минуты. Затем оттитровать раствором NaOH С=0,5 моль/л, как описано выше.
Оформление результатов эксперимента включает следующие операции:
1. Экспериментальное определение V0(NaOH).
2. Экспериментальное определение объёмов NaOH при комнатной температуре и t=450С.
3. Экспериментальное определение V∞(NaOH).
4. Расчёт средних значений k при комнатной температуре и t=450С по уравнению (2).
5. Расчёт Еа по уравнению
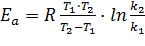 ,
, 
T1 и k1 - значения для комнатной температуры
T2 и k2 – значения для температуры 450С.
