Основные определения и термины. При погружении пластинки металла в водный раствор его соли на границе раздела металл – раствор образуется двойной электрический слой
При погружении пластинки металла в водный раствор его соли на границе раздела металл – раствор образуется двойной электрический слой. Образовавшаяся пограничная разность потенциалов получила название электродного потенциала.
Различают электроды первого и второго рода. Электроды первого рода обратимы относительно одного вида ионов (катионов или анионов), а электроды второго рода – относительно обоих видов ионов раствора.
Примером электрода первого рода является металл, погруженный в раствор, содержащий его ионы, например медный и цинковый электроды в растворах их солей. Они обратимы относительно катионов. Такой электрод можно представить в виде схемы: Мz+ | М. Ему отвечает электродная реакция
Мz+ + z e–↔ М,
где z – число электронов, принимающих участие в процессе.
Потенциал электрода определяется уравнением Нернста:

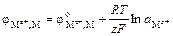
 , (7.1)
, (7.1)
где jо – стандартный (нормальный) электродный потенциал, В; R – универсальная газовая постоянная, Дж/(моль×К); R = 8,314; Т – абсолютная температура, К; z – число электронов, участвующих в реакции; F – постоянная Фарадея, Кл/моль; F = 96485; 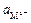 – активность ионов металла в растворе.
– активность ионов металла в растворе.
Электрод второго рода состоит из металла, покрытого слоем его труднорастворимого соединения и погруженного в раствор легкорастворимой соли, содержащий тот же анион, что и малорастворимое соединение, например каломельный и хлорсеребряный электроды. Они обратимы относительно как катиона, так и аниона.
Электрод второго рода записывается в виде схемы Аz– | МА, М. Схема электродной реакции:
МА + z e–↔ М + Аz–.
Потенциал электрода второго рода определяется уравнением
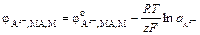 ,(7.2)
,(7.2)
где 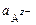 – активность анионов в растворе.
– активность анионов в растворе.
Окислительно-восстановительный электрод состоит из инертного металла (например, платины), погруженного в раствор, содержащий вещества с различной степенью окисления Red и Ox. Металл в такой системе обменивается с участниками окислительно-восстановительной реакции электронами и принимает определенный потенциал при установлении равновесного состояния.
В общем виде схема электрода и уравнение потенциалопределяющей реакции записывается так:
Ox, Red Pt; Ox + z e–↔ Red.
К редокси-электродам относятся в первую очередь электроды, у которых Ox и Red представляют собой ионы, причем электродная реакция состоит в перемене их зарядов. Например, ферри-ферроэлектроду Fe3+, Fe2+ Pt соответствует потенциалопределяющая реакция: Fe3+ + e– ↔ Fe2+.
Потенциал окислительно-востановительного электрода определяется по уравнению
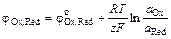 , (7.3)
, (7.3)
где 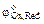 – стандартный окислительно-восстановительный потенциал.
– стандартный окислительно-восстановительный потенциал.
Потенциометрический метод определения рН основан на том, что измеряют ЭДС элемента, состоящего из вспомогательного электрода с известным потенциалом (электрода сравнения) и электрода, потенциал которого зависит от количества водородных ионов (электрода определения). Наиболее часто в качестве электрода с известным потенциалом применяют каломельный, хлорсеребряный и хингидронный электроды. В качестве электрода, потенциал которого зависит от рН, используют водородный, хингидронный и стеклянный. ЭДС такого гальванического элемента равна разности потенциалов двух его электродов и связана определенной зависимостью с активностью водородных ионов, т.е. рН раствора – формулы (7.5 – 7.7). Подставив в соответствующую формулу, выражающую зависимость между ЭДС цепи (Е) и рН раствора, измеренное значение Е, находят искомый рН.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
