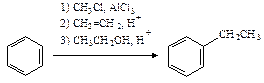Строение бензола. Ароматичность
АРЕНЫ
К аренам относятся соединения, содержащие, по крайней мере, одну бензольную группировку.
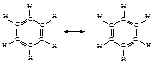
В современной химической литературе понятие “соединение ароматического ряда” означает сходство химических свойств соединения со свойствами бензола и не связаны с запахом соединений.
В соответствии с молекулярной формулой С6Н6 бензол является ненасыщенным соединением и можно ожидать, что для него характерна тенденция вступать в типичные для алкенов реакции присоединения. Однако в условиях, в которых алкен быстро вступает в реакции присоединения, бензол не реагирует или реагирует медленно.
Бензол не вступает в реакции присоединения, в которых разрушилась бы p-электронная система бензольного кольца. Такая устойчивость называется кинетической. Она связана со значительной величиной энергии активации. Вмеcте с тем бензол достаточно легко вступает в реакции замещения. Образующиеся при этом продукты сохраняют специфическую структуру бензола.
Таблица 1.1. Сравнение химических свойств циклогексена и бензола
| Реагент | Бензол 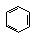 | Циклогексен 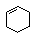 |
| Результат взаимодействия | ||
| КMnO4 (разб. водн. раствор) Br2 (CСl4, в темноте) HВr Н2(Ni) | Не реагирует Не реагирует Не реагирует Медленно гидрируется (100...200 оС, 10 МПа) | Быстро окисляется Быстро присоединяет Быстро присоединяет Быстро гидрируется (25 оС, 0,14 МПа) |
Вывод об устойчивости ароматической системы следует из сравнения теплот гидрирования одного моля 1,3,5-циклогексатриена, содержащего три независимые двойные и три простые связи. Можно ожидать, что теплота гидрирования 1,3,5-циклогексатриена будет равна утроенной теплоте гидрирования одного моля циклогексена: 120,4 ´ 3 =361,2 кДж.
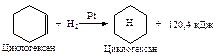
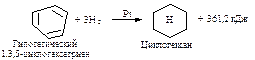
Однако экспериментальная теплота гидрирования одного моля бензола составляет 209 кДж, что на 152 кДж меньше. Следовательно, бензол беднее энергией, чем гипотетический 1,3,5-циклогексатриен. Эта энергия называется энергией резонанса. Стабилизация за счет энергии резонанса является причиной термодинамической устойчивости.
В бензоле каждый атом углерода находится в sp2-состоянии и связан тремя s-связями с двумя атомами углерода и одним атомом водорода. Атомы углерода и водорода лежат в одной плоскости. Четвертый валентный электрон атома углерода находится на 2p-орбитали, перпендикулярной плоскости молекулы. Эти p-орбитали состоят из двух одинаковых долей, одна из которых лежит выше, другая - ниже плоскости кольца. 2р-орбиталь каждого атома углерода перекрывается с 2р-орбиталями обоих соседних атомов углерода. В результате образуется замкнутая шести-p-электронная система в виде двух бубликов, один из которых лежит выше, а другой ниже плоскости правильного шестиугольника (рис. 1.1а).
Благодаря коллективному взаимодействию всех шести p-электронов происходит выравнивание углерод-углеродных связей по длине и кратности: длина всех связей С-С в бензоле (0,1399 нм) является средней между длиной двойной связи в алкенах (0,134 нм) и расчетным значением длины простой связи =С-C=(0,148 нм) (рис. 1.1б). Вторым следствием коллективного p-электронного взаимодействия является электронная и связанная с ней термодинамическая и кинетическая стабилизация.
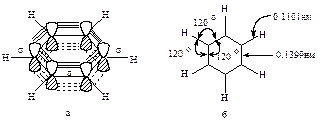
Рис. 1.1.Молекула бензола:
а - перекрывание 2р-орбиталей, образующих p-связи;
б - длины связей и валентные углы в молекуле бензола
Какие свойства должно проявлять вещество для того, чтобы его можно было отнести к ароматическим соединениям? Ароматическимиявляются соединения с молекулярной формулой, указывающей на высокую степень ненасыщенности, которые, однако, не реагируют как ненасыщенные, а вступают в реакции электрофильного замещения с сохранением термодинамически устойчивой ароматической системы.
Условие ароматичности определяет правило Хюккеля: ароматическими свойствами обладает такое соединение, в молекуле которого имеется циклическая система делокализованных p-электронов, число p-электронов должно равняться (4n+2), где n=0,1,2... Для n=1 число сопряженных p-электронов в ароматической системе равно шести. В бензоле как раз имеется шесть p-электронов – ароматический секстет.
Методы синтеза аренов
Ароматизация алканов
Процесс превращения алканов в арены называется дегидроциклизацией, т.к. одновременно включает в себя две реакции: замыкание в цикл линейного углеводорода и отщепление водорода. Из гексана получается бензол, из гептана – толуол, из октана - смесь изомерных ксилолов. Другие арены этим способом не получают.
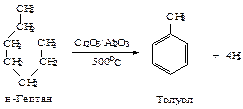
1.3.2. Реакция Вюрца – Фиттига
При взаимодействии галогенаренов с галогеналканами (предпочтительно использовать бромпроизводные) образуются алкилбензолы.
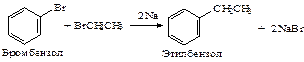
Алкилирование бензола
При действии на бензол алкилирующих агентов (галогеналканов, алкенов, спиртов) в присутствии кислот Льюиса, а также сильных кислот образуется алкилбензол.