Бақылау сұрақтары мен жаттығулар. 1. Титрлеудің эквивалентті бөлімі тұнбаның ерігіштік көбейтіндісіне, температураға және ерітінділердің
1. Титрлеудің эквивалентті бөлімі тұнбаның ерігіштік көбейтіндісіне, температураға және ерітінділердің концентрациясына қалай байланысты?
2. AgNO3 ерітіндісімен: а) 0,100M KI, KBr , KCl ерітінділерін; б) 0,010 М; 0,100M; 1,000M ерітінділерін титрлегенде қай жағдайда титрлеудің эквивалентті бөлімі ең үлкен, қай жағдайда – ең кіші болады?
3. 0,100 М AgNO3 ерітіндісін 0,100 М NH4SCN ерітіндісімен титрлеу қисығын қорытып шығарыңдар.
4. 0,050М NаСІ ерітіндісін 0,050М AgNO3 ерітіндісімен 99,9; 100,0 және 100,1% титрлегендегі рСІ мәнін есептейтін теңдікті қорытып шығарыңдар.
5. 10,00 мл 0,100М KBr ерітіндісіне 0,100 М AgNO3 ерітіндісінің 5,90; ,90;10,0; 10,10; 11,00 мл-ін қосқандағы Br- және Ag+ иондарының концентрацияларын табыңдар.
6. 0,010 М К2CrO4 ерітіндісін 0,100 М AgNO3 ерітіндісімен титрлеу қисығын қорытып шығарыңдар. ЕК(Ag2CrО4) =4,45·10-12.
7. Бромид және хлорид иондарын AgNO3 ерітіндісімен индикаторсыз «тең лайлану» әдісін пайдаланып анықтау негізі. Неге бұл әдіс ең дәл әдіс деп есептеледі?
8. Аргентометриялық әдіспен хлоридтерді титрлегенде К2CrO4 тұзын индикатор ретінде пайдалану неге негізделген?
9. Мор әдісімен хлоридтерді титрлегенде эквивалентті нүктені дұрыс анықтауға сәйкс К2CrO4 концентрациясын есептеп шығарыңыздар.
10. Концентрациясы бірдей NаСІ және NаBr ерітінділерін Фольгард әдісімен титрлегенде қай ионды (Cl-, Br-) анықтау дәлдігі жоғары болады?
11. Иодид – иондарын хлоридтер қатысында титрлегенде қандай адсорбциялық индикаторды пайдаланасыңдар?
12. Хлоридтерді титрлегенде неге эозинді индикатор ретінде пайдалануға болмайды? Адсорбциялық индикатормен титрлегенде ерітінді pН – ның қандай маңызы бар?
13. а) хлориді Мор әдісімен; б) күмісті Фольгард әдісімен; в) бромидті Фаянс әдісімен анықтағанда титрлеудің соңғы нүктесінде жүретін реациялардың теңдеуін жазыңдар.
14. Анализдейтін сынама сілтілік металдың хлориді мен хроматының қоспасы. а) осы қоспадағы хлоридті тікелей титрлеп анықтауға бола ма? б) аргентометриялық әдіспен хлорид пен хроматтың қоспасын анықтауға бола ма?
15. Мор әдісін пайдаланып төмендегі хлоридтердің құрамындағы хлорды анықтауға бола ма: BaCl2; FeCl3; NаСІ + NаС2O4; NаСІ + Nа2SO4 ?
16. Неге Мор әдісімен титрлеуді ерітіндінің pН 7 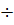 10 аралығында жүргізеді?
10 аралығында жүргізеді?
17. Неге адсорбциялық индикатор фулорецеинді бейтарап, не әлсіз негіздік (pН 7 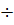 10) ортада пайдаланады?
10) ортада пайдаланады?
18. Хлорид және бромид – иондарын қышқыл ортада титрлеу әдісін таңдап алыңдар.
19. Неге хлоридтерді Фольгард әдісімен анықтағанда индикаторды AgNO3 ерітіндісінің артық мөлшерін құйғаннан кейін ғана қосады?
20. Ерітіндіде AgBr және AgSCN тұнбаларымен тепе – теңдікте жүрген бромид, роданид – иондарының концентрацияларының қатынасы неге тең? ЕК AgBr = 4·10-13; ЕК AgSCN = 1,07·10-12.
21. 0,010 M калий хлориді және иодиді бар ерітіндіге AgNO3 ерітіндісін қосады. Қай тұз – AgСІ (ЕК = 1,78·10-10), не AgІ (ЕК = 8,3·10-17) бірінші болып тұнбаға түседі?
22. Мырышты К4[Fe(CN)6] ерітіндісімен титрлеу реакциясын жазыңдар.
23. Осы теңдікті пайдаланып ZnSO4 пен К4[Fe(CN)6] тұздарының моль×эквивалент мөлшерін табыңдар.
24. Осы титрлеуде эквивалентті нүктені анықтауға ішкі тотығу – тотықсыздандыру индикаторын пайдаланудың негізі неде?
25. Дифениламин индикаторының түсі мырышты К4[Fe(CN)6] –мен титрлегенде және К4[Fe(CN)6] ерітіндісін ZnSO4–пен титрлегенде қалай өзгереді?
26. 0,077 М AgNO3 ерітіндісінің а) СІ арқылы; б) NаСІ арқылы титрін есептеңдер.
27. 0,3000г күмістің құймасы азот қышқылында ерітіледі. Алынған ерітінді титрлеуге 28,30мл 0,100М NH4SCN ерітіндісі жұмсалады. Құймадағы күмістің массалық үлесін есептеңдер?
28. 250,0 мл өлшем колбасында КСІ еріген. Осы ерітіндінің 25,00 мл-ін титрлеуге 34,0 мл 0,105 М AgNO3 ерітіндісі жұмсалса, КСІ-дың массасы неге тең болғаны?
29. 25,0 мл ерітіндіні титрлеуге 20,00 мл 0,100 М AgNO3 жұмсалуы үшін құрамында 75,00% КСІ бар минералдың неше грамын 200,0мл өлшем колбасында еріту керек?
30. Мор әдісімен 0,2332г бромидті титрлеуге 18,77 мл 0,104 М AgNO3 жұмсалады. Анализдеуге қайсы тұз NаBr не KBr алынған?
31. Құйылған 20,00 мл 0,200 М NH4SCN артық мөлшерін титрлеуге 20,00 мл 0,100 М AgNO3 жұмсалуы үшін құрамында 60,00% күміс бар құйманың қандай массасын алу керек?
32. Төмендегі мәліметтерді пайдаланып 250,0 мл ерітіндідегі ВаСІ2 массасын табыңдар: осы ерітіндінің 25,00 мл-не 40,00 мл 0,102М AgNO3 құйылды, артық құйылған AgNO3 титрлеуге 15,00 мл 0,0890 М NH4SCN жұмсалады.
33. 6,700 г. техникалық ВаСІ2 100,0 мл өлшем колбасында ерітіледі. Осы ерітіндінің 25,00мл титрлеуге 23,95 мл AgNO3 (ТAgNO3=0,008048 г/мл) жұмсалады. Үлгідегі ВаСІ2-нің масалық үлесін есептеңдер.
34. 0,8180г таза NаСІ мен NaNO3 қоспасы 200,0 мл өлшем колбасында ерітіледі. Осы ерітіндінің 20,00 мл титрлеуге 18,35 мл AgNO3 (ТAgNO3/ NаСІ=0,003442 г/мл) жұмсалады. Қоспадағы NаСІ мен NаNO3 массалық үлесін табыңдар.
35. 0,1224 г. мырыш тозаңы ерітілген ерітіндіге 50,00мл К4[Fe(CN)6] қосылған (ТК4[Fe(CN)6]=0,008517г/мл). К4[Fe(CN)6]-нің артық мөлшерін титрлеуге 12,28 мл ZnSO4 жұмсалады. К4[Fe(CN)6] ерітіндісінің 1,00 мл-і 1,18 мл ZnSO4 ерітіндісіне эквивалентті. Мырыш тозаңындағы ZnO-нің массалық үлесін есептеңдер.
36. 25,00 мл 0,10М (fэ=1/2) ZnSO4 ерітіндісін титрлеуге жұмсалатын 0,050М (fэ=1/3) К4[Fe(CN)6] ерітіндісінің көлемін есептеңдер.
Тест тапсырмалары
1. Тұндырып титрлеу әдісімен иондарды анықтағанда қандай шарттар сақталуы керек?
1) тұнба іс жүзінде ерімейтін болуы керек;
2) тұнба тез түзілуі қажет;
3) тұнба бетінде иондардың адсорбциясын болдырмау қажет;
4) эквивалент нүктесін анықтау үшін индикатор қажет;
5) барлық шарттар дұрыс.
2. Мор әдісімен хлоридтерді анықтауда титрлеудің аяқталуын қандай белгілер арқылы білуге болады?
1) қызыл-ыш түсті тұнбаның пайда болуынан;
2) қоңыр-қызыл бояудың жоғалуымен;
3) ақ тұнбаның түзілуімен;
4) ақ тұнбаның еруімен;
5) ерітіндінің қызыл түске боялуынан.
3. Хлоридтерді қышқылды ортада күміс нитратымен тура титрлеуге бола ма?
1) болмайды, себебі эквивалент нүктесін анықтауға арналған индикатор жоқ;
2) болмайды, себебі қышқылдық ортада тұнба қиын коагуляцияланады;
3) болмайды, себебі күміс хлориді қышқылда біршама ериді;
4) флуоресцеин индикаторымен титрлеуге болады;
5) титрлеуге болады, егер титрлеудің соңғы нүктесі потенциометрлік немесе амперометрлік әдістермен анықталса.
4. Не себепті хлоридтерді анықтауда адсорбциялық индикатор флуоресцеинді қышқылдық ортада қолдануға болмайды?
1) индикатор қышқылдық ортада ыдырайды;
2) индикатордың адсорбциялануы оның өте үлкен артық мөлшерінде ғана өтеді;
3) индикатор тұнбамен адсорбцияланбайды, себебі қышқылдық ортада индикатордың диссоциациялануы өте аз шамада жүреді;
4) индикатордың тұнбамен адсорбциялануы эквивалент нүктесінен анағұрлым ерте жүреді;
5) барлық себептердің орны бар.
5. Фольгард әдісімен хлоридтерді анықтауға қандай иондар кедергі жасамайды?
1) NO3-; 2) AsO43-; 3) PO43-; 4) CO32-; 5) J-.
6. Қандай жағдайда хлоридтерді Мор әдісімен анықтауға болмайды?
1) нитрат-иондары қатысында;
2) рН = 7 болғанда;
3) рН = 12 болғанда;
4) сульфат-иондары қатысында;
5) натрий иондары қатысында.
7. Хлорды Мор әдісімен қандай хлоридтер ерітіндісінде анықтауға болады?
1) BіCl3; 2) MnCl2; 3) HgCl2; 4) NH4Cl; 5) CaCl2.
8. Мор әдісімен хлорды анықтаған кездегі индикатордың ролін көрсететін дұрыс жауапты табыңыз:
1) күміс иондарының артық мөлшері хромат ионымен қызыл-ыш т‰стҢ тұнба түзеді;
2) хромат-ионы күміс ионымен қызыл-ыш түстес ерітінді береді;
3) эквивалентті нүктеде күміс хлориді күміс хроматына айналады және тұнба үстіндегі ерітінді өз түсін өзгертеді;
4) күміс хлоридінің тұнбасы хромат иондарын адсорбциялайды және өзінің түсін өзгертеді;
5) дұрыс жауап келтірілмеген.
9. Не себепті хлоридтерді Мор әдісімен анықтағанда индикаторды қышқылдық ортада қолдануға болмайды?
1) күміс хлоридінің тұнбасы калий хроматын адсорбциялайды;
2) күміс хроматының тұнбасы күміс бихроматына айналады;
3) күміс хроматының аса қаныққан ерітіндісі түзіледі;
4) күміс хроматы қышқылда жақсы ериді;
5) дұрыс жауап келтірілмеген.
10. Тұндырып титрлеу қисығындағы күрт ауытқу шамасы ең көп дәрежеде неге тәуелді болады?
1) тұнбаның ерігіштік көбейтіндісі мен әрекеттесетін ерітінділер концентрациясы шамаларына;
2) ерітінділер концентрациясына;
3) титрлеу жылдамдығына;
4) индикаторды таңдап алуға;
5) ерітінді температурасына.
11. Аргентометрлік тұндыру әдісі бойынша титрлегенде қандай тұнбаның түзілуі қолданылады?
1) AgCl; 2) Fe(OH)3; 3) CaSO4; 4) PbJ2; 5) Ag2S.
12. Мор әдісімен аргентометрлік титрлеуде қандай индикатор қолданылады?
1) K2Cr2O7; 2) K2CrO4; 3) PbCrO4; 4) Ag2CrO4; 5) Ag2Cr2O7.
13. Төменде келтірілген қосылыстардың қайсысы Фольгард әдісінде индикатор ретінде қолданылады?
1) (NH4)2Fe(SO4)2.6H2O; 2) NH4Fe(SO4) 2.12H2O + HNO3 конц.;
3) FeSO4; 4) K3[Fe(CN)6]; 5). K4[Fe(CN)6].
14. Адсорбциялық индикаторларды қолдануда реакция өнімінің қандай түрі қолайлы деп есептелінеді?
1) аморфты;
2) ұсақ кристалды;
3) ірі кристалды;
4) аморфты-кристалды;
5) дұрыс жауап келтірілмеген.
15. Төменде көрсетілген ерітінділердің қайсысын AgNO3 ерітіндісімен титрлегенде титрлеу қисығының күрт өзгеретін (эквивалентті) бөлігі ең үлкен болады?
1) 1 моль/л NaCl; 2) 0,1 моль/ л NaBr; 3) 0,1 моль/л NH4Cl;
4) 0,1 моль/л KІ; 5) 1 моль/л KІ.
16. Мырыш тұзы ерітіндісін K4[Fe(CN)6] ерітіндісімен титрлеуді қандай ортада жүргізеді?
1) аммиакты ерітіндіде;
2) азотқышқылды ерітіндіде;
3) сұйытылƒан күкірт қышқылды ерітіндіде;
4) рН>9 буферлі ерітіндіде;
5) ерітінді құрамының маңызы жоқ (әсер етпейді).
17. Мырыш тұздарын K4[Fe(CN)6] ерітіндісімен титрлеуде қандай индикатор қолданылады?
1) фенолфталеин; 2) ксиленолды қызғылт; 3) K3[Fe(CN)6];
4) дифениламин; 5) K3[Fe(CN)6] + дифениламин.
18. Мырышты K4[Fe(CN)6] ерітіндісімен титрлеуде индикатор ретінде дифениламиннің азотқышқылды ерітіндісін қолдануға бола ма?
1) титрлеуді кез-келген қышқыл ерітіндісінде жүргізуге болады;
2) болмайды, себебі азотқышқылды ерітінділерде ферроцианид мырыш (ІІ) иондарымен тұнба түзбейді;
3) болмайды, себебі азотқышқылды ортада ферроцианид мырыш-иондарымен құрамы белгісіз тұнба түзеді;
4) болмайды, себебі дифениламин нитрат-иондары әсерінен көк түске боялады;
5) дұрыс жауап келтірілмеген.
Тарау
