Рассмотрим примеры написания некоторых реакций гидролиза солей. Федеральное государственное образовательное Учреждение высшего образования
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
Федеральное государственное образовательное Учреждение высшего образования
«Московский государственный университет технологий и управления имени
К.Г. Разумовского (Первый казачий университет)»
Донской казачий государственный институт пищевых технологий и экономики
(филиал) ФГБОУ ВО «МГУТУ имени К.Г.Разумовского (ПКУ)»
Н.П. ВАССЕЛЬ
Методические указания и задания для выполнения самостоятельной работы по неорганической химии
Ростов - на - Дону
Печатается по решению кафедры химии и биологии ДКГИПТиЭ (филиала) МГУТУ в г. Ростове-на-Дону
Протокол № 8 от 22.04.2016г
Перечень заданий для каждого варианта приведен в таблице 1.
Таблица 1
| Номер варианта | Номера вопросов | ||||
Вассель Н.П.
Неорганическая химия. Методические указания и задания по выполнению самостоятельной работы по неорганической химии. Ростов н/Д: электронная версия, 2016.- 18с.
Методические указания и задания по выполнению самостоятельной работы предназначены для студентов бакалавриата по направлениям подготовки: 19.03.02. 19.03.04, 38.03.07.
Требования к оформлению самостоятельной работы
Работа состоят из 4 заданий. Вариант определяется по последней цифре шифра студенческого билета или зачётной книжки. Например, если последняя цифра шифра 1 то следует выполнять 1-ый вариант заданий, если 0, то – вариант 0.
Самостоятельная работа выполняется в отдельной тетради ясным и разборчивым почерком. Ответ на теоретический вопрос должен быть подробным, однако его объём не должен превышать двух-трех страниц ученической тетради.
Ответы на вопросы надо искать в следующей литературе.
1. Гельфман М. И., Юстратов В. П. Химия. СПб., М., Краснодар, Лань, 2008
2. Вассель Н.П. Неорганическая химия: Учебно-методическое пособие для самоподготовки. Ростов н/Д, 2001.
3. Вассель Н.П. Неорганическая химия. Конспект лекций. Ростов н/Д: электронная версия, 2016.- 28с.
4. Вассель Н.П. Неорганическая химия. Лабораторный практикум. Ростов-на-Дону: электронная версия, 2016. – 46с.
Задания к самостоятельной работе по неорганической химии
Строение атомов элементов
10 . На основании распределения электронов внешнего знергетического уровня по квантовым ячейкам в нормальном и возбужденном состоянии определите возможные валентности атомов указанных элементов углерода, серы.
Химическая связь. ПСЭ и изменение некоторых свойств элементов и их химических соединений
Оределите окислитель и восстановитель в следующей реакции, исходя и положения элемента в ПСЭ.
20. Cl2 + S + H2O.
Ионные реакции обмена. Гидролиз солей.
30. В какой цвет будет окрашена лакмусовая бумажка в водных растворах хлорида аммония, карбоната калия, нитрата натрия? Составьте молекулярные и ионно-молекулярные уравнения происходящих реакций.
Окислительно-восстановительные (о/в) реакции
40. В реакции между растворами дихромата и йодида калия в сернокислой среде, используемой при определении общего количества ароматических веществ в пищевых продуктах.
Теоретические основы разбора заданий
СТРОЕНИЕ АТОМА
Правило записи электронных формул
1. Порядковый номер элемента равен заряду ядра и числу электронов в электронной оболочке атома элемента.
2. Номер периода, в котором находится элемент, определяет число энергетических уровней в электронной оболочке атома.
3. Номер группы и принадлежность к подгруппе (главная, побочная) определяет число и распределение валентных электронов.
В зависимости от того, на какой энергетический подуровень попадает последний электрон при последовательном возрастании порядкового номера, элементы ПСЭ делятся на 4 электронных семейства: s-, р-, d- и f-элементы (исключением являются d-элементы Zn, Cd, Hg, у которых идет восстановление s-подуровня).
Основная цель электронных формул – возможность предсказания и объяснения на их основе свойств элементов и свойств соединений, которые они образуют.
Пример .Составьте электронные формулы для атома с порядковыми номерами 16
Ответ• Элемент с порядковым номером 16 – это сера, находится в третьем периоде, шестой группе. Следовательно, 16 электронов расположены на трех его энергетических уровнях. Электронная формула для атомов серы:
16S 1s2 2s2 2p6 3s2 3p4.
Так как последний электрон поступает на р-подуровень, сера – р-элемент.
16S 1s22s22p63s23p4 16S* –3s23p33d1
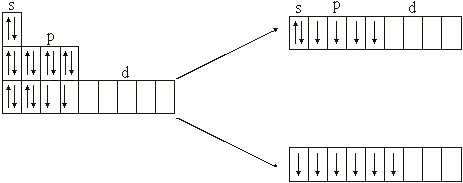
16S* –3s13p33d2
Химическая связь. ПСЭ и изменение некоторых свойств элементов и их химических соединений
Пример 1.Как и почему изменяются кислотно-основные и окислительно-восстановительные свойства кислот в ряду: НСlO — НСlО2 — НСlO3 — НСlO4?
Ответ:Изменение свойств в ряду кислородных кислот хлора можно выразить схемой:
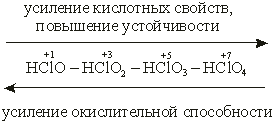
С увеличением степени окисления хлора устойчивость его кислородных кислот растет, а их окислительная способность уменьшается. Наиболее сильный окислитель – хлорноватистая кислота, наименее сильный – хлорная кислота.
Напротив, сила кислородных кислот хлора возрастает с увеличением его степени окисления. (С позиций теории электролитической диссоциации – легкость отщепления иона водорода.) Из всех гидроксидов хлора самая слабая кислота – хлорноватистая, самая сильная – хлорная. Это объясняется тем, что при возрастании степени окисления элемента (хлора) увеличивается заряд иона, что усиливает его притяжение к иону О2– и тем самым затрудняет диссоциацию гидроксида по типу основания. Вместе с тем усилится взаимное отталкивание одноименно заряженных ионов– хлора и водорода, что облегчит диссоциацию по кислотному типу. Таким образом, с увеличением степени окисления элемента усиливаются кислотные свойства и ослабевают основные свойства образуемого этим элементом гидроксида.
Ионные реакции обмена
Реакции, протекающие между растворенными в воде веществами за счет обмена составляющих их ионов, называются ионными реакциями обмена.
Такие реакции протекают необратимо, если образуются:
1) осадок или газообразное вещество;
2) малодиссоциированные соединения.
При написании реакций ионного обмена следует составить:
а) молекулярное уравнение, в котором все исходные вещества и продукты реакции записываются в виде молекул.
б) полное ионное уравнение, в котором все молекулы сильных электролитов записываются в виде ионов, а молекулы слабых электролитов (в том числе и Н2О) и неэлектролитов – в виде молекул.
в) сокращенное ионное уравнение, которое получают из полного ионного уравнения, сокращая, слева и справа, одинаковые частицы.
Продукты реакции ионного обмена образуются за счет электростатического притяжения положительно заряженных частиц одной молекулы и отрицательно заряженных частиц другой.
Рассмотрим примеры написания некоторых реакций ионного обмена.
1. Реакции, протекающие за счет образования малорастворимых веществ:
хлорид меди + фосфат калия
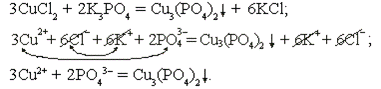 ;
;
Реакция необратима за счет образования не растворимого в воде фосфата меди.
2. Реакции, протекающие за счет образования газообразных веществ:
соляная кислота + гидросульфид бария
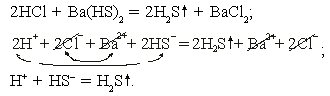
Реакция необратима за счет образования газообразного вещества сероводорода.
3. Реакции, протекающие за счет образования слабодиссоциирующих веществ:
а) ацетат натрия + соляная кислота
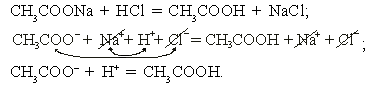
Реакция необратима за счет образования слабодиссоциирующего вещества – уксусной кислоты.
б) гидроксид алюминия + гидроксид натрия
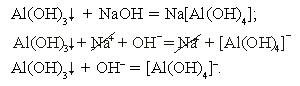
Растворение осадка гидроксида алюминия происходит в избытке щелочи (за счет амфотерных свойств). Реакция необратима за счет образования слабого электролита – комплексного иона [Al(OH)4]–.
По аналогии реакция протекает с гидроксидами сурьмы (III), хрома (III).
Гидролиз солей.
Для правильного ответа на вопросы этой темы необходимо помнить, что:
– Гидролизу подвергаются соли, образованные:
а) слабым основанием, сильной кислотой (рН < 7);
б) слабой кислотой, сильным основанием (рН > 7);
в) слабым основанием, слабой кислотой (рН = 7).
– К сильным основаниям относятся основания, образованные щелочными, щелочноземельными (Ca, Sr, Ba) металлами. К сильным кислотам относятся кислоты с Кд > 10–1 – 10–2 (например: H2SO4, HNO3, HCl, HI, HIO3 и др. ).
– Гидролизу подвергаются только растворимые в воде соли.
– Гидролиз следует рассматривать как реакцию ионного обмена между ионами соли и полярным растворителем – водой (представляющей собой диполь Н+– ОН–).
– В результате гидролиза образуются малодиссоциирующие продукты.
– Гидролиз большинства солей – процесс обратимый. Необратимому гидролизу с образованием осадков и выделением газа подвергаются карбонаты и сульфиды некоторых металлов (Аl3+, Сг3+ и др.).
– Процесс обратимого гидролиза многозарядных ионов протекает в большинстве случаев только по первой ступени из-за накопления в растворе Н+ или ОН–, приводящих к сдвигу равновесия влево.
– В реакциях обратимого гидролиза с одним гидролизующимся ионом – слабым составляющим соли – взаимодействует только одна молекула воды.
Рассмотрим примеры написания некоторых реакций гидролиза солей.
Соли образованные сильным основанием и слабой кислотой, т.е. соли типа KCN, CH3COONa, Na2CO3, K2CO3, Na2S, CaS, Na2SO3 и т.п.
KCN + HOH 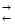 HCN + KOH
HCN + KOH
CN-– + HOH 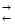 HCN + OH–
HCN + OH–
Раствор приобретает щелочную реакцию, т.е. pH > 7.
Соли, содержащие многозарядные ионы, гидролизуются по стадиям:
На первой стадии образуется кислая соль:
Na2CO3 + HOH 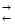 NaHCO3 + NaOH;
NaHCO3 + NaOH;
CO32- + HOH 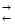 HCO3-+OH-
HCO3-+OH-
На второй стадииобразуются молекулы кислоты:
NaHCO3 + НOH 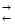 H2CO3 + NaOH;
H2CO3 + NaOH;
HCO3- + HOH 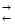 Н2CO3 + OH-
Н2CO3 + OH-
Считают, что при стандартных условиях и умеренном разбавлении раствора гидролиз солей протекает по первой стадии.
Соли образованные слабым основанием и сильной кислотой.Сюда относятся NH4Cl, NH4NO3, ZnCl2, CuSO4, Mn(NO3)2, AlCl3 и др. В этом случае в процессе гидролиза главную роль играет катион соли. Анион же последней не связывает водородных ионов воды и практически в реакции гидролиза не участвует
NH4Cl + HOH 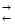 NH4OH + HCl;
NH4OH + HCl;
NH4++ HOH 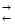 NH4OH + H+;
NH4OH + H+;
раствор приобретает кислую реакцию, т.е. pH < 7.
Как и в предыдущем случае, соли многозарядных ионов гидролизуются по стадиям.
На первой стадии образуются основная соль:
Mn(NO3)2 + HOH 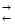 MnOHNO3 + HNO3;
MnOHNO3 + HNO3;
Mn2+ + HOH 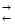 MnOH+ + H+ и далее.
MnOH+ + H+ и далее.
На второй стадии образуются молекулы основания:
MnOHNO3 + HOH 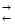 Mn(OH)2 + HNO3;
Mn(OH)2 + HNO3;
MnOH+ + HOH 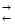 Mn(OH)2 + H+.
Mn(OH)2 + H+.
Как правило, вторая стадия гидролиза незначительна.
Соли образованные слабым основанием и слабой кислотой. Сюда можно отнести такие соли, как NH4CN, CH3COONH4. В этом случае в гидролизе участвуют и катионы, и анионы; они связывают и водородные, и гидроксид-ионы воды, образуя слабые электролиты (слабые кислоты и слабые основания). Соли этого типа полностью разлагаются водой:
NH4CN + HOH 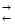 NH4OH + HCN;
NH4OH + HCN;
NH4+ + CN– + HOH 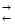 NH4OH + HCN.
NH4OH + HCN.
Соли многозарядных ионов гидролизуются ступенчато:
Необратимому гидролизу с образованием нерастворимых в воде гидроксидов (или гидроксосолей) и выделением газа подвергаются сульфиды и карбонаты некоторых металлов (Cr3+, Al3+, Fe3+, Co2+, Cd2+, Zn2+, Mn2+, Ni2+ и др.).
Например:
Al2S3 + 6H2O = 2Al(OH)3↓ + 3H2S;
2CdCO3 + H2O = (CdOH)2CO3↓ + CO2;
Cr2(CO3)3 + 3H2O = 2Cr(OH)3↓ + 3CO2.
Соли, образованные сильной кислотой и сильным основанием, гидролизу не подвергаются: NaCl, KJ, Na2SO4, Ba(NO3)2 и т. д.
Окислительно-восстановительные (о/в) реакции
При решении задач этого раздела необходимо помнить, что:
– Только окислительные свойства проявляют вещества, в которых элемент находится в высшей степени окисления.
– Только восстановительные свойства проявляют вещества, в которых элемент находится в низшей степени окисления.
– Двойственные свойства проявляют вещества, в которых элемент находится в промежуточной степени окисления.
– Для правильного подбора коэффициентов в о/в реакции необходимо составлять баланс, в котором сумма отданных электронов должна быть равна сумме принятых электронов.
– Для реакций, протекающих в водном растворе, необходимо составлять электронно-ионный баланс.
– При составлении электронно-ионного баланса в виде ионов записывают молекулы сильных электролитов (большинство растворимых в воде неорганических солей, сильных кислот и оснований, комплексные соли-электролиты); в виде молекул записывают молекулы слабых электролитов (нерастворимые в воде соли, слабые кислоты и основания), неэлектролиты (молекулы большинства органических соединений, оксиды, комплексные соли-неэлектролиты, газы).
Чтобы составить уравнение окислительно-восстановительной реакции, необходимо знать, от каких и к каким из участвующих в реакции атомов, молекул или ионов переходят электроны, т.е. определить окислитель и восстановитель
Пример. Расставить коэффициенты в уравнении реакции:
KMnO4 + H2S + H2SO4 → MnSO4 + S + K2SO4 + H2O.
• Пишем схему реакции и проставляем степени окисления элементов.
• Видно, что степень окисления изменилась у марганца и серы: марганец был +7, стал +2, сера была –2, стала 0.
• Отражаем эти изменения степени окисления в электронных уравнениях и определяем элемент-окислитель и элемент-восстановитель:
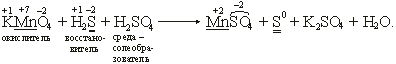
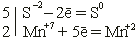
K2S – восстановитель, KMnO4 – окислитель.
Слева от электронных уравнений проводим вертикальную черту и проставляем коэффициенты, соответствующие числу электронов, отданных восстановителем и принятых окислителем. Множители перед вертикальной чертой «5» и «2» и есть основные коэффициенты перед окислителем и восстановителем.
• Переносим найденные основные коэффициенты при восстановителе и окислителе в заданную схему реакции:
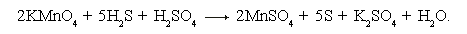
• Находим коэффициенты при других реагирующих веществах в следующем порядке: металлы, кислотные остатки (или неметаллы), водород, кислород.
• Правильность подбора коэффициентов проверяем равенством атомов кислорода в обеих частях уравнения:
2KMnO4 + 5H2S + 3H2SO4 = 2MnSO4 + 5S + K2SO4 + 8H2O.
