Робота 1.1. Дослідження кінетики розкладу пероксиду водню у водному розчині за сталої температури.
Мета роботи: визначити газометричним методом порядок реакції розкладу пероксиду водню у водному розчині та дослідити вплив концентрації каталізатора КІ на швидкість цього процесу.
Пероксид водню у водному розчині самочинно повільно розкладається за рівнянням:
2Н2O2 = 2Н2O + О2 . (1.14)
Наявність у розчині катіонів, аніонів, деяких органічних сполук, які є каталізаторами, значно прискорює цей процес.
За перебігом реакції спостерігають, вимірюючи через певні проміжки часу від початку реакції об’єм кисню, що виділяється (газометричний метод). Схему приладу для дослідження кінетики реакції (1.14) зображено на рис. 1. Порівняльну лійку 4 спочатку закріплюють у штативі так, щоб рівень води у газовій бюретці 3 був на ~ 2 – 2,5 см вище за позначку "0".
В окремі коліна реакційної пробірки 1 наливають піпетками або циліндрами указані викладачем об’єми розчинів пероксиду водню та каталізатора KI. Щільно закривають двоколінний реактор пробкою, до якої прикріплено гумову трубку, що сполучена з газовою бюреткою. Рівень води у газовій бюретці незначно знизиться.
Пробірку занурюють у кристалізатор з водою 2, який виконує роль термостата. Нахиляючи пробірку, змішують розчини пероксиду та каталізатора так, щоб їх суміш повністю опинилась в одному з колін реактора. Через деякий час розчин стане насиченим киснем, який утворюється внаслідок розкладу Н2О2, газ почне виділятися з пробірки і рівень води в газовій бюретці знижуватиметься.
 Звільняють зі штативу порівняльну лійку і, тримаючи її поряд з газовою бюреткою, поступово опускають услід за рівнем води в бюретці. Щоб тиск газу в бюретці в будь-який момент часу відповідав зовнішньому, рівні води в бюретці та порівняльній лійці повинні бути однаковими.
Звільняють зі штативу порівняльну лійку і, тримаючи її поряд з газовою бюреткою, поступово опускають услід за рівнем води в бюретці. Щоб тиск газу в бюретці в будь-який момент часу відповідав зовнішньому, рівні води в бюретці та порівняльній лійці повинні бути однаковими.
Секундомір вмикають тоді, коли рівень води в бюретці досягне позначки "0". Далі записують поточний час від початку реакції (пуску секундоміра), що відповідає виділенню об’єму кисню, який кожного наступного разу збільшується на 3 см3.
Отримавши таким чином 12 – 14 значень загального об’єму газу для відповідних проміжків часу, порівняльну лійку знов закріплюють на штативі так, щоб рівень води в ній був значно нижчий за рівень води у бюретці, і чекають повного розкладу пероксиду. Реакція вважається закінченою тоді, коли рівень води в газовій бюретці вже не змінюється.
Після завершення реакції для визначення кінцевого (максимального) об’єму газу, що виділився, порівняльну лійку розміщують поруч з бюреткою так, щоб вода в них була на одному рівні, і вимірюють об’єм О2 в бюретці (  ). Експериментальні дані записують у табл. 1.1 (див. звіт).
). Експериментальні дані записують у табл. 1.1 (див. звіт).
За даними табл. 1.1 будують графік  . Оскільки зазначена залежність не є прямолінійною, то нульовий порядок, для якого притаманна така зміна концентрації продукту з часом, виключається. Тому за методом підстановки перевіряють перший порядок реакції, використовуючи рівняння (1.5). Враховуючи те, що у формулі (1.5) початкова концентрація пероксиду водню
. Оскільки зазначена залежність не є прямолінійною, то нульовий порядок, для якого притаманна така зміна концентрації продукту з часом, виключається. Тому за методом підстановки перевіряють перший порядок реакції, використовуючи рівняння (1.5). Враховуючи те, що у формулі (1.5) початкова концентрація пероксиду водню  пропорційна
пропорційна  , а х – об’єму кисню
, а х – об’єму кисню 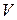 , який виділився за певний проміжок часу, константи швидкості обчислюють за рівнянням:
, який виділився за певний проміжок часу, константи швидкості обчислюють за рівнянням:
 . (1.15)
. (1.15)
Константи швидкості розраховують для 5 – 6 точок середньої частини кінетичної кривої  (за вказівкою викладача). Сталість одержаної за рівнянням (1.15) константи швидкості реакції вказує на те, що розклад пероксиду водню перебігає за першим порядком. Обчислюють середнє значення
(за вказівкою викладача). Сталість одержаної за рівнянням (1.15) константи швидкості реакції вказує на те, що розклад пероксиду водню перебігає за першим порядком. Обчислюють середнє значення  .
.
Середнє значення константи швидкості можна визначити також графічно як тангенс кута нахилу прямої в координатах  .
.
Звіт
1. Дані експерименту:
 4 см3;
4 см3;  см3;
см3;  моль/дм3.
моль/дм3.
Таблиця 1.1. Залежність об’єму кисню, що виділився внаслідок перебігу реакції, від часу
 , см3 , см3 | |||||||||||||
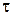 , с , с |
 см3.
см3.
2. Обчислення концентрації КІ у реакційній суміші:  моль/дм3.
моль/дм3.
3. Побудова за даними табл. 1.1 графіка  .
.
4. Розрахунки для табл. 1.2:
Таблиця 1.2. Дані для визначення константи швидкості та порядку реакції
| № виміру | Час з початку реакції 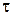 , с , с | Об’єм газу  см3 см3 |  | k, с -1 |
| × |
 с -1
с -1
5. Побудова за даними табл. 1.2. графіка  та обчислення
та обчислення
за ним  с -1.
с -1.
6. Кінетичне рівняння реакції:
7. Визначення часу напівперетворення:
а) за формулою  с;
с;
б) за графіком  :
:  с.
с.
8. Побудова графіка  за даними табл. 1.3 та визначення константи швидкості реакції без каталізатора:
за даними табл. 1.3 та визначення константи швидкості реакції без каталізатора:  с -1.
с -1.
Таблиця 1.3. Залежність константи швидкості реакції від концентрації
каталізатора
 , моль/дм3 , моль/дм3 | |||||
 , с -1 , с -1 |
9. Розрахунок питомої активності каталізатора:

 .
.
10. Висновок.
ЛІТЕРАТУРА: [1, с. 523 – 527, 533 – 542, 616 – 623; 2, с. 290 – 293, 297 – 310, 427 – 433; 3, с. 318 – 329, 401 – 406; 4, с. 322 – 338, 344, 365 – 367; 5, с. 195 – 201, 204 – 205; 6, с. 217 – 225, 229 – 233; 8, с. 43 – 46].
