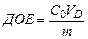Обработка результатов эксперимента
Выполнение работы
1. произвести анализ исходного раствора соли металла (по заданию преподавателя).
2. Налить в колонку раствор соли металла. Осторожно открыть кран так, чтобы раствор проходил через ионит со скоростью 3 – 4 мл в минуту (примерно 1 капля в секунду).
3. Фильтрат собирать в мерный цилиндр порциями по 10 мл.
4. Каждую порцию анализировать на содержание в ней иона металла.
5. Пропускать раствор соли металла через колонку продолжать до тех пор, пока объем трилона Б на титрование порции из колонки не станет равным объему трилона Б при титровании исходной соли металла.
Примечание: при правильном выполнении работы на титрование 3-5 первых проб не должно расходоваться более 0,3 – 0,5 мл раствора трилона Б
Протокол лабораторной работы
= название соли металла и ее химическая формула
= ориентировочное значение концентрации соли металла, указанное на емкости с раствором
= масса катионита в колонке
= объем аликвоты при титровании исходного раствора соли металла Va
= Объем раствора трилона Б, израсходованного на титрование исходного раствора
VТрБ, 1 = ………….мл
VТрБ, 2 = ………….мл
VТрБ, ср = ………….мл
= концентрация раствора трилона Б
=Зависимость объема трилона Б от объема профильтрованного через катионит раствора соли металла
| № | Объем соли металла, мл | Объем трилона Б, мл |
| 20 (10+10) | ||
| … | … |
Проведение анализа содержания металла в пробе.
Анализ содержания меди (2+)
ü отбирают мерной пипеткой в конические колбы аликвоту объемом 10 мл.
ü приливают дистиллированную воду до объема 20-30 мл;
ü добавляют по каплям при перемешивании аммиак до получения прозрачного синего раствора,
ü добавляют немного сухого индикатора «мурексид»;
ü титруют раствором трилона Б до перехода окраски индикатора в эквивалентной точке от желтой (хаки) к сиренево-фиолетовой.
Анализ содержания кобальта и никеля
ü отбирают мерной пипеткой в конические колбы аликвоту объемом 10 мл.
ü приливают дистиллированную воду до объема 20-30 мл;
ü с помощью мерного цилиндра добавляют хлорид аммония 5 мл,
ü добавляют немного сухого индикатора «мурексид»
ü титруют раствором трилона Б до переход окраски индикатора в эквивалентной точке от желтой к фиолетовой.
ü Желтую окраску раствора поддерживают аммиаком: если в процессе титрования раствор краснеет, то добавить несколько капель аммиака.
Обработка результатов эксперимента
1. заполнить таблицу:
| № | V(MeSO4), мл | V(трилона Б), мл | С(MeSO4), моль/л |
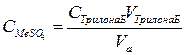
2. Построить график выходной кривой ионообменной адсорбции
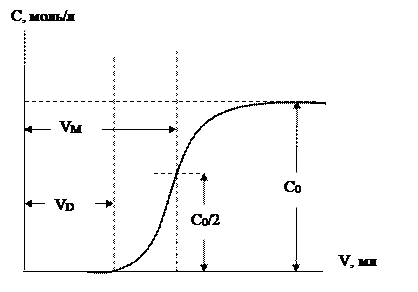
3. Вычислить полную обменную емкость ионита по уравнению:
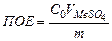 ,
,
где С0 – исходная концентрация иона металла в растворе, моль/л; VМ – объем раствора, соответствующий половине исходной концентрации и определяемый графически по выходной кривой, мл; m – масса сухого ионита, г.
4. Вычислить динамическую обменную емкость до проскока по уравнению: