Разработка энантиоселективных тсх-пластин с иммобилизованным макроциклическим гликопептидным антибиотиком эремомицином
Попова Е.А.
Санкт-Петербургский государственный университет,
Санкт-Петербург, Россия.
Студент V курса.
Научный руководитель: Карцова А.А., Малахова И.И.
В работе предлагается способ разделения энантиомеров с использованием иммобилизации хирального селектора в состав неподвижной фазы в условиях ТСХ. Иммобилизованные макроциклические гликопептидные антибиотики, к которым относятся ванкомицин, тейкопланин, ристоцетин А, авопарцин и др., успешно зарекомендовали себя в качестве компонентов хиральных фаз при разделении энантиомеров методом ВЭЖХ. Высокая энантиоселективность таких сорбентов связана с наличием в их структуре различных по строению фрагментов, способных к многоточечным взаимодействиям с разделяемыми соединениями в различных растворителях. В качестве хирального селектора нами выбран макроциклический антибиотик эремомицин.
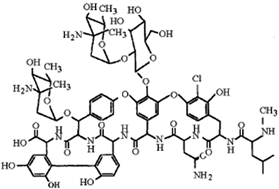
Структурная формула эремомицина.
Модификацию ТСХ-пластин (Sorbfil ПТСХ-П-В) проводили в две стадии: на первой – силикагель активировали эпоксигруппами, на второй – к эпоксиактивированному силикагелю прививали хиральный селектор. В качестве объектов для выявления энантиоселективных свойств полученных ТСХ-пластин выбраны модельные системы α-аминокислот и профенов. Оптимизированы условия иммобизизации эремомицина на силикагеле, найдены условия разделения оптических изомеров ряда α-аминокислот, кетопрофена, фенопрофена и флурбипрофена.
РАЗДЕЛЕНИЕ ЭНАНТИОМЕРОВ БИОЛОГИЧЕСКИ АКТИВНЫХ СОЕДИНЕНИЙ (АМИНОКИСЛОТ, НЕСТЕРОИДНЫХ ПРОИВОВОСПАЛИТЕЛЬНЫХ СРЕДСТВ) В УСЛОВИЯХ ВЫСОКОЭФФЕКТИВНОЙ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ С ДЕНСИТОМЕТРИЧЕСКИМ ДЕТЕКТИРОВАНИЕМ
Протасова И.Д.
Санкт-Петербургский государственный университет,
Санкт-Петербург, Россия.
Студент V курса.
Научный руководитель: Карцова А.А., Объедкова Е.В.
Многие фармацевтические препараты являются рацематами. При этом положительный терапевтический эффект оказывает только один из энантиомеров; другой - может быть неактивным или обладать в конкретных условиях тератогенным действием. Для контроля энантиомерной чистоты фармацевтических препаратов наиболее широкое применяются методы капиллярного электрофореза (КЭ) и высокоэффективной жидкостной хроматографии (ВЭЖХ), что, в свою очередь, требует дорогостоящего оборудования.
В работе выявлены возможности использования различных хиральных селекторов (циклодекстрины, аминокислоты, макроциклические антибиотики) для экспрессного разделения энантиомеров нестероидных противовоспалительных препаратов (ибупрофен, кетопрофен, кеторолак) и аминокислот методом высокоэффективной ТСХ с денситометрическим детектированием. Оптимизированы условия разделения рацематов (состав элюирующих систем, концентрация модификаторов и способ модификации). Определены пределы обнаружения, эффективность и факторы разрешения. Выявлены возможности использования принципа лигандного обмена для ВЭТСХ-хирального разделения аналитов. Результаты сопоставлены с соответствующими данными лигандообменного капиллярного электрофореза (ЛОКЭ). Разработана процедура пробоподготовки реальных образцов (фармацевтические препараты, биологические жидкости) и проведен их анализ методом ВЭТСХ.
