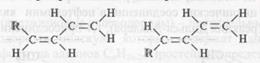
Химиялық қасиеттері
Алкендердің химиялық қасиеттері олардағы қос байланыс бойынша анықталады (1-кесте). Оның құрамына кіретін π–байланыс оңай бұзылып, әлсіздеу π– байланыстың әсерінен алкендерге тән қосылу, сонымен қатар изомерлену және тотығу (оның ішінде жану реакциясы да) реакциясы жүреді.
1- кесте.
Көміртек–көміртекті байланыстың сипаттамасы:
| Байланыс | Энергия, кДж моль | Байланыс ұзындығы, нм |
| C–C | 0,154 | |
| C=C | 0,133 |
Алкендер қалыпты жағдайда катализатор қатысында сутекті қосып алып қаныққан көмірсутектерге ауысады:
CH2=CH–CH3+H2―›CH3–CH2–CH3;
пропен пропан
CH2=CH2+Cl2―›Cl–CH2–CH2–Cl
бутен–2 l,2–дихлорэтан
π-байланыстың реакцияға жоғары бейімділігінен алкендер гидрогалогендеу және гидратациялану реакциясына оңай түседі:
CH2=CH2+HCl―›CH3–CH2–Cl
этен хлорэтан
CH2=CH–CH3+HBr―›CH3–CH–CH3
пропен 2–бромпропан
CH2=CH2+HOH―›CH3–CH2–OH
этен этанол
Мұнда Марковников ережесіне сәйкес – сутек атомы қос байланыстағы неғұрлым сутектендірілген (қос байланыстағы көп сутек атомдарына) көміртек атомына қосылады.
Алкендер оңай тотығады, мұнда түзілген өнімдер мен олардың құрылысы процесті жүргізу жағдайына байланысты болады:
Жану: Толық емес каталитикалық тотығу:
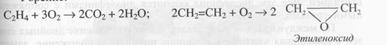
Калий перманганатымен бейтарап немесе сілтілік ортада тотықтырғанда екі атомды спирттер–гликольдар (Вагнер реакциясы) түзіледі:

 3CH2=CH2+2KMnO4+4H2O―›3CH2–CH2+2KOH+2MnO2
3CH2=CH2+2KMnO4+4H2O―›3CH2–CH2+2KOH+2MnO2
Этилен
OH OH
Этиленгликоль
Калий перманганатымен қышқылдық ортада (карбон қышқылдары түзіледі) тотықтырғанда қос байланыстың тотыға ыдырауы болады:
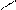
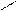 O
O
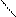 CH3–CH=CH–CH3+4(O) ―›2CH3 –C
CH3–CH=CH–CH3+4(O) ―›2CH3 –C
OH
Бутен -2 (KMnO4-нан) сірке қышқылы
Алкендер полимерленеді, полимерлену процесі әртүрлі жоғары молекулалы қосылыстар түзе жүреді:
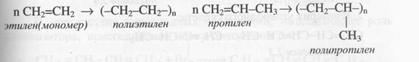
Алкадиендер (диендер) – молекуласында екі қосбайланыс болатын қанықпаған алифатты көмірсутектер. Алкадиендердің жалпы формуласы СnН2n-2. Қос байланыстардың орналасуы бойынша алкадиендерді оқшауланған, кумирленген және орайлас (сопряженные) деп бөледі:
| Оқшауланған | Кумулирленген | Орайлас |
| СН2=СН-СН2-СН=СН2 | СН2=С=СН2(аллен) | СН2=СН-СН=СН2 |
Бу фазасы крекингісі мен пиролиз өнімдерінің құрамында 5-тен 15%-ке дейін диолефиндер болуы мүмкін. Бұлар – бутадиен, пиперилен, циклопентадиен. Осы диолефиндердің барлығы орайлас байланысты диолефиндер болып табылады.
Халықаралық аталым бойынша алкадиендердегі қос байланыстың орналасуын атауының соңында, ал орынбасарлардың орнын атауының басында көрсетеді:
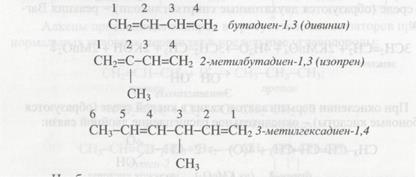
Алкадиендердің ішінде маңызды орын алатыны орайлас қос байланысты дидердер. Олар полимерленуге және бағалы полимерлі материалдар түзуге қабілетті. Орайлас диендерге изомерленудің мынадай түрлері тән:
1. Орайлас қос байланыстың орналасу изомериясы:
СН2=СН-СН=СН-СН2-СН3 СН3-СН2=СН-СН=СН-СН3
гексадиен-1,3 гексадиен-2,4
2. Көміртек қаңқасының изомериясы:
 СН2=СН-СН=СН-СН3 СН2=С-СН=СН2
СН2=СН-СН=СН-СН3 СН2=С-СН=СН2
пентадиен-1,3 сн3
2-метилбутадиен-1,3 (изопрен)
3. Алкиндер және циклоалкендер (С4Н6) арасындағы изомерия:
сн = сн

 СН2=СН-СН=СН2 СН=С-СН2-СН3
СН2=СН-СН=СН2 СН=С-СН2-СН3
СН2-СН2
бутадиен-1,3 бутин-1 циклобутен
Диендердің кеңістік изомерлері