Гальваникалық элемент (ГЭ)үшін дұрыс жағдай
B)Анодта –ГЭ теріс зарядталған электрод
D)Анод-ГЭ теріс полюсі
Гальваникалық элементтің электр қозғауышы күші (ЭҚК) жоғарырақ болатын электрод жұбы  :
:
Mg – Cu; 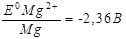
Al – Cu; 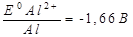
Mn – Cu; 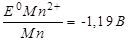
Донорлы-акцепторлы байланыс нәтижесінде түзілетін молекула:


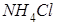
Диссоциациясы бірнеше сатыда жүретін электролиттер:
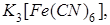
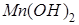 ,
, 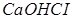
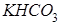 ,
, 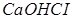 ,
, 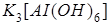
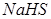 ,
, 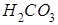 ,
, 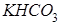
Диссоциациясы бір сатыда жүреді:
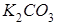 ,
, 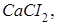
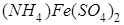
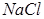 ,
,  ,
, 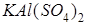
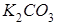 ,
, 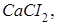
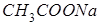
Диссоциациялану константасы К= 5·10‾8 тең 0,1 М НСlО ерітіндісіндегі сутек иондарының концентрациясы:
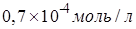
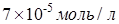
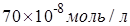
Дұрыс тұжырым:
В)Кд мәні тек әлсіз электролит үшін қажет
F)а мәні кез-келген электролит үшін қажет
G)а>30% күшті электролит
Диспропорциялану типіне жататын ТТР:
A)Cl2+KoH=KCL+KCLO+H2O
G)4KCLO3=KCL+3KCLO4
Ерігіштік көбейтіндісінің мәні бар зат:
барий сульфаты
күміс хлориді
кальций карбонаты
Ерігіштік көбейтіндісі (ЕК) 1,1×10‾10тең барий сульфатының (г/л) ерігіштігі:
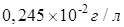
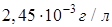
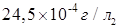
Еріген заттың дисперстік бөлшегі бойынша ерітінділерді ажыратады:
шынайы
коллоидты
өрескел дисперсті
Егер диссоциациялану дәрежесі 1,3% болса, 0,1 М сірке қышқылы
ерітіндісіндегі сутек иондары концентрациясы:
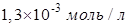
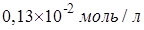
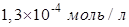
Ерітінді ортасы қышқылдық, егер рН мәндері:
2, 4, 3.
1, 2, 5.
5, 6, 2.
Ерітіндісі бейтарап орта көрсететін тұздар:
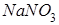
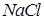
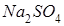
Ерітінді ортасы сілтілік тұздар:
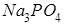
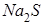
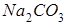
Жүзеге аспайтын реакциялар
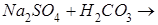


Жүйе күйінің термодинамикалық функциялары:
энтропия, энтальпия
энтропия, гиббс энергиясы
энтальпия, гельмгольц энергиясы
Жүйенің бастапқы және соңғы күйімен анықталатын термодинамикалық функциялар:
энтальпия, гельмгольц энергиясы
энтропия, гиббс энергиясы
энтропия, энтальпия
Жүйе ретсіздігінің кемуі байқалатын реакциялар:
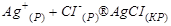
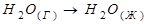
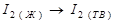
Жоғары температурада өз бетінше жүретін реакция:
энтропия артуымен, эндотермиялық
жүйенің көлемінің артуымен және энергия жұтылуымен
энтальпия және энтропия факторларының артуымен
Жүйенің ретсіздігінің мәні артатын реакция:
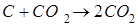
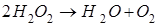
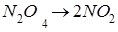
Жүйенің ретсіздігінің мәні төмендейтін реакция:
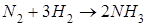
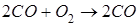

Жылдамдығы фаза аралық беттік ауданындағы заттың концентрацияларының өзгеруімен анықталатын реакциялар:

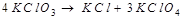
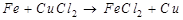 Жүйеэнтропиясының кемүі байқалатын реакциялар
Жүйеэнтропиясының кемүі байқалатын реакциялар
I_2©----I_2 (k)
Жүйеде қысымның жоғарылауы тепе-теңдіктің тура бағытта ығысуына әкелетін реакция:
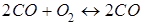
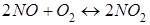
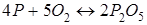
Заттардағы донорлы-акцепторлы байланыс түзілу шарттары:
бос атом орбитальдары бар элемент атомдары
акцептор ролін атқаратын атом (атомдар тобы)
донор ролін атқаратын атом (атомдар тобы)
Заттың еру шегінің дәрежесі бойынша ерітінділерді ажыратады:
қанықпаған
қаныққан
аса қаныққан
