Кислотно-основные реакции в воде
Вода – слабый электролит, поэтому за константу химического равновесия можно принять концентрационную константу, выраженную через равновесные концентрации участников реакции:
К = 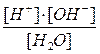
При постоянной температуре постоянна и константа химического равновесия. Концентрация чистой воды также постоянна и равна 55,55 моль/дм3. Перенесем постоянные величины в одну сторону:
К [H2O] = [H+] [OH-]
K [H2O] = const K[H2O] =Kw
Kw = [H+] [OH-]
Величина Kw называется ионным произведением воды. Из уравнения диссоциации воды видно, что [H+] =[OH-] Степень диссоциации воды весьма мала. При 22 0С в 1дм3 воды распадается на ионы лишь 10-7моля воды (установлено физическими методами следовательно [H+]=[OH-] = 10-7 моль/л.) Тогда Kw = [H+] [OH-] =10-14
Смысл этого уравнения заключается в следующем: как бы ни менялись концентрации ионов Н+ или ОН-, их произведение во всяком водном растворе сохраняет приблизительно постоянное значение, равное 10-14 при 22 0С.
Всякий водный раствор, независимо от того, какова его реакция, должен содержать как ионы Н+, так и ионы ОН-. Поскольку концентрации их связаны обратно пропорциональной зависимостью, реакцию любого раствора можно охарактеризовать количественно, указав в нем концентрацию ионов Н+:
кислая среда [H+]>[OH-]>10-7 моль/л
нейтральная среда [H+] = [OH-] = 10-7 моль/л
щелочная среда [H+]<[OH-]< 107 моль/л
Так как числовые значения Kw , а также [H+] и [OH-] очень маленькие, то вместо них принято использовать десятичный логарифм этих величин с противоположным знаком, при этом –lg[H+] обозначается рН и называется водородным показателем; –lg[ОH-] –рОН – гидроксильным показателем.
В кислой среде рН<7
В нейтральной среде рН =7
В щелочной среде рН>7
Если уравнение [H+][OH-]=10-14 прологарифмировать, а затем перенять у логарифмов знаки на обратные, то получим
рН+рОН=14
Расчет рН растворов кислот и оснований.
Растворы сильных кислот
Как известно, сильные кислоты практически полностью диссоциируют в растворах, например:
HCl=H+ +Cl-
рH=-lg[H+]
[H+]=α · n ·Cк-ты,
где α – степень диссоциации кислоты, n – число ионов Н+, получающихся в результате диссоциации, С – концентрация кислоты, моль/л α ≈1; n=1, тогда [H+] ≈ Cк-ты, а рН=-lgCк-ты.
Растворы сильных оснований, например NaOH.
Рассуждая аналогично, получаем
NaOH=Na+ +OH-
[OH-]= α · n · Cосн
n=1, α ≈1, [OH-] ≈ Cосн
-lg[OH-] =-lgCосн
[H+] = 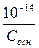 → рН =14+lgCосн
→ рН =14+lgCосн
Растворы слабых кислот
Выведем формулу для вычисления рН растворов слабых кислот на примере уксусной кислоты
CH3COOH D CH3COO- + H+
Kк-ты= 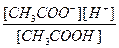
Если раствор кислоты не слишком разбавлен, то почти вся она присутствует в виде недиссоциированных молекул, следовательно [CH3COOH] ≈ const. Из уравнения диссоциации кислоты видно, что [H+] = [CH3COO-], тогда
Кк-ты= 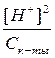
[H+]2 = Kк-ты · Ск-ты,
[H+] = 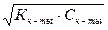
pH = 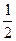 pKк-ты -
pKк-ты - 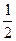 lgCк-ты,
lgCк-ты,
где рК = -lgK
