Стандартные абсолютные энтропии Sо298 некоторых веществ
| Вещество | Состояние | Sо298, Дж/(моль×К) | Вещество | Состояние | Sо298, Дж/(моль×К) |
| С | Алмаз | 2,44 | H2O | г | 188,72 |
| С | Графит | 5,69 | N2 | г | 191,49 |
| Fe | к | 27,2 | NH3 | г | 162,50 |
| Ti | к | 30,7 | CO | г | 197,91 |
| S | Ромб. | 31,9 | C2H2 | г | 200,82 |
| TiO2 | к | 50,3 | O2 | г | 205,03 |
| FeO | к | 54,0 | H2S | г | 205,64 |
| H2O | ж | 69,94 | NO | г | 210,20 |
| Fe2O3 | к | 89,96 | CO2 | г | 213,65 |
| NY4Cl | к | 94,5 | C2H4 | г | 219,45 |
| CH3OH | ж | 126,8 | Cl2 | г | 222,95 |
| H2 | г | 130,59 | NO2 | г | 240,46 |
| Fe3O4 | к | 146,4 | PCl3 | г | 311,66 |
| CH4 | г | 186,19 | PCl5 | г | 352,71 |
| HCl | г | 186,68 |
Пример 3. На основании стандартных теплот образования (табл. 5) и абсолютных стандартных энтропий веществ (табл. 7) вычислите DGо298 реакции, протекающей по уравнению:
СО(г) + Н2О(ж) = СО2(г) + Н2(г)
Решение. DGo = DHo – TDSo; DH и DS – функции состояния, поэтому:
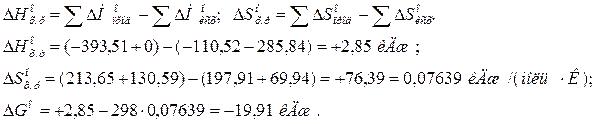
Пример 4. Реакция восстановления Fe2O3 водородом протекает по уравнению:
Fe2O3(к) + 3Н2(г) = 2Fe(к) + 3Н2О(г); DН = +96,61 кДж.
Возможна ли эта реакция при стандартных условиях, если изменение энтропии DS = 0,1387 кДж/(моль×К)? При какой температуре начнется восстановление Fe2O3?
Решение. Вычисляем DGo реакции:
DG = DH – TDS = 96,61 – 298 × 0,1387 = +55,28 кДж.
Так как DG > 0, то реакция при стандартных условиях невозможна; наоборот, при этих условиях идет обратная реакция окисления железа (коррозия). Найдем температуру, при которой DG = 0:
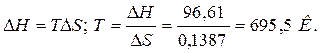
Следовательно, при температуре » 696,5 К начнется реакции восстановления Fe2O3. Иногда эту температуру называют температурой начала реакции.
Пример 5. Вычислите DНo, DSo и DGoT реакции, протекающей по уравнению:
Fe2O3(к) + 3С = 2Fe + 3СО
Возможна ли реакция восстановления Fe2O3 углеродом при температурах 500 и 1000 К?
Решение. DНoх.р и DSoх.р находим из соотношений (1) и (2) так же, как в примере 3:
DНoх.р = [3(-110,52)+2×0] – [-822,10+3×0] = -331,56+882,10 = 490,54 кДж;
DSoх.р = (2×27,2 + 3×197,91) – (89,96 + 3×5,69) = 541,1 Дж/К.
Энергию Гиббса при соответствующих температурах находим из соотношения DGoT = DНo – ТDS:
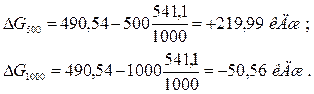
Так как DG500 > 0, а DG1000 < 0, то восстановление Fe2О3 углеродом возможно при 1000 К и невозможно при 500 К.
Контрольные вопросы
101. Вычислите DGо298 для следующих реакций:
а) 2NaF(к) + Cl2(г) = 2NaCl(к) + F2(г)
б) PbO2(к) + 2Zn(к) = Pb(к) + 2ZnO(к)
Можно ли получить фтор по реакции (а) и восстановить PbO2 цинком по реакции (б)? Ответ: +313,94 кДж; -417,4 кДж.
102. При какой температуре наступит равновесие системы:
4НСl(г) + О2 (г) 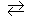 2Н2О(г) + 2С12(г); DH = -114,42 кДж?
2Н2О(г) + 2С12(г); DH = -114,42 кДж?
Хлор или кислород в этой системе является более сильным окислителем и при каких температурах? Ответ: 891 К.
103. Восстановление Fe3O4 оксидом углерода идет по уравнению:
Fe3О4(к) + СО(г) = 3FeO(к) + СО2(г)
Вычислите DGо298 и сделайте вывод о возможности самопроизвольного протекания этой реакции при стандартных условиях. Чему равно DSо298 в этом процессе? Ответ: +24,19 кДж; +31,34 Дж/ (моль • К).
104. Реакция горения ацетилена идет по уравнению:
С2Н2(г)+ 5/202(г) = 2С02(г) + Н2О(ж)
Вычислите DGо298 и DSо298. Объясните уменьшение энтропии в результате этой реакции. Ответ: -1235,15 кДж; -216,15 Дж/ (моль • К).
105. Уменьшается или увеличивается энтропия при переходах: а) воды в пар; б) графита в алмаз? Почему? вычислите DSо298 для каждого превращения. Сделайте вывод о количественном изменении энтропии при фазовых и аллотропических превращениях.
Ответ: а)118,78 Дж/ (моль • К); б) -3,25 Дж/ (моль • К).
106. Чем можно объяснить, что при стандартных условиях невозможна экзотермическая реакция:
Н2(г) + СО2(г) = СО(г) + Н2О(ж); DН = -2,85 кДж?
Зная тепловой эффект реакции и абсолютные стандартные энтропии соответствующих веществ, определите DGо298 этой реакции. Ответ: +19,91 кДж.
107. Прямая или обратная реакция будет протекать при стандартных условиях в системе:
2NO(г) + O2 (г) 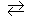 2NO2(г)
2NO2(г)
Ответ мотивируйте, вычислив DGо298 прямой реакции. Ответ: -69,70 кДж.
108. Исходя из значений стандартных теплот образования и абсолютных стандартных энтропии соответствующих веществ, вычислите DGо298 реакции, протекающей по уравнению:
NH3(г) + HCl(г) = NH4Cl(к)
Может ли эта реакция при стандартных условиях идти самопроизвольно? Ответ: -92,08 кДж.
109. При какой температуре наступит равновесие системы:
СО(г) + 2Н2(г) 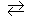 СН3ОН(ж); DH = -128,05 кДж?
СН3ОН(ж); DH = -128,05 кДж?
Ответ: »385,5 К.
110. При какой температуре наступит равновесие системы:
СН4(г) + СО2(г) = 2СО(г) + 2Н2(г); DН = +247,37 кДж?
Ответ: »961,9 К.
111. На основании стандартных теплот образования и абсолютных стандартных энтропии соответствующих веществ вычислите DGо298 реакции, протекающей по уравнению:
4NН3(г) + 5О2(г) = 4NО(г) + 6Н2О(г)
Возможна ли эта реакция при стандартных условиях? Ответ: -957,77 кДж.
112. На основании стандартных теплот образования и абсолютных стандартных энтропии соответствующих веществ вычислите DGо298 реакции, протекающей по уравнению:
СО2(г) + 4Н2(г) = СН4(г) + 2Н2О(ж)
Возможна ли эта реакция при стандартных условиях? Ответ: -130,89 кДж.
113. Вычислите DНo, DSoи DGoT реакции, протекающей по уравнению:
Fe2O3(к) + ЗН2(г) = 2Fe(к) + 3Н2О(г)
Возможна ли реакция восстановления Fе2О3 водородом при температурах 500 и 2000 К? Ответ: +96,61 кДж; 138,83 Дж/К; 27,2 кДж; -181,05 кДж.
114.Какие из карбонатов: ВеСО3 или BaCO3 – можно получить по реакции взаимодействия соответствующих оксидов с СО2? Какая реакция идет наиболее энергично? Вывод сделайте, вычислив DGо298 реакций. Ответ: +31,24 кДж; -130,17 кДж;
-216,02 кДж.
115.На основании стандартных теплот образования и абсолютных стандартных энтропии соответствующих веществ вычислите DGо298 реакции, протекающей по уравнению:
СО(г) + 3Н2(г) = СН4(г) + Н2О(г)
Возможна ли эта реакция при стандартных условиях? Ответ: -142,16 кДж.
116. Вычислите DНo, DSoи DGoT реакции, протекающей по уравнению:
ТiO2(к) + 2С(к) = Ti(к) + 2СO(г)
Возможна ли реакция восстановления TiO2 углеродом при температурах 1000 и 3000 К? Ответ: +722,86 кДж; 364,84 Дж/К; +358,02 кДж; -371,66 кДж.
117. На основании стандартных теплот образования и абсолютных стандартных энтропий соответствующих «веществ вычислите DGо298 реакции, протекающей по уравнению:
С2Н4(г) + 3О2(г) = 2СО2(г) + 2Н2О(ж)
Возможна ли эта реакция при стандартных условиях? Ответ: -1331,21 кДж,
118. Определите, при какой температуре начнется реакция восстановления Fе3О4, протекающая по уравнению:
Fe3O4(к) + СО(г) = 3FeO(к) + СО2(г); DН = +34,55 кДж.
Ответ: 1102,4 К.
119. Вычислите, при какой температуре начнется диссоциация пентахлорида фосфора, протекающая по уравнению:
РС15(г) = РС13(г) + Сl2(г); DН = +92,59 кДж.
Ответ: 509 К.
120. Вычислите изменение энтропии для реакций, протекающих по уравнениям:
2СН4(г) = С2Н2(г) + 3Н2(г)
N2(г) + 3H2(г) = 2NH3(г)
С (графит) + О2(г) = СО2(г)
Почему в этих реакциях DSо298 > 0; <0; @ 0?
Ответ: 220,21 Дж/К; -198,26 Дж/К; 2,93 Дж/К.
