Фильтрование при обычном давлении 4 страница
Очень удобны специальные насадки с перегородкой из вплавленной фильтрующей пластинки из пористого стекла (рис. 413). Они устойчивы к влажным и корродирующим газам, однако их можно применять только в, том случае, если газовая струя идет с давлением, не превышающим 1 кг/см2.
Для промывки газов и очистки их от твердых частиц очень хорошо применять стеклянный газопромыватель.] (рис. 414). Его заполняют водой или серной кислотой.'!
Кроме того, для промывания газов применяют описанные выше склянки Дрекселя, Тищенко и Вульфа.д
* Очистка газов от пыли путем использования электрических полей в так называемых аппаратах Коттреля здесь не описывается; об этом см. У ж о в Н. В., Очистка промышленных газов электрофильтрами, Госхимиздат, 1962.
Для этих же целей можно использовать колбу Бунзена. В ее горло вставляют резиновую пробку, снабженную стеклянной трубкой. Эта трубка должна доходить почти до дна колбы и выступать наружу примерно на 5 см.
Для разделения смеси газов ее пропускают через растворы, поглощающие те или иные газы. Так, для отделения кислорода применяют влажный фосфор, пирогаллол (пользующийся наибольшим распространением),
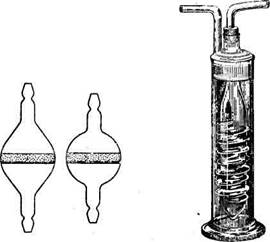
Рис. 413. Насадка для фильт- Рис. 414. Стеклянный
рования газов с пластинкой газопромыватель,
из пористого стекла.
гидросульфит натрия, аммиачный раствор закиси меди и др.
Для получения поглотительного раствора пирогаллола отдельно приготовляют 25%-ный раствор пирогаллола и 60%-ный раствор едкого кали; затем берут на 1 объем раствора пирогаллола 5 объемов раствора едкого кали и смешивают, избегая окисления смеси кислородом воздуха. Лучше всего смешивание проводить в том сосуде, в котором будет происходить поглощение кислорода (пипетки для поглощения, склянки Дрекселя и пр.); 1 мл такого раствора поглощает 13 мл кислорода.
Хорошим поглотителем является также раствор пирогаллола, рекомендуемый Гофманом. Растворяют 40 г
31-117
пирогаллола в 90 мл воды и этот раствор смешивают с 70 г (45 мл) концентрированного раствора едкого кали (df — 1,55) при соблюдении указанных выше условий. При изготовлении поглотительных растворов пирогаллола нужно брать именно едкое кали, а не едкий натр, так как с последним поглощение идет хуже и медленнее. Обычно бывает достаточно одного прибора с раствором пирогаллола; нужно следить, чтобы газ пропускался не очень сильной струей. Для большей уверенности в том, что кислород поглощается полностью, иногда берут два поглотительных прибора и соединяют их последовательно. Для поглощения кислорода вместо обычного пирогаллола применяют так называемый пирогаллол А. Он представляет собой триацетат оксигидрохинона (1,2,4-триок-сибензол); поглотительная способность пирогаллола А такая же, как и у пирогаллола.
Преимущество пирогаллола А перед обычным пирогаллолом состоит в том, что при поглощении им кислорода не выделяется окись углерода.
Вместо раствора пирогаллола можно пользоваться раствором СгС12. Для получения раствора СгС12 сначала растворяют 40 г Сг(ОН)3 в 100 мл 2 н. раствора НС1 или же 193 г хромовых квасцов в 1 л воды и осаждают гидроокись хрома концентрированным раствором NH4OH. Осадок Сг(ОН)3 промывают водой до отрицательной реакции на ионы SOf~; 40 г гидроокиси хрома растворяют в 200 «2 н. раствора НС1. В раствопе образуется СгС13, который восстанавливают до СгС12 амальгамой цинка. Для изготовления последней к 100 г металлической ртути прибавляют 5 г гранулированного цинка, несколько миллилитров 2 н. раствора НС1 и при помешивании нагревают на водяной бане до полного растворения цинка. Охлажденную амальгаму промывают водой с применением декантации, добавляют солянокислый раствор СгС13 и взбалтывают до изменения зеленой окраски в голубую. Полученным раствором СгС12 заполняют поглотительную пипетку газоанализатора, предназначенную для поглощения кислорода; 1 мл 20%-ного раствора GC12 поглощает 9 мл кислорода.
Отработанный раствор регенерируют взбалтыванием его с амальгамой цинка, как описано выше. Поглощение кислорода протекает по уравнению:
4СгС12 + 02 + 4НС1------ > 4СгС13 + 2Н20
Для поглощения азота можно применять металлический кальций при красном калении, когда он жадно поглощает азот, или же смесь, состоящую из 1 части магниевого порошка и 5 частей СаО (свежеобоженного) в виде зерен размером макового зерна. Перед употреблением следует добавить 0,25 части тонко нарезанного металлического натрия. Поглощение азота проводят при светло-красном калении этой смеси.
В качестве поглотителя кислорода при газовом анализе используют также кальциевую соль гидрохинон. С кислородом она очень активно реагирует как в твердом, слегка увлажненном состоянии, так и в водных растворах.
Для этой же цели применяют щелочной раствор тан-нина*. Для приготовления этого раствора 24 г таннина (галлотаннин или скумпиевый таннин) растворяют в 150 мл 17,5—18%-ного раствора КОН.
А. С. Садыков и А. Исмаилов (АН КазССР) предложили заменять пирогаллол госсиполом, получаемым из коры корней хлопчатника. По эффекту поглощения кислорода госсипол аналогичен пирогаллолу и поэтому с успехом может заменять последний.
Для связывания кислорода, растворенного в воде, иногда применяют сульфит натрия. Для этих же целей хорошие результаты дает применение гидразина.
Для очистки инертных и восстановительных газов от следов кислорода рекомендуется использовать промывал-ку, заполненную амальгамой алюминия. Применение амальгамы позволяет снизить содержание кислорода в пробе до ничтожно малого. Для этой цели используют также амальгамы магния и кальция. Для облегчения соприкосновения газа с амальгамой промывалку непрерывно встряхивают или используют магнитную мешалку.
Для отделения СО газовую смесь обычно пропускают через раствор СиС12, приготовляемый растворением 1 г Си2С12 в 20%-ной НС1.
Окись углерода поглощают раствором СиС12. Для этого взбалтывают 200 г СиС12 с раствором 250 г NH4C1 в 750 мл воды в закупоренной склянке, в которую потом вставляют доходящую до шейки медную спираль. Перед наполнением поглотительного сосуда 3 объема этого рас-
| 31* |
* Т у р г е л ь Е. О., Труды ВНИИ нефтехимических процессов, вып. 5, 1962, стр. 80; РЖХим, 1963, реф. 1Г76.
твора смешивают с 1 объемом водного раствора аммиака (df> = 0,903). 1 мл этого раствора поглощает 16 мл СО.
Раствор следует часто менять, так как он может отдавать СО более бедному этим соединением газу. Он поглощает также кислород и применим лишь после предварительного удаления кислорода из газовой смеси.
Для поглощения СО из газовых смесей рекомендованы также аммиачные растворы однохлористой меди примерно следующего состава: Си2С12 — 11 —12 частей, NH3 — 13—14 частей, вода — 74—76 частей, т. е. навеску Си2С12 растворяют приблизительно в 90 мл раствора NH3 (df = 0,940); 1 мл этого раствора поглощает 31 мл СО.
Для стабилизации раствора рекомендуется добавлять NH4C1 в количестве 10% по массе от количества Си2С12-
Аммиачные растворы Си2С12 выделяют NH3. Поэтому после прибора ставят газопромыватель с 86%-ной серной кислотой для поглощения аммиака. Следует отметить, что растворы однохлористой меди не полностью поглощают СО, и поэтому для абсорбции остатков СО газовую смесь необходимо пропускать через газовую пипетку с Р-нафтолом.
РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА
О различных случаях применения стеклянных фильтров см. Красиков Е. С, Стеклянные фильтры в лабораторной практике, Зав. лаб., 7, № 8—9, 1045 (1938).
О пористых фильтрах из полиэтилена см. К п i z a k M., Chem. listy, 54, № 4, 383 (1960); РЖХим, 1961, № 9, 157, реф. 9Е57.
О простом фильтре для вакуум-фильтрации полумикрометодом см. Mitchell M. J., Chemist Analyst, 49, № 1, 30 (1960); РЖХим, 1961, № 9, 157, реф. 9Е54.
О приспособлении для ускорения фильтрования в лаборатории см. Feinstein H. J., Chem. Educ, 35, № 10, 509 (1958); РЖХим, 1960, № 5, 12, реф. 16435.
О стеклянных пористых фильтрах см. Czyzewski M., Pomiary, automat., kontrol., 7, № 11, 476 (1961); РЖХим, 1962, реф. 22Е61.
Автоматический прибор для фильтрования в инертной атмосфере см. Lebl M., Chem. listy, 56, № 7, 813 (1962); РЖХим, 1963, реф. 4Д58.
О поршневом стеклянном фильтре для низкотемпературного фильтрования см. Ferguson 1. М., Chem. a. Ind., 1348, № 34, 1961; РЖХим, 1962, реф. 8Е44.
О приборе для фичьтрования при постоянной температуре см. Furst H., Chem. Techn., 5, № 2, 78 (1953).
Об автоматизации процесса фильтрования см. Конев Ф. А., Колесников Н. А., К о л е с н и к о в Д. Г., Зав. лаб.,,
24 № 3, 375 (1958); Lebl M., Chem. listy, 53, № 12; 1280 (I95D); РЖХим, 1961, № 1, 160 (60), реф. 1Е85.
Прибор для быстрого фильтрования описан в Lab. Sci., 12, Ко 3, 92 (1964); РЖХим, 1965, 19Д37.
Лабораторный дисковый вакуум-фильтр описал Т а р у-т „ и В. П., Хим. и нефт. машиностр., № 12, 3 (1965); РЖХим, 196S, ЮД96.
О воронке для ускоренного отделения осадков см. Ч у х л а н-u е в В. Г., Зав. лаб., 30, № 1, 113 (1964); РЖХим, 1966, 12Д60.
Новый прибор для фильтрования — фильтрующая центрифужная обойма — описан Stoerbach A., Kem. Tisl., 22, 10, 745 (1965); РЖХим, 1966, 13Д104.
О применении фильтров из стекловолокна в анализе воды см. GieblerG., Kempt Т., Z. anal. Chem., 199, № 1, 23(1964); РЖХим, 1964, 14Г53.
Прибор для фильтрования под давлением описал М а е i о-I е k J. A., Limnolog. a. Oceanogr., 8, № 2, 301 (1963); РЖХим, 1964, 15Д76.
Об ускорении фильтрования в химическом анализе см. Wolf С, S с h г е i t е г е г R., Z. angew. Geol., 9, № 12, 662 (1963); РЖХим, 1964, 16Г4.
Прибор для фильтрования пульпы при отборе проб щелоков описал Jackson R. J., Lab. Pract., 13, № 5, 422 (1964); РЖХим, 1964, 24Д87.
Об удобной микронасадке для фильтрования см. Cooper P. D., Chem. Educ, 41, № 2, 85 (1964); РЖХим, 1965, 1Д71.
Прибор для фильтрования под давлением описал К о н о в а-л о в Г. С, Зав. лаб., 30, № 9, 1149 (1964); РЖХим, 1965, 4Д62.
О фильтрующей способности различных сортов бумаги см. Н о и п m a n R. F., Ann. Occupat. Hyd., 4, № 3—4, 301 (1962); РЖХим, 1962, реф. 20Е28.
О фильтровальной бумаге и других фильтрующих средах, используемых в лаборатории, см. Brinkman A. М., Chemie en techniek, 18, № 4, 141 (1963); РЖХим, 1Д24.
Об аналитических фильтровальных бумагах см. Griine A., Oster. Chem. Ztg., 64, J^b 7, 206 (1963); РЖХим, 1964, 5Г73.
О фильтрующих порошках см. Kemikalietacket, 23, № 3, 63, 84 (1964); РЖХим, 1965, 2Д82.
Об экспериментальном и теоретическом исследовании фильтрационного эффекта и о различной скорости фильтрования катионов и анионов см. Жариков В. А., Дюжикова Т. Н., Изв. АН СССР, Сер. геол., № 1, 41 (1962); РЖХим, 1962, реф. 13Г43.
О новых методах фильтрования см. Canal F., Lab. Sci., 3, № 6, 161 (1955); РЖХим, 1956, № 16, 306, реф. 51366.
Об ускорении фильтрования растворов, содержащих двуокись кремния, см. П р о с к у р н я к о в Г. Ф., Зав. лаб., 16, № 3, 864 (1950).
О фильтровании труднофильтрующихся осадков см. Р i с t s с h R., Mikrochim. Acta, № 4, 859 (1955); РЖХим, 1956, Л° 6, 282, реф. 16539.
О фильтровании насыщенных горячих растворов под давлением в органической полумикро- н микротехнике см. РЖХим, 1964,
48«
О простом приборе для ультрафильтрации см. Burns D. А., BudnaJ. N., Chamberlin J.M., Sci., 138, № 3537 (1962); РЖХим, 1963, реф. ПД39.
О простом приборе для диализа и ультрафильтрации малых объемов см. К о ё s J., Chem. listy, 55, № 10, 1229 (1961); РЖХим, 1962, реф. 6Е92.
Об ультрафильтрации см. ЯндерГ., Заковский И., Мембранные, целла- и ультратонкие фильтры, Хнмтеоретиздат, 1937; Б е р л ь-Л у н г е, Химико-технические методы исследова- ( ния, т. 1, вып. 2, Хнмтеоретиздат, 1937, стр. 582.
Батарейная установка для ультрафильтрования золей описана 1 в Укр. хим. ж., 20, вып. 1, 31 (1954).
Об ультрафильтровании через мембрану из целлофана см. \ L a u s e n H. H., Acta Pharmacol, et toxicol., 11, № 4, 353 (1955); РЖХим, 1958, № 5, 118, реф. 14282.
О применении ионитовых мембран и лабораторном способе их • изготовления см. Мелешко В. П., Червинская О. В.,1 Романов М. Н., И з м а й л о в Д. Г., Сборник трудов Bo-j ронежского отд. ВХО им. Д. И. Менделеева, вып. 2, 1959, 169Д РЖХим, 1963, реф. 9Д73.
Об изготовлении мембран см. С а г п е 1 1 Р. Н., С a s s i-dy H. S., J. Polymer Sci., 55, № 161, 233 (1960); РЖХим, 1962,1 реф. 18Б478.
О новом применении мембранных фильтров см. S с h e n e г-m a n n E. A., Prakt. Chem. 14, № 6, 244, 247 (1963); РЖХнмД 1964, 6Д73.
О мембранных фильтрах и ультрафильтрах см. S с h е п е г-m а п п Е. A., Prakt. Chem. Lab. und Betried, 15, № 2, 51 (1964)jl РЖХим, 1964, 16Д41.
О лабораторных центрифугах и их применении см. О е г t а 1 С,' Chem. Techn., 14, № 8, 476 (1962); РЖХим, 1963, реф. 11Д40.
О специальной лабораторной центрифуге, дающей возможность проводить центрифугирование в колбе, см. Терещенко П. Н. 1 Антонов В. И., Зав. лаб., 24, № 9, 1153 (1958).
О высокотемпературной лабораторной центрифуге см. Ван ю-.: к о в А. В., У т к и н Н. И., Р е м о в В. А., Зав. лаб., 25,' № 2, 222 (1959).
Обзор об ультрацентрифугах см. D a g 1 е у S., J. Roy Inst. Chem., 84, 382 (1960); РЖХим, 1961, № 12, 171 (57), реф. 12Е67^
О поглотителях кислорода см. Халтурин А. И., Азер| б а е в И. И., Изв. АН КазССР, Сер. хим., вып. 2 (14), 98 (1959)3
О приспособлении для быстрого удаления кислорода из полет рографируемых растворов (продувание азотом) см. В а й н-J штейн Г. М., Зав. лаб., 27, № 4, 485 (1961).
Об установке для тонкой очистки инертных газов от кислорода и паров воды см. Грачев В. С, Кириллов П. Л., Атомй ная энергия, 6, № 3, 327 (1959).
Об очистке газов см. Блаженова А. Н., Ильинская А. А., Рапопорт Ф. М., Анализ газов в химической*! промышленности, под ред. М. М. Файнберга, Госхимиздат, 1954"*
О действии замораживания на свойства осадков гидратирован-ных сульфидов см. ВольхинВ. В., КубареваА. Г.З Изв. высш. уч. завед., Сер. химия и хим. техн., 7, № 5, 725 (1964)/ РЖХим, 1965, 10Г2.
Глава 12
дистилляция
ОБЩИЕ ПОНЯТИЯ
При нагревании жидкости повышается ее температура и давление насыщенного пара. Повышение температуры и давления происходит до тех пор, пока давление пара не станет равным внешнему (атмосферному) давлению. При этом температупа достигнет некоторого определенного значения (температуры кипения) и жидкость закипит.
Если взять ряд химически чистых жидкостей, например толуол, воду, спирт, эфир, то, кроме запаха, плотности и т. д., различие между ними может быть установлено также и по температуре кипения. Если нагревать все эти четыре жидкости в одинаковых условиях, то раньше всех закипает эфир, затем спирт, потом вода и, наконец, толуол. Каждая жидкость кипит при определенной температуре: эфир при 34,5 °С, спирт ппи 78 °С, вода при 100 СС, температура кипения толуола 111 °С.
Когда начинается кипение, повышение температуры жидкости прекращается*, несмотря на то что нагревание поодолжается.
Определение температуры кипения может служить для определения чистоты вещества.
На температуру кипения жидкости прежде всего влияет давление. Если давление изменяется, то изменяется и температура кипения. Поэтому, когда говорят о нормальной температуре кипения жидкости, имеют в виду ту температуру, при которой жидкость кипит, находясь под нормальным давлением (одна атмосфера, или 760 мм рт. ст.). При уменьшении внешнего давления уменьшается и температура кипения жидкости. Наоборот,
* Если жидкость не является смесью различных веществ, имеющих разные температуры кипения.
если давление увеличивается, температура кипения повышается.
Этим свойством — изменением температуры кипения при уменьшении давления — пользуются очень часто, в особенности в лаборатории.
Некоторые вещества при нагревании их до температуры кипения при нормальном давлении разлагаются, } Поэтому если такие вещества нужно перегнать (напри-} мер, для очистки), то применяют перегонку под уменьшен-! ным давлением, так называемую вакуум-перегонку. Как! уже упоминалось, при уменьшении давления жидкость! закипает при более низкой температуре и таким путем! удается перегнать жидкость без ее разложения. В хими-1 ческих справочниках всегда указывают, при какой тем-J пературе и при каком давлении жидкость кипит. Если,! например, в справочнике указано 118°/14, это значит, что! данная жидкость при давлении 14 мм рт. ст. кипит при» 118 °С.
Большое влияние на характер кипения жидкости ока-» зывает растворенный в ней воздух. Еще около 170 лет! тому назад физик де-Люк высказал предположение, чтц| кипение жидкости происходит потому, что пузырьки паря образуются вокруг мельчашийх пузырьков воздуха, pacfl творенного в жидкости. Если эти пузырьки удалить теш или иным путем, то воду можно нагреть до 130 °С при] обычном давлении и она не закипит. Но достаточно ввести! пузырек воздуха — и вода сразу вскипает. Это оченм хорошо заметно на дистиллированной воде. Нагреть ди-jg стиллированную воду до кипения много труднее, чем обык-| новенную. Но если ее перед нагреванием взболтать, та кипение происходит легче. Точно так же, если в воду, Щ{ которой удален воздух, при нагревании внести какое-] либо пористое твердое тело, например пемзу или кусочей неглазурованного фарфора, у поверхности их тотчас жа начинается образование пузырьков пара и кипение будет* происходить при соответствующей температуре. Это объяс-* няется тем, что на поверхности этих твердых тел находится слой воздуха.
Такие твердые тела, вводимые для облегчения кипения, называют «к и п е л к а м и». Их используют только, один раз, и для каждой перегонки следует брать свежие «кипелки». Лучшим способом предупреждения толчков прИ кипении является введение в горло перегонной колбы
слоя (выше уровня жидкости) стеклянной ваты. Иногда к перегоняемой жидкости добавляют такие соединения, которые при нагревании разрушаются, выделяя неактивный газ. Гримером таких соединений является двууглекислый натрий, при разложении которого вследствие нагревания выделяется двуокись углерода.
Естественно, что в качестве соединений, выделяющих неактивный газ, можно применять только такие вещества, продукты распада которых не действуют как-либо на перегоняемое вещество. Рекомендовано также применение кусочков материала, не смачиваемого перегоняемой жидкостью. Из таких материалов часто оказываются пригодными продукты полимеризации тетрафторэтилена. Они выдерживают нагревание до 200 °С.
Очень хорошо применять просто механическое перемешивание, которое легче и удобнее всего проводить при помощи магнитной мешалки.
При перегонке в вакууме наилучшим приемом предупреждения толчков является пропускание через жидкость инертного газа в виде мельчайших пузырьков.
Ксоме того, для предотвращения толчков, сопровождающих кипение, было предложено вносить в жидкость диски из спрессованного стеклянного волокна. Они не загрязняют раствор и, двигаясь быстро под действием конвекционных токов, предотвращают образование перегретых участков, около которых образуется внезапное вскипание, вызывающее толчки.
Для предотвращения перегрева и связанной с этим задержки кипения используют также принцип перегрева в малом объеме. На дно стакана помещают часовое стекло выпусклостью вверх, а в круглодонную колбу — также часовое стекло выпуклостью вниз или диск. Между дном сосуда и часовым стеклом или диском создается зазор, и кипение происходит в этом зазоре.
Если жидкость нагревать до кипения и отводить образующиеся пары по трубке, то при охлаждении их на стенках начнется образование капель жидкости. Этими свойствами жидкости — кипеть с образованием паров — и способностью их при охлаждении конденсироваться пользуются для очистки жидкостей, применяя процесс д и-стилляции, или перегонки.
Перегонка является одним из способов очистки с целью получения химически чистого вещества.
Различают три способа перегонки жидкости: под обыкновенным давлением, под уменьшенным давлением и в водяным паром.
