Химическая кинетика и равновесие
Химическая кинетика
Скорость химической реакции – это изменение количества вещества Dn вступающего в реакцию или образующегося в результате реакции в единицу времени в единице реакционного пространства.
Для гомогенной реакции, протекающей во всем объеме V системы, единицей реакционного пространства является единица объема. Тогда средняя скорость реакции по данному веществу за промежуток времени Dt выразиться формулой
vср.= 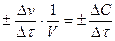 , (2.3.1)
, (2.3.1)
где DС – изменение молярной концентрации вещества за промежуток времени, моль/л.
Знак «+» используется, если за скоростью реакции следят по увеличению концентрации продуктов реакции, а знак «-» – если о скорости судят по убыли концентрации исходных веществ.
Только при линейной зависимости концентрации вещества от времени истинная скорость реакции (скорость в данный момент времени) постоянна и равна средней скорости. При нелинейной зависимости истинная скорость реакции изменяется со временем. Поэтому средняя скорость за некоторый промежуток времени является грубым приближением истинной.
Чтобы определить скорость реакции в данный момент времени t, необходимо взять бесконечно малый интервал времени dt, иными словами, истинная скорость реакции определяется первой производной количества вещества по времени:
v = 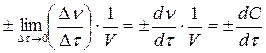 (2.3.2)
(2.3.2)
Для гетерогенной реакции, протекающей на границе раздела между веществами, единицей реакционного пространства является единица площади S поверхности раздела фаз. Выражения для средней и истинной скорости реакции по данному веществу имеют следующий вид:
vср.= 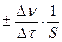 ; (2.3.3)
; (2.3.3)
v= 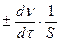 . (2.3.4)
. (2.3.4)
Скорость химической реакции зависит от многих факторов. Рассмотрим влияние некоторых из них.
Прежде всего, скорость химической реакции зависит от природы реагирующих веществ.
Зависимость скорости реакции от концентрации реагирующих веществ выражается законом действующих масс. Этот закон формулируется для простых реакций, то есть реакций, протекающих в одну стадию, или для отдельных элементарных стадий сложных химических реакций:  скорость реакции при заданной температуре пропорциональна произведению концентраций реагирующих веществ в степенях, равных соответствующим стехиометрическим коэффициентам в уравнении реакции.
скорость реакции при заданной температуре пропорциональна произведению концентраций реагирующих веществ в степенях, равных соответствующим стехиометрическим коэффициентам в уравнении реакции.
Для простой реакции вида
аА + вВ→продукты реакции
этот закон выражается уравнением
v = k(CA)a×(CB)b (2.3.5)
Это выражение называются кинетическими уравнениями. Коэффициент пропорциональности k называется константой скорости реакции, его величина зависит от природы веществ, температуры, присутствия катализатора, но не зависит от концентрации.
В большинстве случаев химическая реакция представляет собой сложный многостадийный процесс, и уравнение реакции отражает материальный баланс, а не действительный ход процесса. Поэтому закон действующих масс не может быть применен ко всему процессу в целом. Иногда зависимость скорости реакции от концентрации веществ вообще не может быть описана степенной функцией вида (2.3.5).
Для характеристики кинетики экспериментально изучаемых реакций вводят понятие порядка реакции. Порядок реакции по данному веществу (частный порядок) – это число, равное показателю степени, в которой концентрация этого вещества входит в кинетическое уравнение реакции. Частный порядок определяется экспериментально. Он может принимать целые, дробные, отрицательные значения, быть равным нулю. В общем случае частный порядок не равен соответствующему стехиометрическому коэффициенту в уравнении реакции, хотя иногда, по случайному совпадению, оказывается таким, каким его следовало бы ожидать на основании стехиометрии реакции.
В кинетике гетерогенных реакций существуют определенные особенности.
- В кинетические уравнения таких реакций не входят концентрации конденсированной фазы, поскольку реакция идет на поверхности раздела фаз, и концентрация конденсированной фазы остается постоянной.
- Гетерогенные реакции всегда представляют собой сложные процессы. Они включают не только стадии собственно химической реакции на поверхности, но и диффузионные стадии: подвод реагирующего вещества к поверхности, отвод от поверхности продуктов взаимодействия. Если скорость диффузии меньше скорости химической реакции, то именно диффузионные стадии будут определять скорость процесса. Скорость таких реакций возрастает при перемешивании.
- Удельная скорость собственно химического взаимодействия, отнесенная к единице поверхности, от площади поверхности не зависит. Однако если необходимо ускорить гетерогенный процесс в целом, прибегают к измельчению реагирующих веществ. Это приводит к увеличению поверхности контакта, уменьшению протяженности диффузионных путей.
Скорость большинства химических реакций возрастает при повышении температуры. Для реакций, протекающих со средними скоростями, в не очень больших интервалах температур выполняется приближенное эмпирическое правило Вант-Гоффа: при повышении температуры на 100 скорость реакции увеличивается в 2 – 4 раза.
Математически это можно записать так:
v2 = v1× 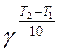 , (2.3.6)
, (2.3.6)
где v1 и v2 – скорости реакции при начальной Т1 и конечной Т2 температурах соответственно;
g – температурный коэффициент скорости реакции.
Температурный коэффициент скорости показывает во сколько раз увеличится скорость реакции при повышении температуры на 100.
Более точно влияние температуры на скорость химической реакции выражается уравнением Аррениуса для константы скорости простой реакции или элементарной стадии сложного процесса:
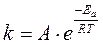 , (2.3.7)
, (2.3.7)
где А – предэкспоненциальный множитель;
R – газовая постоянная;
Т – абсолютная температура;
e – основание натурального логарифма;
Еа – энергия активации.
Уравнение Аррениуса применимо также ко многим (но не всем) сложным реакциям. В этих случаях энергию активации называют кажущейся.
В ходе реакции система проходит через переходное состояние (активированный комплекс). Активированный комплекс имеет более высокую энергию, чем исходные вещества и продукты реакции. Энергия активации представляет собой энергию, необходимую для образования активированного комплекса.
Одним из методов влияния на скорость реакции является катализ, который осуществляется при помощи катализаторов – веществ, изменяющих скорость химической реакции вследствие многократного участия в промежуточном химическом взаимодействии с реагентами, но после каждого цикла промежуточного взаимодействия восстанавливающих свой химический состав. Катализатор в конечные продукты реакции не входит. Как правило, вводится в небольших количествах по сравнению с исходными веществами.
Катализатор открывает новые пути процесса через переходные состояния с его участием, причем эти пути характеризуются меньшей энергией активации, чем некаталитическая реакция. Это приводит к увеличению скорости процесса.
Снижение энергии активации является определяющей, но не единственной причиной увеличения скорости реакции в присутствии катализатора. Катализатор может вызывать увеличение предэкспоненциального множителя в уравнении Аррениуса. По теории активированного комплекса предэкспоненциальный множитель зависит от энтропии образования переходного состояния, которая может увеличиваться в присутствии катализатора.
Катализатор не изменяет теплового эффекта реакции.
Различают положительный катализ, приводящий к ускорению реакции, и отрицательный, уменьшающий скорость реакции. В последнем случае, в силу избирательности (селективности), катализатор ускоряет ранее наиболее медленные стадии сложного процесса, тем самым исключая один из возможных без него путей процесса. В результате реакция замедляется или практически полностью подавляется.
Замедлять химические реакции могут также вещества, называемые ингибиторами, но механизм их действия несколько иной.
Различают гомогенный и гетерогенный катализ. При гомогенном катализе реагирующие вещества и катализатор образуют одну фазу, между ними отсутствует поверхность раздела. При гетерогенном катализе катализатор и реагирующие вещества находятся в разных фазах, реакция идет на поверхности катализатора.
Химическое равновесие
Химические реакции бывают обратимые и необратимые. Необратимые протекают только в одном направлении, в сторону образования продуктов реакции до полного расходования исходных веществ. Обратимые реакции одновременно протекают в двух взаимно противоположных направлениях. Такие реакции не доходят до конца ни в одном из направлений, ни одно из реагирующих веществ не расходуется полностью.
Состояние системы, характеризующееся одновременным протеканием с одинаковыми скоростями двух противоположно направленных химических процессов, называется химическим равновесием. В состоянии равновесия концентрации всех веществ остаются неизменными.
Признаки химического равновесия:
- состояние системы неизменно во времени при отсутствии внешних воздействий;
- состояние системы изменяется под влиянием внешних воздействий, сколь бы малы они ни были; через некоторое время в такой системе вновь устанавливается равновесие, но уже при другом соотношении равновесных концентраций всех веществ;
- состояние системы не зависит от того, с какой стороны она подходит к равновесию (со стороны прямой или обратной реакции);
- при снятии внешнего воздействия система вновь возвращается в исходное состояние.
В изобарно-изотермических условиях (P; T=const) при равновесии изменение энергии Гиббса системы равно нулю (DG=0).
Рассмотрим условную обратимую реакцию
aA+bB⇄ cC+dD.
Закондействующих масс для нее запишется в виде:

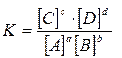 , (2.3.8)
, (2.3.8)
где К – константа равновесия;
[A], [B], [C], [D] – равновесные концентрации веществ;
a, b, c, d – стехиометрические коэффициенты в уравнении реакции.
Константа равновесия зависит от температуры и природы веществ, но не зависит от их концентраций Чем больше величина константы равновесия, тем в большей степени равновесие смещено в сторону образования продуктов реакции. Таким образом, константа равновесия характеризует глубину протекания процесса к моменту равновесия.
Для реакций с участием газов константу равновесия (Кр)можно выразить и через парциальные давления газообразных веществ. Если газы не сильно отличаются по свойствам от идеальных, то между константой, выраженной через парциальные давления (Кр), и константой, выраженной через концентрации (Кс), существует связь:
Kp=Kc×(RT)Dn, (2.3.9)
где Dn– изменение числа моль газообразных веществ в ходе реакции в соответствии с ее стехиометрией.
Константа равновесия при температуре Т связана с изменением стандартной энергии Гиббса реакции DG0 при той же температуре соотношением
DG0= - RT×lnK. (2.3.10)
В гетерогенных реакциях концентрация конденсированной фазы практически постоянна, она в неявной форме входит в константу равновесия. В выражение для константы равновесия концентрации конденсированной фазы не включаются.
При изменении внешних условий равновесие смещается потому, что эти изменения по-разному влияют на скорости прямой и обратной реакций. Равновесие смещается в сторону той реакции, скорость которой становится больше.
На равновесие влияет изменение температуры, концентрации веществ, давления в системе (если реакция идет с изменением числа моль газообразных веществ). Введение катализатора не смещает равновесие, так как он в равной мере изменяет скорость как прямой, так и обратной реакции. Катализатор лишь сокращает время достижения системой состояния равновесия.
В общем случае направление смещения равновесия определяется принципом Ле Шателье: если на систему, находящуюся в равновесии, оказать внешнее воздействие, то равновесие сместится в том направлении, которое ослабляет это воздействие.
Пример 1
Во сколько раз возрастет скорость реакций:
а) C + 2 H2 = CH4
б) 2 NO + Cl2 = 2 NOCl
при увеличении давления в системе в три раза?
Решение
Увеличение давления в системе в три раза эквивалентно увеличению концентрации каждого из газообразных компонентов в три раза.
В соответствии с законом действующих масс запишем кинетические уравнения для каждой реакции.
а) Углерод представляет собой твердую фазу, а водород газовую. Скорость гетерогенной реакции не зависит от концентрации твердой фазы, поэтому она не входит в кинетическое уравнение. Скорость первой реакции описывается уравнением 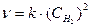
Пусть начальная концентрация водорода равнялась х, тогда v1 = kх2. После увеличения давления в три раза концентрация водорода стала 3х, а скорость реакции v2 = k(3х)2 = 9kх2. Далее найдем отношение скоростей:
v1:v2 = 9kx2:kx2 = 9.
Итак, скорость реакции возрастет в 9 раз.
б) Кинетическое уравнение второй реакции, которая является гомогенной, запишется в виде 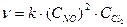 . Пусть начальная концентрация NO равна х, а начальная концентрация Сl2 равна у, тогда v1 = kx2y; v2 = k(3x)23y = 27kx2y;
. Пусть начальная концентрация NO равна х, а начальная концентрация Сl2 равна у, тогда v1 = kx2y; v2 = k(3x)23y = 27kx2y;
v2:v1 = 27.
Скорость реакции возрастет в 27 раз.
Пример 2
Температурный коэффициент скорости реакции g равен 2,8. На сколько градусов была повышена температура, если время протекания реакции сократилось в 124 раза?
Решение
В соответствии с правилом Вант-Гоффа v1 = v2× 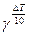 . Время реакции t есть величина, обратно пропорциональная скорости, тогда v2/v1 = t1/t2 = 124.
. Время реакции t есть величина, обратно пропорциональная скорости, тогда v2/v1 = t1/t2 = 124.
t1/t2 = 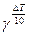 = 124
= 124
Прологарифмируем последнее выражение:
lg( 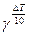 ) = lg124;
) = lg124;
DТ/10×lgg= lg124;
DT = 10×lg124 / lg2,8 » 470.
Температура была повышена на 470.
Пример 3
При повышении температуры с 100С до 400С скорость реакции возросла в 8 раз. Чему равна величина энергии активации реакции?
Решение
Отношение скоростей реакции при различных температурах равно отношению констант скорости при тех же температурах и равно 8. В соответствии с уравнением Аррениуса
k2 / k1 = A× 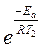 / A
/ A 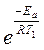 = 8
= 8
Так как предэкспоненциальный множитель и энергия активации практически не зависят от температуры, то
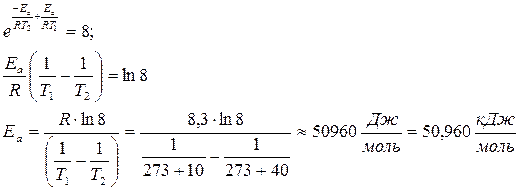
Пример 4
При температуре 973 К константа равновесия реакции
NiO+H2 = Ni+H2O(г)
равна 0,32. Рассчитать равновесные концентрации веществ газовой смеси, если начальная концентрация водорода равна 3 моль/л.
Решение
Считаем, что начальная концентрация паров воды равнялась нулю. Выражение для константы равновесия данной гетерогенной реакции имеет следующий вид: 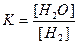 .
.
Пусть к моменту равновесия концентрация паров воды стала равна х моль/л. Тогда в соответствии со стехиометрией реакции, концентрация водорода уменьшилась на х моль/л и стала равной (3 – х) моль/л.
Подставим равновесные концентрации в выражение для константы равновесия и найдем х:
К = х / (3 – х); х / (3 – х)=0,32; х=0,73 моль/л.
Итак, равновесная концентрация паров воды равняется 0,73 моль/л, равновесная концентрация водорода равняется 3 – 0,73 = 2,27 моль/л.
Пример 5
Как повлияет на равновесие реакции 2SO2+O2 ⇄2SO3; DH= -172,38 кДж:
1) увеличение концентрации SO2, 2) повышение давления в системе,
3) охлаждение системы, 4) введение в систему катализатора?
Решение
В соответствии с принципом Ле Шателье, при увеличении концентрации SO2 равновесие сместится в сторону процесса, приводящего к расходованию SO2, то есть в сторону прямой реакции образования SO3.
Реакция идет с изменением числа моль газообразных веществ, поэтому изменение давления приведет к смещению равновесия. При повышении давления равновесие сместится в сторону процесса, противодействующего данному изменению, то есть идущего с уменьшением числа моль газообразных веществ, а, следовательно, и с уменьшением давления. В соответствии с уравнением реакции, число моль газообразных исходных веществ равно трем, а число моль продуктов прямой реакции равно двум. Поэтому при повышении давления равновесие сместится в сторону прямой реакции образования SO3.
Так как DН< 0, то прямая реакция идет с выделением тепла (экзотермическая реакция). Обратная реакция будет протекать с поглощением тепла (эндотермическая реакция). В соответствии с принципом Ле Шателье, охлаждение вызовет смещение равновесия в сторону реакции, идущей с выделением тепла, то есть в сторону прямой реакции.
Введение в систему катализатора не вызывает смещения химического равновесия.
Пример 6
Вычислить константу равновесия реакции FeO(к)+H2(г) ⇄Fe(к)+H2O(г) при 250С. В какую сторону смещено равновесие? Определить температуру установления равновесия, если все вещества находятся в стандартных состояниях, а зависимостью DH0 и DS0 от температуры можно пренебречь.
Решение
Константа равновесия связана с изменением стандартной энергии Гиббса реакции уравнением 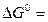
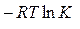 , следовательно,
, следовательно, 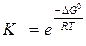 .
.
Воспользовавшись справочными значениями стандартных энергий Гиббса образования веществ, найдем DG0р-ции:
DG0р-ции=DG0(H2O(г))+DG0(Fe(к))-DG0(FeO(к))-DG0(H2(г))= -228,61 кДж/моль + + 0 – (-244,3 кДж/моль) – 0 = 15,59 кДж = 15,59 × 103 Дж
К= 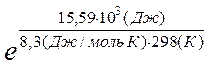 =0,0018
=0,0018
Константа равновесия меньше единицы, следовательно, равновесие при 250С (298 К) смещено в сторону обратной реакции.
В состоянии равновесия DG0= 0. Так как DG0= DН0 - TDS0, то равновесие установится при температуре T=DН0 / DS0.
Воспользовавшись справочными значениями стандартных энтальпий образования веществ и стандартных энтропий, вычислим DН0р-ции и DS0р-ции.
DН0р-ции=DН0(Н2О(г))+DН0(Fe(к))- DН0(FeO(к)) -DН0(Н2(г))= -241,82 кДж/моль+ + 0 – (- 263,7 кДж/моль) – 0 = 21,88 кДж.
DS0р-ции=S0(Н2О(г)) + S0(Fe(к)) - S0(FeO(к)) - S0(Н2(г)) =
=0,1887 кДж/моль× К + 0,02715 кДж/моль× К – 0,05879 кДж/моль× К –
- 0,13058 кДж/моль× К = 0,02648 кДж/К.
Найдем значение температуры, при которой установится равновесие:
Т = 21,88 кДж : 0,02648 кДж/К = 826 К.
