Сильные электролиты. Активная концентрация. Ионная сила раствора.
Сильные электролиты — химические соединения, молекулы которых в разбавленных растворах практически полностью диссоциированы на ионы. Степень диссоциации таких электролитов близка к 1. К сильным электролитам относятся многие неорганические соли, некоторые неорганические кислоты и основания в водных растворах, а также в растворителях, обладающих высокой диссоциирующей способностью (спирты, амиды).
Активной концентрацией-электролита(α) называется отношение числа его молекул, распавшихся в данном растворе на ионы, к общему числу его молекул в растворе, 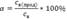


Ионная сила раствора — мера интенсивности электрического поля, создаваемого ионами в растворе. Полусумма произведений из концентрации всех ионов в растворе на квадрат их заряда.
22.Диссоциация воды. Ионное произведение воды. Водородные показатель рН
Вода является слабым электролитом, в незначительной степени она диссоциирует на
ионы. H2O ↔ H+ + OH-
Запишем выраженеи константы диссоциации воды Kд = [H+]*[OH-] / [H2O]
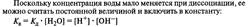
Произведение молярных концентраций ионов Н+ и ОН- называют ионным произведением воды Кв.

Величина рН называется водородным покзаателем. рН = -lg [H+] = -lg (1*10^-7) = 7


23.Гидролиз солей. Роль в живом организме.
Гидролизом соли называется обменная реакция соли с водой. В большинстве случаев это обратимая реакция. Гидролиз является реакцией, обратной нейтрализации – взаимодействию кислот с основаниями. Гидролиз – эндотермический процесс, поэтому он усиливается с повышением температуры.





Живые организмы осуществляют гидролиз различных органических веществ в ходе реакций катаболизма при участии ферментов. Например,в ходе гидролиза при участии пищеварительных ферментов белки расщепляются на аминокислоты, жиры — на глицерин и жирные кислоты, полисахариды (например, крахмал и целлюлоза) — на моносахариды (например,на глюкозу), нуклеиновые кислоты —на свободные нуклеотиды.
24.Современная модель состояния электрона в атоме. Квантовые числа. Принцип Паули.

Под состоянием электрона в атоме понимают совокупность информации об энергии определенного электрона и пространстве, в котором он находится. Мы уже знаем, что электрон в атоме не имеет траектории движения, то есть можно говорить лишь о вероятности нахождения его в пространстве вокруг ядра. Он может находиться в любой части этого пространства, окружающего ядро, и совокупность различных положений его рассматривают как электронное облако с определенной плотностью отрицательного заряда. Пространство вокруг атомного ядра, в котором наиболее вероятно нахождение электрона, называется орбиталью. Важнейшей характеристикой движения электрона на определенной орбитали является энергия его связи с ядром. Электроны, обладающие близкими значениями энергии, образуют единый электронный слой или энергетический уровень. Энергетические уровни нумеруют, начиная от ядра: 1, 2, 3, 4, 5, 6 и 7.

Целое число n, обозначающее номер энергетического уровня, называют главным квантовым числом.Оно характеризует энергию электронов, занимающих данный энергетический уровень. Наименьшей энергией обладают электроны первого энергетического уровня, наиболее близкого к ядру. По сравнению с электронами первого уровня электроны последующих уровней будут характеризоваться большим запасом энергии. Следовательно, наименее прочно связаны с ядром атома электроны внешнего уровня.

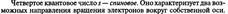
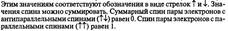

25.Распределение электронов в атоме. Правило Хунда.

