Энтальпия, или тепловой эффект химической реакции, зависит от природы и состояния исходных веществ и конечных веществ и не зависит от пути, по которому протекает данная реакция.
Закон Гесса является вполне строгим для процессов, происходящих при постоянном давлении или при постоянном объёме. Для этих процессов он может рассматриваться как частная форма выражения закона сохранения энергии применительно к химическим реакциям.
| Герман Иванович Гесс (7.VIII 1802—12.XII 1850). Русский химик, академик Петербургской АН (с 1830). Родился в Женеве 7 августа 1802 г. Окончил Дерптский университет (доктор медицины, 1825). Совершенствовал образование в Стокгольмском университете (1825). С 1830 – профессор Петербургского технологического института, в 1832–1849 –Петербургского горного института.Один из основоположников термохимии. Значительно раньше J. П. Ю. Ю. Томсена и П. Э. М. Бертло выдвинул (1840) положение, согласно которому величины тепловых эффектов реакции могут служить мерой химического сродства. |  |
Открыл (1840) основной закон термохимии – закон постоянства количества теплоты, по которому тепловой эффект реакции зависит только от начального и конечного состояния реагирующих веществ, а не от количества её стадий (закон Гесса). Доказал (1842), что при смешении нейтральных солевых растворов тепловой эффект отсутствует (правило термонейтральности). Установил, что при нейтрализации эквивалента сильной кислоты сильным основанием выделяется одинаковое количество теплоты (13,5 ккал). Открыл и определил (1830–1834) состав четырех новых минералов – вертита, уваровита, гидроборацита и фольбортита. Предложил (1833) способ получения теллура из теллурида серебра — минерала, который был им впервые изучен. Изучал (1832) оксиды кобальта. Установил каталитические и адсорбционные свойства мелкораздробленной платины. Одним из первых изучал состав кавказских нефтей. Открыл сахарную кислоту. Написал учебник «Основания чистой химии» (1831), выдержавший семь изданий.
В честь Г.И.Гесса теллурид серебра назван гесситом.
Закон Гесса можно проиллюстрировать следующей схемой:
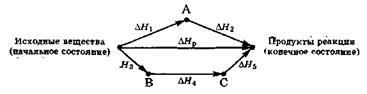
Переход системы из начального состояния в конечное можно осуществить разными путями:
= непосредственно химической реакцией, энтальпия которой равна DHр;
= в результате двухстадийной реакции через промежуточное состояние А в результате двухстадийной реакции, энтальпии отдельных стадий которой равны DH1 и DH2;
= в результате трёхстадийной реакций через промежуточные состояния В и С в результате трёхстадийной реакций, энтальпии отдельных стадий которой равны DH3, DH4 и DH5.
Согласно закону Гесса:
DHр = DH1 + DH2 = DH3 + DH4 + DH5.
В термохимических расчётах большое значение имеют следствия из закона Гесса.
Первое следствие. Энтальпия химической реакции равна разности алгебраических сумм энтальпий образования продуктов реакции и исходных веществ:
DHр = ∑vкон DHкон (Yкон) - ∑vисх DHисх (Xисх),
где DH (Y), DH (X) - энтальпии образования продуктов реакции Y и исходных веществ X;
vкон. и vнач - соответствующие стехиометрические коэффициенты в уравнении химической реакции.
Например, для реакции образования хлороводорода
Н2 + Cl2 = НCl
энтальпия реакции равна
DHр = 2DH (НCl) – [DH (Н2) + DH (Cl2)
Первое следствие позволяет определять энтальпии различных химических реакций (в том числе и биохимических, осуществление которых in vitro* невозможно), используя табличные значения стандартных энтальпий образования исходных веществ и продуктов реакции.
Рассчитаем, например, энтальпию реакции получения мочевины в организме из аммиака и оксида углерода (IV):
2NH3(г) + СО2(г) = СО(NH2)2(т) + Н2О(г)
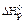 = [
= [ 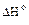 (СО(NH2)2(т) +
(СО(NH2)2(т) + 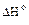 ( Н2О(г))] – [2
( Н2О(г))] – [2 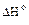 ( NH3(г) +
( NH3(г) + 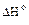 ( СО2(г)) =
( СО2(г)) =
= (–333 – 242) – (–2 ∙ 46 – 394) = 89 кДж/моль.
Второе следствие Энтальпия прямой реакции численно равна энтальпии обратной реакции, но с противоположным знаком:
∆ 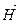 = – ∆
= – ∆ 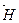 .
.
Рассчитаем, например, стандартную энтальпию реакции фотосинтеза глюкозы, которая является обратной реакцией окисления (горения) глюкозы:
6СО2(г) + 6Н2О(ж) 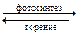 С6Н12О6(т) + 6О2(г)
С6Н12О6(т) + 6О2(г)
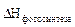 = –
= – 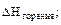
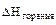 (С6Н12О6(т)) = – 1273 кДж/моль.
(С6Н12О6(т)) = – 1273 кДж/моль.
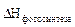 (С6Н12О6(т)) = – (– 1273) = 1273 кДж/моль.
(С6Н12О6(т)) = – (– 1273) = 1273 кДж/моль.
Основным источником энергии для живых организмов является химическая энергия, заключённая в продуктах питания. Для человека главными компонентами пищи являются жиры, углеводы сахара и белки, окисление которых сопровождается выделением энергии. В медицине энергетическую характеристику продуктов питания принято выражать в калориях. Пища представляет собой смесь питательных веществ сложного состава, поэтому калорийность пищи указывается в расчёте на 1 г, а не на 1 моль.
Калорийностью питательных веществ называется энергия, выделяемая при полном окислении (сгорании) 1 г этих веществ.
Взаимосвязь между единицами энергии выражается соотношением: 1 калория = 4,18 Дж.
Согласно закону Гесса теплота, которая выделяется при окислении питательных веществ, не зависит от того, как или где они окисляются, конечно, при условии, что продукты реакции остаются неизменными. Жиры, углеводы и белки окисляются в организме до тех же продуктов, что и при сгорании в калориметре:
“С” 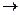 СO2; “Н”
СO2; “Н” 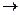 Н2О; “N”
Н2О; “N” 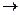 N2*
N2*
Поэтому для энергетической оценки большинства продуктов питания может служить энтальпия реакции их сгорания. Наибольшую энергетическую ценность имеют жиры, при окислении которых выделяется 37,7=39,8 кДж/г (9,0=9,5 ккал/г). В процессе усвоения углеводов в организме человека выделяется 16,5=17,2 кДж/моль (4,0=4,1 ккал/г). На этом же уровне находится и калорийность белков: 16,5=17,2 кДж/г (4,0=4,1 ккал/г). Биоэнергетику организма можно регулировать не только при помощи выбора отдельных продуктов, но, главным образом, их сочетанием. Для взрослого человека суточная норма потребления составляет: жиров – 60=70 г, белков – 80=100 г (при тяжёлом физическом труде – 130=140 г), а потребляемая масса углеводов должна в 4=5 раз превышать массу белков, причём только небольшая часть от этого количества должна быть в виде сахарозы (около 8 г).
В основе научной диетологии лежит соответствие калорийности пищевого рациона энергозатратам человека. Суточная потребность человека в энергии составляет:
8 400=11 700 кДж (2 000=2 800 ккал) при лёгкой работе в сидячем положении (портные, канцелярские работники);
12 500=15 100 кДж (3 000=3 600 ккал) при умеренной и напряженной мышечной работе (учащиеся, студенты, врачи, рабочие-станочники);
16 700=20 900 кДж (4 000=5 000 ккал) при тяжёлом физическом труде (литейщики, кузнецы)
до 30 100 кДж (7 200 ккал) при особо тяжёлом труде (землекопы, косари, спортсмены).
3. ПОНЯТИЕ О САМОПРОИЗВОЛЬНЫХ ПРОЦЕССАХ. ЭНТРОПИЯ
Одним из важнейших аспектов термодинамики является формулировка условий самопроизвольности протекания химических и физико-химических процессов.
Самопроизвольным (или спонтанным) является процесс, который совершается в системе без затраты работы извне и который уменьшает работоспособность системы после его завершения.
Следовательно, самопроизвольно система может переходить только из менее устойчивого состояния в более устойчивое. На основе I закона термодинамики можно сформулировать один из важных принципов самопроизвольности протекания процессов в системе, заключающийся в стремлении системы к минимуму энергии за счёт выделения энергии в окружающую среду.
Этот энергетический принцип особенно важен для систем, которые можно рассматривать как единую частицу.
Например, капля дождя самопроизвольно падает вниз, уменьшая при этом свою потенциальную энергию. Каплю воды необходимо рассматривать как совокупность большого числа молекул, когда происходит процесс её испарения, протекающий самопроизвольно, несмотря на то, что он как эндотермический процесс требует поступления энергии из окружающей среды.
Следовательно, для описания условий протекания самопроизвольных процессов одного энергетического принципа недостаточно, особенно в системах, состоящих из большого числа частиц. Главное изменение, которое происходит при испарении капли, заключается в переходе системы из жидкого состояния (с частично упорядоченным состоянием частиц) в парообразное, в котором частицы не упорядочены. Таким образом, для описания движения в системах, содержащих большое число частиц, необходимо учитывать неупорядоченность расположения и движения этих частиц, то есть энтропию системы (разд. 1).
Значение энтропии как меры неупорядоченности системы зависит от агрегатного состояния и природы веществ (компонентов системы), температуры, давления и сложности данной системы.
Энтропия вещества в газообразном состоянии больше, чем энтропия его в жидком состоянии, а последняя больше энтропии этого вещества в твёрдом состоянии:
S(г) > S(ж) > S(т).
Энтропия простых веществ зависит от их аллотропной модификации:
S(Сграфит) > S(Салмаз); S(О2) < S(О3).
Энтропия системы при повышении температуры возрастает, так как увеличивается неупорядоченность движения частиц:
если Т2 > Т1, то S2 > S1.
Энтропия системы при повышении давления уменьшается, так как снижается неупорядоченность движения частиц:
если p2 > р1, то S2 < S1.
Энтропия системы с увеличением её сложности повышается, так как возрастает число типов частиц и вариантов их расположения.
Для энергетической характеристики веществ при стандартных условиях, наряду со стандартной энтальпией, используют и их стандартную энтропию Sо. В отличие от стандартной энтальпии, стандартная энтропия простых веществ не равна нулю.
В случае идеально упорядоченного кристалла при температуре 0 К его энтропия S = 0. Это даёт естественную нулевую точку отсчёта для значений энтропии (отсутствующую для ранее рассмотренных функций состояния: внутренней энергии U и энтальпии Н) и позволяет измерить или теоретически рассчитать значения энтропии. Поэтому перед символом энтропии веществ не ставят знак изменения (D-дельта). Значения энтропии для стандартных состояний веществ приведены в справочниках термодинамических величин.
Изменение стандартной энтропии в химической реакции ( 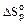 ) определяется разностью алгебраических сумм стандартных энтропии продуктов реакции Yкон. и исходных веществ Хисх. с учётом соответствующих стехиометрических коэффициентов:
) определяется разностью алгебраических сумм стандартных энтропии продуктов реакции Yкон. и исходных веществ Хисх. с учётом соответствующих стехиометрических коэффициентов:
DSр = ∑vкон DSкон (Yкон) - ∑vисх DSисх (Xисх),
где DS (Y), DS (X) - энтропии образования продуктов реакции Y и
исходных веществ X;
vкон.. и vнач.- соответствующие стехиометрические коэффициенты
в уравнении химической реакции.
4. ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ.
ЭНЕРГИЯ ГИББСА
Второй закон (второе начало) термодинамики определяет направленность и пределы протекания самопроизвольных химических и физико-химических процессов, в том числе и биохимических.
Рассмотрим изолированную систему, где исключён обмен энергией и веществом. Допустим, что в изолированной системе находятся два любых газа, например гелий Не и аргон Аr, которые химически и физически не взаимодействуют между собой и не перемешаны. Естественно, что эти газы будут самопроизвольно и необратимо смешиваться, однако свойства системы останутся без изменения, за исключением её энтропии. В исходном состоянии системы, когда газы ещё не смешались, её энтропия (Sнач) меньше, чем после смешивания газов (Sкон), характеризующегося неупорядоченностью расположения и движения молекул газов. Следовательно, в результате самопроизвольного необратимого процесса в изолированной системе её энтропия возростает: DS = Sкон - Sнач > 0. отсюда сформулирован II закон термодинамики гласит для изолированных систем.
