Ход выполнения работы. Обработка результатов. 1. В тщательно вымытый сухой бюкс помещают вчетверо сложенный беззольный фильтр «белая лента», сверху бюкса кладут крышку
1. В тщательно вымытый сухой бюкс помещают вчетверо сложенный беззольный фильтр «белая лента», сверху бюкса кладут крышку, перевернув её на ребро, и высушивают в сушильном шкафу при 1050С в течение часа. Затем тигельными щипцами переносят бюкс с фильтром в эксикатор и охлаждают его в течение 25 – 30 мин.
2. Охлаждённый до комнатной температуры бюкс с фильтром взвешивают на технических, затем на аналитических весах.
3. Проводят второе взвешивание бюкса с фильтром, предварительно поместив его в сушильный шкаф на 30 мин., затем в эксикатор на 25 – 30 мин. Необходимо довести массу бюкса с фильтром до постоянного значения (разность результатов взвешивания не должна превышать ± 0,0002 г). Массу бюкса с фильтром фиксируют в рабочем журнале.
4. Для определения взвешенных веществ отмеряют цилиндром заданный объём контрольной пробы воды и профильтровывают его. Оставшийся на фильтре осадок промывают небольшим количеством дистиллированной воды и влажный фильтр с осадком переносят в бюкс.
5. Бюкс с фильтром и осадком помещают в сушильный шкаф на 1 час при 1050 С, после чего с помощью тигельных щипцов переносят в эксикатор на 25 – 30 мин.
6. Охлаждённый до комнатной температуры бюкс с фильтром и осадком взвешивают на технических и аналитических весах. Массу бюкса с фильтром и осадком доводят до постоянного значения и фиксируют в рабочем журнале.
7. Расчёт концентрации взвешенных веществ в заданной пробе воды производят, используя формулу:
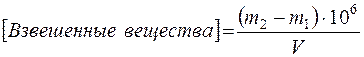 ,
,
где m1 – масса бюкса с фильтром в г;
m2 – масса бюкса с фильтром и осадком в г;
V - объём пробы воды в мл.
Результаты округляют с точностью до 1 мг/л, а если найденная величина превышает 1000 мг/л, то до 10 мг/л.
Требования к отчёту
Письменный отчёт по данной лабораторной работе должен включать:
1) название лабораторной работы;
2) перечень оборудования и реактивов;
3) кратко изложенный ход выполнения работы;
4) экспериментальные данные и расчёты:
1. масса бюкса (указать номер) с фильтром после первого просушивания на технических весах ..,.. г.
2. масса бюкса с фильтром после первого просушивания на аналитических весах ..,… г.
3. масса бюкса с фильтром после второго просушивания на аналитических весах ..,…. г.
4. постоянная масса бюкса с фильтром
m1 = ..,…. г
5. масса бюкса с фильтром и осадком после первого просушивания на технических весах ..,.. г.
6. масса бюкса с фильтром и осадком после первого просушивания на аналитических весах ..,…. г.
7. масса бюкса с фильтром и осадком после второго просушивания на аналитических весах ..,…. г.
8. постоянная масса бюкса с фильтром и осадком
m2 = ..,…. г.
9. [Взвешенные вещества] = , мг/л
Примечание: в начале занятия преподаватель проводит дополнительный инструктаж по технике безопасности и охране труда при работе с электроприборами, используя инструкцию, разработанную на кафедре химии. Преподаватель объясняет и показывает, как надо работать с техническими и аналитическими весами, сушильным шкафом и эксикатором.
ВОПРОСЫ ДЛЯ САМОПОДГОТОВКИ
1. Какие вещества называют взвешенными?
2. Какими аналитическими методами можно определить концентрацию взвешенных веществ?
3. В чём заключается сущность гравиметрического метода определения взвешенных веществ?
4. Правила взвешивания.
5. Перечислить и охарактеризовать операции, необходимые при проведении гравиметрического анализа.
Лабораторная работа № 3
Качественное определение содержания в природных и сточных вода некоторых ионов и веществ
Цель занятия: ознакомить студентов с элементами качественного анализа на примере обнаружения некоторых ионов в водных растворах и питьевой (водопроводной) воде с помощью известных аналитических реакций.
Природные и сточные воды представляют собой сложные дисперсные системы, содержащие в растворённом, коллоидном и взвешенном состояниях различные неорганические и органические вещества. В природных водах из неорганических веществ чаще всего присутствуют хлориды, сульфаты, гидрокарбонаты и карбонаты натрия, калия, кальция, магния, железа, марганца, а также гидросиликаты и силикаты этих металлов; из органических – органические кислоты и их соли, белки и продукты их распада, углеводы и другие соединения. Помимо этого могут присутствовать биогенные вещества, которые возникают в связи с жизнедеятельностью гидробионтов: это – различные формы азота (аммиачный, нитритный, нитратный), фосфора, кремния и железа.
Сточные воды промышленных предприятий, загрязняя природную воду, могут в сильной степени загрязнять её природный состав и делать непригодной для питьевых и хозяйственно-бытовых нужд.
Основные катионы природных вод: Na+, K+, Ca2+, Mg2+, Fe2+, Fe3+; основные анионы: Cl-, SO42-, HCO3-, CO32-, HsiO3-, SiO32-.
В химическом анализе качественное определение катионов и анионов осуществляется посредством специфических реакций, в результате которых образуются либо осадки, либо окрашенные комплексные соединения, либо газы. Такие реакции называются реакциями обнаружения, а используемые при этом реактивы – реагентами на данный ион.
Оборудование и реактивы:
1. Штатив с пробирками.
2. Часовые стекла.
3. Водяная баня.
4. Соляная кислота (1:3).
5. Азотная кислота (1:4).
6. Серная кислота (конц.).
7. Азотная кислота (конц.).
8. 2н. раствор серной кислоты.
9. 2н. раствор гидроксида натрия (гидроксида калия).
10. Хлорид бария (10%-ный раствор).
11. Нитрат серебра (5%-ный раствор).
12. Раствор аммиака (конц.).
13. Раствор аммиака(2 н.).
14. Раствор NH4Cl (2 н.)
15. Пероксид водорода (5%-ный раствор).
16. Роданид калия (аммония) – 20%-ный раствор.
17. Раствор K4[Fe(CN)6].
18. Раствор K3[Fe(CN)6].
19. Метилоранж – 0,2%-ный раствор.
20. Фенолфталеиновая бумажка.
21. Реактив Несслера (раствор K2[HgI4] в растворе КОН).
22. Раствор дифениламина ((С6Н5)2NH).
23. Водные растворы Na2SO4, NaCl, NH4Cl, NaNO2, NaNO3, FeCl3, FeSO4 (0,2н.), (NH4)2CO3, (NH4)2C2O4.
24. Хлорная вода.
25. Известковая вода (раствор гидроксида кальция).
Ход выполнения работы
ЧАСТЬ 1. Обнаружение основных анионов и катионов природных вод и «активного хлора» с помощью качественных реакций
РЕАКЦИИ ОБНАРУЖЕНИЯ КАТИОНОВ
ОПЫТ 1.Реакция обнаружения иона кальция
1. Действие карбоната аммония (NH4)2CO3
Карбонат аммония образует с ионами кальция белый аморфный осадок, при нагревании и последующим отстаиванием переходящий в мелко кристаллический: Са2+ + СО32− = СаСО3.
Реакцию проводят в аммиачной среде в присутствии NH4Cl при температуре 700 С. Такие условия позволяют подавить гидролиз карбоната аммония.
В пробирку внести 2 капли раствора соли кальция, добавьте по 1 капле 2н. растворов NH4OH и NH4Cl, смесь нагрейте на водяной бане и добавьте3 капли раствора (NH4)2CO3.
Действие оксалата аммония
Оксалат аммония (NH4)2C2O4 образует белый осадок с ионами кальция: Са2+ + С2О42− = СаС2О4.
К 2 каплям раствора соли кальция прибавьте 2 капли раствора оксалата аммония.
ОПЫТ 2.Реакция обнаружения иона железа
Fe2+, Fe3+ - формулы ионов железа (II) и железа (III). Для обнаружения ионов железа используют ряд цветных реакций, протекающих с образованием окрашенных комплексных соединений.
Реакции обнаружения Fe3+
1. Реакция с гексацианоферратом (II) калия K4[Fe(CN)6]
В пробирку поместите несколько капель раствора соли трёхвалентного железа, подкислите 1 -2 каплями раствора HCl, прибавьте 2 – 3 капли раствора K4[Fe(CN)6]. Выпадает тёмно-синий осадок берлинской лазури Fe4[Fe(CN)6]3. Сильное подкисление и избыток реактива приводит к растворению осадка.
4Fe3+ + 3[Fe(CN)6]4− = Fe4[Fe(CN)6]3↓
4FeCl3 + 3K4[Fe(CN)6] = Fe4[Fe(CN)6]3↓ + 12KCl
