Вопрос 48. Признаки объектов коллоидной химии. Классификация дисперсных систем.
Для объектов коллоидной химии характерны два общих признака - гетерогенность и дисперсность. Все особые свойства, присущие им, являются следствиями или функциями гетерогенности и дисперсности.
Гетерогенность(многофазность) - признак, указывающий на наличие межфазной поверхности раздела. В отличие от других гетерогенных систем дисперсные системы обладают высокой степенью раздробленности и большим количеством частиц дисперсной фазы.
Дисперсность(раздробленность) определяется размерами частиц дисперсной фазы. Чем меньше линейные размеры частиц фазы, тем больше её дисперсность. Количественно дисперсность может быть выражена такими характеристиками:
1) линейные размеры частиц а. Размерность а в системе СИ - м. В случае изометрической формы частиц – кубической или сферической, под линейными размерами подразумевается диаметр или ребро куба, а в случае нитей, капилляров, плёнок и других неизометрических частиц - это длина наименьшей оси частицы.
2) степень дисперсности D, часто называемая просто дисперсностью. D - это величина, обратная линейным размерам частиц D = 1/a. Размерность D в системе СИ – м-1. D можно представить себе как число частиц, укладывающихся на единице длины, т. е. на 1 м.
3) удельная поверхность S уд, определяемая отношением межфазной поверхности к объёму или к массе частиц дисперсной фазы.
Классификация дисперсных систем:
Система называется дисперсной, если в каком-либо веществе (дисперсионной среде) распределено другое вещество (дисперсная фаза) в виде мельчайших частиц. Все дисперсионный системы по размеру частиц дисперсионной фазы можно классифицировать на молекулярно-ионные (меньше одного нм), коллоидные (от одного до ста нм), грубодисперсные (более ста нм). Молекулярно-дисперсные системы. Указанные системы содержат частицы, размер которых не превышает одного нм. К данной группе относятся разнообразные истинные растворы неэлектролитов: глюкозы, мочевины, спирта, сахарозы. Грубодисперсные системы характеризируются наиболее крупными частицами. К ним относят эмульсии и суспензии. Дисперсные системы, у которых твердое вещество локализируется в жидкой дисперсионной среде (раствор крахмала, глины), называются суспензиями. Эмульсии – это системы, которые получают в результате смешивания двух жидкостей, где одна в виде капелек диспергирована в другой (масло, толуол, бензол в воде или капельки триацилглицеролов (жира) в молоке
Коллоидные дисперсные системы. В них размеры коллоидных частиц достигают до 100 нм. Такие частицы легко проникают через поры бумажных фильтров, однако не проникают через поры биологических мембран растений и животных. Поскольку коллоидные частицы (мицеллы) имеют электрозаряд и сольватные ионные оболочки, благодаря которым они остаются во взвешенном состоянии, они достаточно продолжительное время могут не выпадать в осадок. Ярким примером коллоидной системы являются растворы желатина, альбумина, гуммиарабика, коллоидные растворы золота и серебра. Степень дисперсности позволяет различить гомогенные и гетерогенные дисперсные системы. В гомогенных дисперсных системах частицы фазы измельчены до молекул, атомов и ионов. Примером таких дисперсионных систем может быть раствор глюкозы в воде (молекулярно-дисперсная система) и кухонной соли в воде (ионно-дисперсная система). Они являются истинными растворами. Размер молекул дисперсной фазы не превышает одного нанометра.
Вопрос 49. Поверхностное натяжение. Адсорбция.
Пове́рхностноенатяже́ние — термодинамическая характеристика поверхности раздела двух находящихся в равновесии фаз, определяемая работой обратимого изотермокинетического образования единицы площади этой поверхности раздела при условии, что температура, объём системы и химические потенциалы всех компонентов в обеих фазах остаются постоянными.
Поверхностное натяжение имеет двойной физический смысл — энергетический (термодинамический) и силовой (механический). Энергетическое (термодинамическое) определение: поверхностное натяжение — это удельная работа увеличения поверхности при её растяжении при условии постоянства температуры. Силовое (механическое) определение: поверхностное натяжение — это сила, действующая на единицу длины линии, которая ограничивает поверхность жидкости.
Адсорбция — увеличение концентрации растворенного вещества у поверхности раздела двух фаз (твердая фаза — жидкость, конденсированная фаза — газ) вследствие нескомпенсированности сил межмолекулярного взаимодействия на разделе фаз. Адсорбция является частным случаем сорбции, процесс, обратный адсорбции — десорбция
Поглощаемое вещество, ещё находящееся в объёме фазы, называют адсорбтив, поглощённое — адсорбат. В более узком смысле под адсорбцией часто понимают поглощение примеси из газа или жидкости твёрдым веществом (в случае газа и жидкости) или жидкостью (в случае газа) — адсорбентом. Адсорбция — всеобщее и повсеместное явление, имеющее место всегда и везде, где есть поверхность раздела между фазами. Наибольшее практическое значение имеет адсорбция поверхностно-активных веществ и адсорбция примесей из газа либо жидкости специальными высокоэффективными адсорбентами. В качестве адсорбентов могут выступать разнообразные материалы с высокой удельной поверхностью: пористый углерод (наиболее распространённая форма — активированный уголь), силикагели, цеолиты а также некоторые другие группы природных минералов и синтетических веществ.
Вопрос 50. Молекулярно-кинетические свойства свободнодисперсных систем (броуновское движение, осмос, диффузия).
Молекулярно-кинетическими называются свойства, которые связаны с хаотическим тепловых движением частиц. К ним относятся – броуновское движение, диффузия, осмотическое давление, седиментация. Эти свойства определяются размерами частиц и их фракционным составом.
Броуновское движение – хаотическое движение частиц дисперсной фазы под действием ударов частиц дисперсионной среды. Этот вид движения характерен для частиц с размерами < 10-6 м. Если размеры частиц дисперсной среды больше, то частицы лишь колеблются. Интенсивность броуновского движения зависит от размера частиц, температуры, вязкости дисперсионной среды.
Диффузия – процесс самопроизвольного переноса вещества за счет теплового движения, который приводит к выравниванию концентраций или к установлению равновесных концентраций.
Диффузия имеет определенную скорость, которая определяется законом Фика: Скорость диффузии прямо пропорциональна разности концентраций и площади поверхности, через которую происходит диффузия.
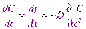
где - скорость диффузии, кг/с
S – площадь поверхности,
– градиент концентраций, кг/м4
D – коэффициент диффузии, м2/с
D – экспериментально определяемая величина.
D=
где kб – константа Больцмана;
r –радиус частицы;
h – вязкость среды. Определив D, можно рассчитать размеры коллоидных частиц. Для коллоидных частиц коэффициент диффузии 100 раз меньше, чем для атомов и молекул.
Осмотическое давление подчиняется закону Вант-Гоффа:
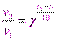
где Сn – частичная концентрация, м-3 – число частиц в единице объема, определяется отношением массы дисперсной фазы к массе коллоидной частицы. Осмотическое давление коллоидных растворов в 1000 раз меньше осмотического давления истинных растворов.
