Зависимость механических свойств сплавов от толщины стенок отливок 9 страница
Дегазация хлористыми солями. В качестве дегазаторов алюминиевых сплавов используют хлориды различных элементов: хлористый цинк ZnCl2, хлористый марганец МпС12, хлористый барий ВаС13, гексахлорэтан С2С16 и др. Дегазирующие соли вводятся в глубину расплава с помощью колокольчика, показанного на рис. 8.9, в.
Действие хлоридов основано на том, что в результате их взаимодействия с алюминием в расплаве образуется летучий хлористый алюминий (температура кипения А1С13 равна 183 °С):
3ZnCl2 + 2А1 = 2А1С13Т + 3Zn, ЗМпС12 + 2А1 = 2А1С13Т + ЗМп, 4ВС13 + 4А1 = 4А1С13Т + 4В, С2С16 + 2А1 = 2А1С13Т + 2С.
Пузырьки хлористого алюминия, выходя на поверхность ванны, уносят с собой газы и твердые неметаллические включения, т. е. действуют аналогично пузырькам СО при кипении стали.
Сущность всех рассмотренных способов дегазации состоит в том, чтобы создать поверхность раздела металл—газовая фаза, над которой парциальное давление растворенного газа меньше равновесного, описываемого уравнением Сивертса.
Вымораживание. Способ основан на том, что растворимость водорода в расплаве алюминия в процессе кристаллизации снижается примерно в 10 раз. При охлаждении расплавленного металла в печи до температуры солидуса из него удаляются газы, растворившиеся в процессе расплавления, когда защита покровным шлаком была недостаточно эффективной. После этого металл перегревают до заданной температуры, но это происходит под сплошным слоем покровного флюса и не приводит к насыщению металла газами.
Метод практически не применяется в связи с низкой производительностью и большими энергозатратами.
8.7. Раскисление металла
Как уже отмечалось, в подавляющем большинстве случаев плавка литейных сплавов сопровождается преднамеренным или нежелательным, но неизбежным, окислением основного металла и легирующих элементов. При плавке стали и медных сплавов оксиды основного металла растворяются в нем, ухудшая качество сплава. Поэтому в конце плавки стали и медных сплавов проводят раскисление металла, т. е. восстановление оксидов основного металла.
В качестве раскислителей применяют элементы, имеющие большее сродство к кислороду, чем основной металл. При этом важно, чтобы образующиеся оксиды раскислителя не растворялись в металле, но удалялись в шлак или газовую фазу.
Кроме двух указанных свойств раскислители должны быть экологически чистыми, недорогими и недефицитными.
Сплавы на основе алюминия и магния не раскисляют, так как эти металлы обладают исключительно высоким сродством к кислороду, сами образуют прочные нерастворимые оксиды, которые можно удалить из расплава в процессе дегазации.
При плавке чугуна специальной операции раскисления не проводят в связи с тем, что функцию раскисления выполняет легирующий элемент чугуна — кремний, содержание которого в металле всегда превышает требуемое количество раскислителя, вводимого в расплав. По той же причине не раскисляют сплавы на основе цинка, содержащие не менее 4 % А1.
Таким образом, закономерности процесса раскисления имеют существенное значение только для плавки стали и медных сплавов. При плавке литейных сталей чаще всего используется глубинное или осаждающее раскисление. В качестве раскислителей применяют марганец (в виде ферромарганца), кремний (в виде ферросилиция). Содержание элемента-раскислителя в ферросплаве составляет 45... 75 %. Раскисление протекает по следующим реакциям с положительным тепловым эффектом Q:
[FeO] + [Mn] = [Fe] + (MnO) + Q,
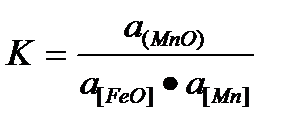
или
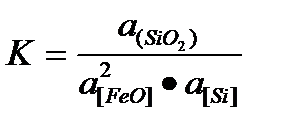
2[FeO] + [Si] = 2[Fe] + (Si02) + Q,

В результате реакций образуются малорастворимые в металле оксиды марганца или кремния, плотность которых меньше плотности стали, т.е. образующийся «осадок» всплывает в шлак, отсюда название метода — «осаждающий». Этот метод называют также «глубинным», так как раскислитель  вводят в глубь ванны металла.
вводят в глубь ванны металла.
Важно отметить, что всплытие продуктов раскисления затруднено из-за малых размеров образующихся частиц МпО и Si02, а также по причине значительной вязкости расплава. Кроме того, в результате раскисления прекращается кипение стали и выделение пузырьков СО, которое способствовало флотации неметаллической мути при кипении. Поэтому при осаждающем раскислении невозможно получить сталь, чистую от неметаллических включений, что является существенным недостатком рассматриваемого метода. Однако этот метод получил наибольшее распространение как самый простой и дешевый.
Уменьшения количества оставшихся в стали неметаллических включений добиваются применением комплексных раскислите - лей. Они представляют собой сплавы нескольких раскислителей: силикомарганец (Si + Мп), силикокальций (Si + Са), сплав АМС (А1 + Мп + Si), сплав КМК (Si + Мп + Са) и др. При использовании комплексных раскислителей продукты реакций раскисления вступают во взаимодействие между собой, образуя более крупные и легко всплывающие включения. (Напомним, что Si02 является кислотным, или, что у практиков чаще используется, «кислым» оксидом, а МпО и СаО — это основные оксиды).
Кроме того, взаимодействие продуктов реакций раскисления между собой приводит к уменьшению их активности и смещению равновесия реакций в сторону более полного раскисления. Количество вводимого раскислителя должно быть необходимым и достаточным для полного восстановления оксида железа, растворенного в металле. Присадка избыточного количества раскислителя приводит к увеличению содержания в металле элемента-раскис- лителя по сравнению с заданным химическим составом стали. Поэтому в процессе раскисления отбирают пробы «на раскислен- ность металла», в частности «на ковкость» и «на рост».
Технологическая проба «на ковкость» основана на том, что оксид железа сообщает сталям красноломкость. Поэтому после введения первой порции раскислителя отливают небольшой цилиндрический образец, и после затвердевания его расковывают в лепешку. Образование трещин по краям лепешки свидетельствует о красноломкости стали и необходимости введения дополнительной порции раскислителя.
Проба «на рост» основана на том, что в процессе кристаллизации недостаточно раскисленной стали происходит реакция кипения:
FeO + С = Fe + COt - Q.
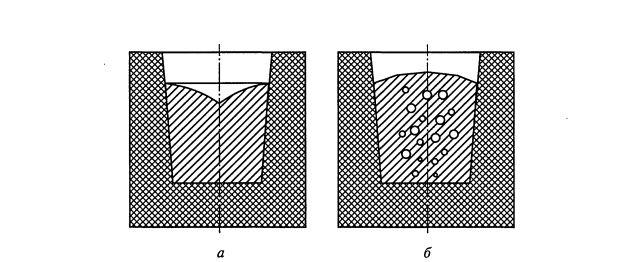 Рис. 10. Технологическая проба раскисленности стали (проба «на рост»): а — образец раскисленной стали; б — образец недораскисленной стали Рис. 10. Технологическая проба раскисленности стали (проба «на рост»): а — образец раскисленной стали; б — образец недораскисленной стали |
Эта эндотермическая реакция протекает при относительно низкой температуре (в интервале кристаллизации) благодаря тому, что зарождение пузырьков СО облегчается образованием твердых кристаллов металла, а также выделением скрытой теплоты кристаллизации. Образующиеся при этом пузырьки СО заполняют усадочные пустоты в затвердевающем образце и препятствуют образованию утяжины на его свободной поверхности. Поэтому образец недораскисленной стали имеет выпуклую или плоскую свободную поверхность, тогда как наличие утяжины на образце свидетельствует о раскисленности стали (рис. 8.10).
После получения образца раскисленной стали предварительное раскисление заканчивают. При выпуске стали из печи проводят окончательное раскисление алюминием, который задают на желоб печи или в ковш, под струю металла. Раскислительная способность алюминия настолько велика, что при остаточном содержании его в стали 0,001 % содержание растворенного кислорода в стали составляет около 0,001 %, что приближается к пределу определения концентрации кислорода.
Для каждой марки или группы марок стали разрабатывают и используют свою технологию раскисления.
Диффузионное раскисление основано на применении закона распределения, согласно которому равновесное отношение концентраций оксида железа в шлаке (FeO) и в металле [FeO] является постоянной величиной при данной температуре, не зависящей от абсолютного количества оксида в системе, т.е.
| а |
^Feo = (FeO,%)/[FeO,%] = const.
С позиции закона распределения безразлично, куда вводится раскислитель — в шлак или в металл — в обоих случаях фазы будут раскисляться пропорционально благодаря диффузии FeO из одной несмешивающейся фазы в другую.
При диффузионном раскислении стали раскислитель вводят в шлак. Обычно при диффузионном раскислении используют сильные восстановители: углерод (в виде электродного боя, древесного угля), ферросилиций, алюминий.
Преимущество диффузионного раскисления состоит в том, что продукты реакций раскисления образуются и остаются в шлаке и не «замутняют» металл. Однако скорость процесса диффузионного раскисления значительно меньше скорости глубинного (осаждающего) раскисления даже при высокой температуре металла и шлака. Это приводит к существенному уменьшению производительности печи.
Раскисление медных сплавов проводится введением раскислителей как в расплав, так и в шлак (поверхностное раскисление). Некоторые из используемых раскислителей способствуют дегазации расплава и увеличению электропроводности медных отливок.
Науглероживание расплавов железа
Процесс растворения углерода в расплавах железа имеет большое практическое значение в связи с широким распространением так называемых «синтетических» чугунов. Производство отливок из синтетических чугунов, выплавляемых с использованием в шихте повышенного количества стального лома, оказалось экономически и экологически выгодным. Однако в процессе переплава дешевых стальных, отходов требуется существенно повысить содержание углерода в расплаве.
В общем виде процесс растворения углерода с поверхности на- углероживателя в расплаве железа можно представить в виде схемы, изображенной на рис. 11.
На схеме косой штриховкой обозначен науглероживатель, по поверхности которого со скоростью v движется расплав железа. В слое толщиной 8 характер движения расплава ламинарный (т. е. траектории движения струек металла параллельна одна другой). Выше ламинарного слоя характер движения потока расплава турбулентный, что обозначено завихренными стрелками.
В слое с ламинарным характером движения массоперенос углерода от одной струйки расплава к другой происходит так же, как в неподвижной жидкости, путем диффузии. Поэтому этот слой называют ламинарным диффузионным.
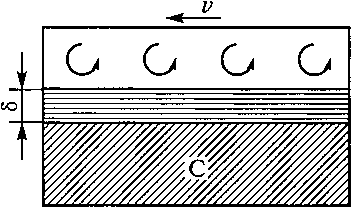 Рис. 11. Схема процесса науглероживания Рис. 11. Схема процесса науглероживания |
Массоперенос углерода в турбулентном слое осуществляется с большей скоростью, чем в ламинарном. Поэтому в целом скорость процесса растворения углерода в расплаве определяется скоростью массопереноса в ламинарном диффузионном слое и описывается уравнением:
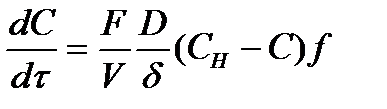 (8.17)
(8.17)
где С — концентрация углерода в расплаве; т — время науглероживания; F — площадь поверхности контакта расплава с наугле- роживателем; V— объем науглероживаемого металла; D — коэффициент диффузии углерода, зависящий от химического состава и температуры расплава; 8 — толщина ламинарного диффузионного слоя, зависящая от кинематической вязкости расплава и скорости его движения по поверхности науглероживателя; / — коэффициент качества науглероживателя (его значения равны: для графита электродного — 0,95; для кокса — 0,32; для антрацита — 0,29); Сн — концентрация насыщенного раствора углерода в расплаве.
Численное значение Сн зависит от температуры расплава и от его химического состава и определяется эмпирической формулой
Сн = 1,30 + 2,57 • I0~3t-0,31Si - 0,37Р - 0,22S - 0,1 lCu +
+ 0,03Mn + 0,075Cr + 0,15Ti +0,1V. (8.18)
Два первых слагаемых уравнения (8.18) характеризуют растворимость углерода в чистом железе при температуре °С, а последующие — влияние легирующих элементов. Из формулы следует, что при температуре 1550 °С в расплаве чистого железа может раствориться 5,28 % С. Введение в расплав 1 % Si приводит к уменьшению Сн до 5,28 - 0,31 = 4,97 %.
Результаты исследований кинетики растворения углерода в расплаве железа позволяют оптимизировать режимы науглероживания при плавке чугуна в разных печах.
Взаимодействие футеровки с расплавами шлакаи металла
Многообразные процессы взаимодействия расплавов металла и шлака с футеровкой можно подразделить на пять видов, описываемых соответствующими типовыми реакциями.
1. Переход оксидов из футеровки в шлак в результате оплавления футеровки[6]:
. (Me О)(Me О).
2. Оплавление футеровки в результате химического взаимодействия оксидов футеровки с оксидами шлака и образования легкоплавкой соли. Ярче всего это взаимодействие проявляется между кислой футеровкой и основным шлаком:
(Me О) + (Ме'О) -> (Me О • Ме'О).
3. Взаимодействие оксидов легирующих элементов с оксидами шлака и футеровки (эти взаимодействия рассмотрены в подразд. 8.4. «Закономерности угара элементов в кислых и основных печах»):
[Me О] + (Ме'О) -> (Me О • Ме'О),
[Me О] + (Ме'О) -> (Me О • Ме'О).
4. Восстановление оксида футеровки основным металлом расплава. Примером этого взаимодействия является реакция восстановления кремнезема кислой футеровки при плавке алюминиевых сплавов:
3<Si02> + 4[А1] = 2(А1203) + 3[Si]
или в общем виде восстановление оксида футеровки легирующим элементом расплава
(Me О) +[Меи] = (Меп О) + [Ме].
Примером такого взаимодействия является так называемая тигельная реакция.
В процессе плавки железоуглеродистых сплавов в печах с кислой футеровкой нередко наблюдается увеличение содержания кремния в расплаве — пригар кремния.
Этот пригар является результатом взаимодействия углерода, содержащегося в чугунах и сталях, с кремнеземом кислой футеровки и кислого шлака. Взаимодействие описывается тигельной реакцией:
<Si02> + 2[С] = [Si] + 2{СО}Т - Q,
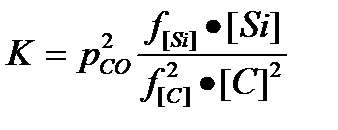
Движущей силой этой эндотермической реакции (-Q) является только энтропийный фактор (об увеличении энтропии в результате реакции свидетельствует увеличение количества газов на 2 моль).
Из этого следует, что реакция может протекать только при высоких температурах, способствующих возрастанию восстанавливающей способности углерода.
Другим важнейшим условием ее протекания является раскис- ленностъ металла. В нераскисленном металле углерод будет восстанавливать железо из FeO.
Анализ уравнения тигельной реакции с позиций закона действующих масс показывает, что полноте ее протекания способствуют: 1) высокая концентрация углерода в расплаве; 2) низкая концентрация кремния в нем; 3) низкое парциальное давление СО над зеркалом металла.
Протекание тигельной реакции приводит к разрушению футеровки, поэтому в большинстве случаев в ходе плавки следует по возможности учитывать приведенные выше соображения для уменьшения разгара футеровки.
ИСХОДНЫЕ МАТЕРИАЛЫ ДЛЯ ПЛАВКИ ЛИТЕЙНЫХ СПЛАВОВ
Первичные металлические материалы
Все многообразие компонентов шихты, используемых при плавке литейных сплавов, можно подразделить на первичные и вторичные металлы, флюсы и твердое топливо.
Первичные металлы получают из рудных материалов на металлургических заводах. В литейные цехи они поступают, как правило, в виде чушек или дробленых кусков.
Чушковые чугуны. В настоящее время в литейных цехах используются литейные и передельные доменные чугуны.
Чугуны литейные (ГОСТ 4832—80) подразделяют на шесть марок по содержанию кремния. Наибольшее количество кремния содержится в чугуне марки JI1 (3,2...3,6 % Si включительно), наименьшее — в чугуне марки JI6(1,2... 1,6 % Si).
В чугуне каждой из шести марок содержание марганца может быть разным в зависимости от группы, обозначаемой римскими цифрами от I до IV. Наибольшее количество марганца содержится в чугуне группы IV (от 0,9 до 1,5%), наименьшее — в чугуне группы I (до 0,5 %).
В чугуне каждой марки и группы содержание фосфора может соответствовать одному из пяти классов, обозначаемых буквами А, Б, В, Г и Д. В группах А, Б и В ограничивается максимальное содержание фосфора — до 0,08; 0,12 и 0,3 % соответственно. В чугуне группы Г допускается свыше 0,3 до 0,7 % Р включительно и в чугуне группы Д — свыше 0,7 до 1,2 % Р включительно.
Наконец по содержанию серы литейные чугуны делятся на четыре категории, обозначаемые арабскими цифрами 1, 2, 3 и 4. Самый чистый от серы чугун категории 1 содержит не более 0,02 % S, а в чугунах категории 4 ее содержание достигает 0,05 %.
В документе о качестве чугуна, прилагаемом к каждой поставляемой партии, указывается действительное содержание элементов, которое должно укладываться в допуски ГОСТ 4832—80.
Например, маркировка ЛЗ-Н-Б-2 означает:
• чугун литейный марки 3 с содержанием ) | кремния от 2,2 до 2,8 %; " J
• группа II — содержание марганца 0,3 ...0,5 %;
• класс Б — содержание фосфора до 0,12 %;
• категория 2 — содержание серы до 0,01 %.
Содержание углерода в литейных чугунах не оговаривается ГОСТом, однако чугуны всех марок должны поставляться с указанием его содержания в мае. %.
Это объясняется чрезвычайно высокой интенсивностью процесса науглероживания металла в доменной печи, который не поддается регулированию и зависит от химического состава и температуры чугуна. Достаточно отметить, что в течение времени между выпусками чугуна, которое составляет от 1,5 до 3 ч, чугун в горне домны накапливается между кусками кокса. В результате этого содержание углерода в чугуне практически достигает концентрации насыщенного раствора (Сн). Эта величина определяется эмпирической формулой (8.18), согласно которой с увеличением содержания кремния в чугуне растворимость углерода в нем снижается. В табл. 9.1 приведено соотношение содержаний углерода и кремния в чугуне марок JI1 и JI6, которое хорошо согласуется с формулой (8.18). Однако по требованию заказчика чугун изготавливают с нормированным содержанием углерода — от 3,4... 3,9 мае. % С в чугуне марки JI1 оно увеличивается до 3,9...4,4 мае. % С в чугуне марки JI6.
По ГОСТ 4832—80 предусмотрены семь марок литейного чугуна, рафинированного магнием. Главное отличие этих чугунов состоит в пониженном содержании серы (0,005...0,01 %). Марка рафинированного чугуна начинается с букв «ЛР».
Таблица 9.1 Соотношение содержаний С и Si в литейных чугунах \
|
Передельно-литейные чугуны (ГОСТ 805—80) выпускаются марок ПЛ1 и ПЛ2. Как и литейные, передельно-литейные чугуны делятся на группы по марганцу, классы по фосфору и категории по сере. Передельно-литейные чугуны содержат меньше кремния, чем литейные чугуны, поэтому они дешевле литейных чушковых чугунов, но для их получения требуются добавки в шихту большего количества кремния в виде ферросилиция.
Для выплавки чугуна и стали в литейном производстве используются также передельные высококачественные чугуны марок ПВК1, ПВК2 и ПВКЗ, отличающиеся пониженным содержанием фосфора и серы.
Для производства прокатных валков согласно ОСТ 1465—80 предусмотрены две марки специального валкового чугуна — ЧВ1 и ЧВ2.
Природнолегирован- ные чугуны получили свое название потому, что руды некоторых месторождений железа содержат оксиды хрома, меди и Других металлов. В процессе доменной плавки на таких рудах оксиды металлов частично восстанавливаются и легируют выплавленный чугун. Содержание легирующих элементов в природнолегированных чугунах невелико (0,3...3%), поэтому присадка их в шихту позволяет получать низколегированные конструкционные чугуны при минимальном угаре легирующих элементов. Это особенно важно при плавке в печах с окислительной атмосферой.
Наибольшее распространение получили три вида природнолегированных чугунов: хромоникелевые марок JIXH1 ...ЛХНЮ (0,4...3,2% Сг и 0,4... 1,0% Ni); титановые марок БТЛЗ... BTJI7 (0,3% Ti) и титаномедистые марок BTMJI3...BTMJI7 (0,3... 1,2% Ti и 2,0...3,0% Си).
Ферросплавы. Сплавы железа с одним или несколькими легирующими элементами называют «ферросплавами», при этом содержание легирующих элементов в сплавах этого класса часто превышает содержание самого железа. Первая буква во всех марках ферросплавов — «Ф», за ней следуют буквы, соответствующие легирующему элементу.
Ферросилиций (ГОСТ 1415—78). В марке указывается среднее содержание кремния в процентах (например, ФС20, ФС75). Для легирования чугунов и сталей используется ферросилиций марок ФС20...ФС45, в качестве раскислителей — ФС45...ФС75, в качестве модификаторов — ФС75...ФС90.
Ферромарганец (ГОСТ4755—80). В низко- и среднеуглеро- дистых ферромарганцах после букв Мн указывается содержание углерода в сплаве в процентах (например, ФМн2), а содержание марганца в них по умолчанию — 85... 75 %. В ферромарганце высокоуглеродистых марок — ФМн75... ФМн78 указывается содержание марганца в процентах (содержание углерода в них около 7 %). В ферромарганце обычных марок содержится повышенное количество фосфора (0,3...0,55 %). Буква «А» в конце марки означает пониженное (до 0,05...0,1 %) содержание фосфора, буква «К» — пониженное содержание кремния, «С» — повышенное содержание кремния.
При выплавке низкоуглеродистых сталей с пониженным содержанием фосфора используется металлический марганец (ГОСТ 6008—82), марки которого начинаются с букв «Мр». Содержание углерода в металлическом марганце 0,02...0,2%, а фосфора — 0,005...0,07 %.
Силикомарганец (ГОСТ 4756—77). В марке указывается минимальное содержание кремния в процентах — СМн10...СМн2б. Содержание марганца в силикомарганце всех марок не менее 60...65 %.
Силикокальций (ГОСТ 4762—71). В марке указывается минимальное содержание кальция в процентах — СК10... СК30. Суммарное содержание кремния и кальция в силикокальции всех марок 75... 95 % соответственно.
Феррохром (ГОСТ 4757—79). Так же как и ферромарганец, различают низко-, средне- и высокоуглеродистый феррохром с содержанием углерода соответственно до 0,5; 4 и 8 %. Содержание углерода указывается в марке в сотых долях процента (например, в феррохроме ФХ050 содержится 0,50 % С). В маркировке азотированного феррохрома содержание азота указывается в сотых долях процента после буквы Н (например, в феррохроме ФХН200 — 2 % N). Содержание хрома во всех марках составляет 6068 %.
Ферросиликохром (ГОСТ 11861—77). В марке указывается среднее содержание кремния в процентах (ФСХЗЗ содержит 30...37 % Si). Содержание хрома — от 28 до 55 %.
Ферротитан (ГОСТ 4761—80). В марке указывается содержание титана в процентах (ФТи20А, ФТи68). Буквы А или Б в конце марки указывают на разное содержание фосфора.
Ферровольфрам (ГОСТ 17293—82) содержит не менее 65 % W. Пример обозначения — ФВ80.
Ферромолибден (ГОСТ 4759—79) содержит молибден в количестве, указанном в конце марки в процентах ФМобО.
Феррофосфор (ТУ 14-5-72-80) помимо железа содержит фосфор в количестве, указанном после букв (в процентах). Например, феррофосфор ФФ14.
Феррованадий (ТУ 14-5-98-78) содержит 85 % V в металле марок Вд35А, Вд35Б и Вд350.
Ферробор (ГОСТ 14848—69) содержит 6...20% В, что отражено в написании марок ФБ6...ФБ20.
Металлы цветные первичные. Поставляются в литейные цехи в виде чушек, слитков, гранул. Их маркируют в зависимости от степени чистоты.
Алюминий первичный по ГОСТ 11069—74 имеет три вида чистоты: особой чистоты с содержанием алюминия 99,999 % А1 (обозначается А999), высокой чистоты — 99,995...99,95% А1 (А99...А95) и технической чистоты — 99,85...99,0 % А1 (А85...А0).
В чушках первичной плавки поставляется силумин, содержащий 10 ... 13 % Si. Цифры в марке силумина показывают степень загрязненности сплава. Если наиболее чистым является СИЛ-00, то силумин СИЛ-2 содержит около 2 % примесей Fe, Мп, Cu, Zn и Са в сумме.
Медь в зависимости от чистоты и способа изготовления маркируют по ГОСТ 859—78: М006 (99,99 % Си) — наиболее чистая бескислородная медь; М1р, М2р, М1ф (до 99,9% Си) и медь огневого рафинирования М2 и МЗ (до 99,7 % Си).
Магний первичный в чушках по ГОСТ 804—72 маркируется в зависимости от содержания магния: Мг96, Мг95, Мг90 (соответственно 99,96; 99,95 и 99,90% Mg).
Также в зависимости от чистоты маркируются цинк (ГОСТ 3640-79) - от ЦВ00 до ЦЗ (99,997...97,5 % Zn); олово (ГОСТ 860—75) от ОВЧ-ООО до 04 (99,999...96,43 % Sn); свинец (ГОСТ 3778-77) -от СО до СЗС (99,992. ..99,5 % Pb); никель (ГОСТ 849-70) - от НО до Н4 (99,99...97,6 % Ni); хром (ГОСТ 5905- 79) - от Х99А до Х97 (99...97 % Сг).
Титан (ГОСТ 17746—79) маркируется по твердости от ТГ-90 до ТГ-150.
Сплавы цветные в чушках маркируются следующим образом: первая буква марки сплава обозначает его основной металл: А — сплавы на основе алюминия (ГОСТ 1586—73); М — сплавы магния (ГОСТ 2581—78); Ц — сплавы цинка (ГОСТ 19424- 74); последующие буквы в марке обозначают легирующие элементы сплава. Содержание этих элементов в процентах указывается в той же последовательности, что и буквенные обозначения.
Бронзы в чушках (оловянистые ГОСТ 614—73 и безоло- вянистые ГОСТ 17328—78), а также латуни литейные в чушках маркируются аналогично соответствующим сплавам в отливках.
9.2. Вторичные металлические материалы
Вторичные черные металлы, используемые в качестве металлической шихты в плавильных агрегатах литейных цехов (ГОСТ 2787—86).
Различают две категории вторичных черных металлов: А — углеродистые и Б — легированные. В зависимости от физического состояния и показателей качества, различают 21вид кусковых (габаритных и негабаритных), прессованных (брикетированных и пакетированных) ломов, отходов и стружки (табл. 9.2).
Таблица 9.2 Вторичные черные металлы
|
| Категория | Вид | Номер вида | Общее обозначение | Плавильный агрегат* |
| А, Б | Стальные канаты и проволока | 12 А, 12Б | МП | |
| А | Стальная стружка № 1 | 13А | ДСП, ИСТ, ИЧТ | |
| А, Б | Стальная стружка № 2 | 13А, 4Б | МП | |
| Чугунный лом и отходы | ||||
| А, Б | Чугунный лом и отходы № 1 | 16 А, 16Б | ИЧТ, в | |
| А | Чугунный лом и отходы № 2 | 17А | ИЧТ, в | |
| А | Брикеты из чугунной стружки | 20А | в | |
| А, Б | Чугунная стружка | 21А, 21Б | МП, ДСП, ИЧТ |
* Условные обозначения плавильных печей: ДСП — дуговая сталеплавильная печь; ИСТ — индукционная сталеплавильная тигельная печь; В — вагранка, МП — мартеновская печь; ИЧТ — индукционная чугуноплавильная печь промышленной частоты
Таблица 9.3 Физические характеристики* важнейших шихтовых материалов
|
