Зависимость скорости ферментативной реакции от рН
Скорость ферментативных реакций значительно зависит от кислотности среды, в которой они протекают. Для каждого фермента имеется определенное значение рН, при котором наблюдается наибольшая скорость реакции — рН-оптимум.При отклонении в любую сторону от этого значения рН резко уменьшается ферментативная активность. Важно подчеркнуть, что величина рН-оптимума у разных ферментов колеблется в большом диапазоне значений рН, в то время как температурный оптимум для большинства ферментов составляет 37-40 °С. В качестве примера можно привести значения рН-оптимума следующих ферментов (рис. 5):
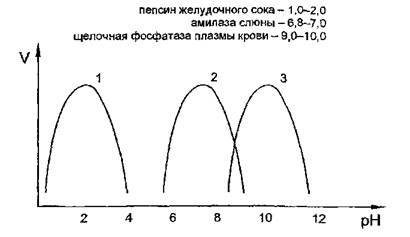
Рис. 5. Зависимость скорости ферментативной реакции от рН
(1 - пепсин, 2 - амилаза, 3 - щелочная фосфатаза)
Влияние кислотности среды на скорость ферментативных реакций обусловлено тем, что при изменении кислотности меняется конформация всей белковой молекулы фермента, в том числе изменяется конформация активного центра и его способность осуществлять катализ. При рН-оптимуме фермент находится в оптимальной для проявления каталитических свойств конформации. При небольшом отклонении величины кислотности от рН-оптимума наблюдается незначительное изменение конформации, носящее обратимый характер. При значительном отклонении от рН-оптимума (в сильнокислой и сильнощелочной среде)происходит необратимая денатурация ферментного белка, приводящая к полной утрате каталитической активности.
При работе с ферментами в лабораторных условиях в реакционную среду вводят буферные растворы, рН которых соответствует рН-оптимуму изучаемых ферментов.
Ингибиторы ферментов
Скорость ферментативной реакции существенно зависит от присутствия ингибиторов и активаторов.
Ингибиторы(I) – это химические соединения (обычно низкомолекулярные), которые, находясь в низких концентрациях, избирательно тормозят определенные ферментативные реакции. При этом ингибитор всегда присоединяется к ферменту с образованием фермент-ингибиторного комплекса. Фермент, связанный с ингибитором, теряет свою каталитическую активность.
Если связи между ферментом и ингибитором прочные, то действие ингибитора носит необратимый характер, и торможение нарастает во времени вплоть до полного прекращения ферментативной реакции:
 Е + I EI
Е + I EI
Такие ингибиторы называются необратимыми. Примером необратимых ингибиторов являются фосфорорганические соединения (табун, зарин, дихлофос, карбофос и др.), избирательно и необратимо угнетающие важнейший фермент организма холинэстеразу, участвующую в передаче нервных импульсов.
Если ингибитор присоединяется к ферменту за счет непрочных связей, то торможение фермента является обратимым и не зависит от времени:

 Е + I EI
Е + I EI
Ингибиторы такого типа называются обратимыми.
В свою очередь, обратимые ингибиторы делятся на две разновидности: конкурентные и неконкурентные.
Конкурентные ингибиторыприсоединяются к активному центру фермента, т.е. к тому же участку поверхности фермента, что и субстрат. Поэтому между ингибитором и субстратом идет конкуренция за присоединение к активному центру. Занимая активный центр, ингибитор тем самым препятствует образованию фермент-субстратного комплекса – первой стадии ферментативного катализа. Конкурентные ингибиторы обычно по строению похожи на субстрат.
Неконкурентные ингибиторыприсоединяются к ферменту вне активного центра. Этот участок поверхности фермента называется аллостерический центр(т.е. находящийся в другом месте по сравнению с активным центром).
Присоединение неконкурентного ингибитора к аллостерическому центру вызывает неблагоприятное изменение пространственной структуры (конформации) всей молекулы фермента, в том числе и активного центра. В результате каталитические свойства фермента снижаются.
Неконкурентные ингибиторы участвуют в регуляции скорости ферментативных реакций, протекающих в организме. В роли неконкурентных ингибиторов могут быть гормоны, конечные и промежуточные продукты ферментативных реакций, ионы металлов, лекарственные вещества.
Активаторы ферментов
Активаторы– вещества, избирательно повышающие скорость определенных ферментативных реакций. Активаторы, подобно неконкурентным ингибиторам, присоединяются обратимо к аллостерическому центру фермента. Но в этом случае изменение конформации фермента будет благоприятным для функционирования активного центра, что приводит в итоге к повышению скорости ферментативной реакции. В организме активаторами являются некоторые гормоны, промежуточные продукты метаболических процессов, ионы металлов, а также лекарственные препараты.
РЕГУЛЯЦИЯ СКОРОСТИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ
Особенностью ферментативных реакций является наличие механизмов регуляции их скорости. Благодаря регуляторным механизмам ферментативные реакции протекают со скоростями, соответствующими потребностям организма. Например, при выполнении мышечной работы резко повышается скорость реакций окисления, сопровождающихся выделением энергии, и одновременным снижением скорости реакций синтеза, потребляющих энергию. Во время отдыха после работы наблюдается возрастание скорости реакций синтеза химических соединений, использованных при выполнении физических нагрузок.
К основным механизмам регуляции скорости ферментативных реакций можно отнести следующие:
• Изменение скорости синтеза ферментов.Ферменты, являясь белками, постепенно разрушаются, и поэтому в клетках постоянно синтезируются новые ферментные белки. При повышении скорости образования новых ферментов их содержание в клетках возрастает. При этом скорость ферментативных реакций увеличивается, так как зависимость скорости реакции от концентрации фермента носит прямолинейный характер.
При уменьшении выработки ферментов их концентрация в клетках постепенно снижается, что сопровождается падением скорости катализируемых ими реакций.
Изменение скорости синтеза ферментов обычно происходит под влиянием гормонов, которые ускоряют или замедляют первый этап синтеза ферментных белков – считывание генетической информации – транскрипцию. Поэтому данный механизм регуляции часто называется регуляцией на генетическом уровне.
• Модификация ферментов.Под модификацией понимается незначительное изменение химического состава молекулы фермента, приводящее к изменению каталитической активности.
Модификация может быть обратимой и необратимой.
В первом случае изменение строения фермента носит обратимый характер и фермент может многократно менять свою активность. Например, некоторые ферменты содержат в своей молекуле остаток фосфорной кислоты. При отщеплении фосфатного остатка у одних ферментов каталитическая активность снижается; при включении его снова в состав ферментов активность их возрастает. У других же ферментов фосфорилированная форма (содержащая фосфат), наоборот, малоактивна. Отщепление фосфорной кислоты от таких ферментов ведет к повышению их активности.
Примером необратимой модификации служит активация пищеварительных ферментов, действующих на пищевые белки. Так, в составе желудочного сока содержится белок пепсиноген, не обладающий каталитической активностью. В полости желудка под действием соляной кислоты от этого белка отщепляется небольшой полипептид и образуется очень активный фермент, расщепляющий в пищевых белках пептидные связи, – пепсин. (Белки, являющиеся предшественниками ферментов, называются проферментами.)
• Изменение конформации ферментов.Изменение конформации, т.е. пространственного строения ферментного белка, происходит под действием неконкурентных ингибиторов и активаторов, которыми могут быть гормоны, промежуточные и конечные продукты ферментативных реакций, ионы металлов, лекарства (см. выше). Изменение конформации ферментов возможно и при изменении условий среды, например при повышении или снижении кислотности.
КЛАССИФИКАЦИЯ И ИНДЕКСАЦИЯ ФЕРМЕНТОВ
Современная классификация ферментов основывается на характере химической реакции, катализируемой ферментом. Все ферменты делятся на шесть классов в зависимости от типа катализируемой реакции:
I класс — оксидоредуктазы — ферменты, катализирующие окислительно-восстановительные реакции.
Схематично действие ферментов I класса можно записать:
 А+В C + D
А+В C + D
II класс – трансферазы – ферменты, катализирующие перенос химических группировок с молекулы одного вещества на молекулу другого:
 АВ + С А + ВС
АВ + С А + ВС
III класс – гидролазы – ферменты, расщепляющие химические связи путем присоединения воды, т.е. путем гидролиза:
 АВ + Н2О А – Н + В – ОН
АВ + Н2О А – Н + В – ОН
IV класс – лиазы – ферменты, катализирующие расщепление химических связей без присоединения воды:
 АВ А+В
АВ А+В
V класс – изомеразы – ферменты, катализирующие изомерные превращения, т.е. перенос отдельных химических групп в пределах одной молекулы:
 А В
А В
VI класс – сиитетазы – ферменты, катализирующие реакции синтеза, протекающие за счет энергии гидролиза АТФ:
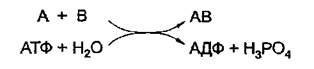
Каждый класс, в свою очередь, делится на подклассы, внутри подклассов выделены подподклассы. Каждый подподкласс содержит список индивидуальных ферментов в строго определенной последовательности, которая не изменяется, а лишь продлевается по мере открытия новых ферментов.
В основе подразделения ферментов на подклассы и на подподклассы лежит тип химической связи или химическое строение группировки субстрата, на которую действует фермент.
С классификацией ферментов тесно связана их индексация (нумерация). Индекс (шифр) каждого фермента состоит из четырех чисел, разделенных точками, и составляется по следующему принципу: первая цифра индекса указывает, к какому из шести классов принадлежит данный фермент. Второе и третье числа индекса обозначают соответственно порядковые номера подклассов и подподклассов. Четвертое число индекса – порядковый номер индивидуального фермента внутри своего подподкласса.
Например, фермент слюны амилаза, расщепляющий крахмал, имеет индекс 3.2.1.1, что свидетельствует о принадлежности этого фермента к классу гидролаз.
НОМЕНКЛАТУРА ФЕРМЕНТОВ
Название фермента, как правило, состоит из двух частей. Первая часть является названием субстрата, превращения которого катализируется данным ферментом. Вторая часть названия, имеющая окончание «-аза», указывает природу реакции. Например, фермент, отщепляющий от лактата (молочная кислота) атомы водорода, называется лактатдегидрогеназа; фермент, катализирующий изомеризацию глюкозо-6-фосфата в фруктозо-6-фосфат, имеет название глюкозофосфатизомераза, а фермент, участвующий в синтезе гликогена, – гликогенсинтетаза.
* 1 ккал = 4,18 кДж.
