Расчет плавки стали в кислородном конвертере
1. ТЕОРЕТИЧЕСКИЕ СВЕДЕНИЯ
Целью плавки является получение заданной массы жидкой стали с требуемым химическим составом и температурой при минимальных затратах материально-сырьевых, топливно-энергетических и трудовых ресурсов.
Все физико-химические процессы, связанные с получением заданного содержания примесей в готовой жидкой стали делятся на две группы:
-рафинирование металла – удаление избыточного количества примесей, содержащихся в исходном металле;
-раскисление-легирование металла – достижение необходимого содержания кислорода и полезных примесей, которые вводятся в металл в виде ферросплавов.
Оба процесса проводят, как правило, последовательно. Рафинирование металла, которое является более сложной задачей, обычно проводят в несколько стадий.
Стадии рафинирования металла:
Предварительное рафинирование - сводится к удалению из чугуна серы, фосфора и других примесей. Проводят его до подачи чугуна в сталеплавильный агрегат, как правило, в чугуновозных ковшах, сводится, главным образом, к обработке чугуна кальцинированной и каустической содой, магнием и жидкими синтетическими шлаками с целью его десульфурации.
Основное рафинирование - проводится в сталеплавильном агрегате за счет окисления примесей кислородом дутья, газовой фазы и твердых окислителей (обезуглероживание, дефосфоризация и десульфурация и др.).
Дополнительное рафинирование - проводят обычно сталеразливочном ковше путем обработки металла синтетическим шлаком и применяется, в основном, для удаления серы.
Дегазация металла с целью удаления водорода, кислорода и азота. Её проводят методом вакуумной обработки или продувки нейтральным газом в сталеразливочном ковше.
Процесс обезуглероживания металла регулируется изменением расхода кислорода, поступающего в ванну. При этом характерно, что реакция окисления углерода может быть как явно экзотермической, если она протекает за счет газообразного кислорода, так и резко эндотермической, если она протекает за счет кислорода твердых окислителей.
Процессы дефосфоризации и десульфурации осуществляются регулированием шлакового режима плавки, т.е. изменением химического состава и количества шлака.
Химический состав и количество шлака зависят, в основном, от количества кремния в чугуне и от расхода шлакообразующих материалов. Поэтому расчеты, связанные с управлением шлаковым режимом (десульфурация и дефосфоризация) сводятся к определению количества шлака и соответственного расхода флюсов.
Раскисление-легирование металла является обязательным и заключительным этапом плавки, обеспечивающим получение заданного содержания примесей в готовой стали. Поэтому этот этап является весьма ответственным, поскольку определяет качество литого и готового металла.
Порядок расчета плавки
Проведение расчетов производится в два приема – предварительный и окончательный.
Предварительный расчет выполняется с целью установления технологической схемы плавки – процесс может быть одношлаковый или многошлаковый.
Окончательный расчет выполняется для установления оптимального режима (расход исходных материалов и энергоресурсов, определение выхода и состава плавки).
Определение любого параметра плавки производится по формуле, полученной из уравнения материального и теплового балансов, путем определения их относительного искомого параметра.
Определение основных параметров плавки производится на 100 кг чугуна и стали. Расход материалов и выход продуктов плавки в основных расчетах выражается на 100 кг металлошихты (в процентах от массы металлошихты), что создает удобство при экономической оценке процесса плавки и практическом управлении плавкой.
Обеспечение оптимального шлакового режима начинается с установления оптимальных значений его параметров, которыми являются, в первую очередь, – основность и количество шлака, а также режим взаимодействия шлака и металла.
Основность шлака позволяет оценивать фосфоро- и серопоглотительную способность шлака. Универсальной формой выражения основности (B) шлака является отношение концентрации основных оксидов к концентрации кислотных и амфотерных оксидов:
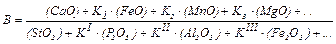 ,
,
где - 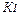 ,
, 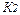 ,
, 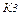 – коэффициенты, учитывающие эквивалентность FeO, MnO, MgO по сравнению с CaO;
– коэффициенты, учитывающие эквивалентность FeO, MnO, MgO по сравнению с CaO; 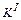 ,
, 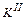 ,
, 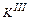 – коэффициенты, учитывающие эквивалентность P2O5, Al2O3, Fe2O3 по сравнению с SiO2.
– коэффициенты, учитывающие эквивалентность P2O5, Al2O3, Fe2O3 по сравнению с SiO2.
В связи с неизученностью указанных коэффициентов, основность шлака определяют обычно упрощенно:
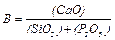 ,
,
т.е. учитывают только самый сильный основной оксид (CaO), оказывающий решающее влияние на химические свойства шлака, и два главных кислотных (SiO2, P2O5) оксида, массовое содержание которых выражают в процентах.
2. ЗАДАНИЕ
Выполнить расчет плавки заданной марки стали в кислородном конвертере заданной ёмкости для разливки на МНЛЗ. Исходные данные принять согласно варианта из таблиц А.1 и А.2 приложения А.
Вместимость конвертора _________________ т;
Химический состав чугуна и лома – табл. 1;
Температура жидкого чугуна ______________°С;
Химический состав стали - _таблица 1;
Интенсивность продувки ванны __________нм3/(т·мин);
Химический состав металлической и неметаллической частей шихты и готовой стали сводим в таблицу 1 и 2.
Таблица 1
Химический состав металлической части шихты и стали
| Материалы | C | Si | Mn | P | S | Fe |
| Чугун жидкий | ||||||
| Металлический лом1 | ||||||
| Ферромарганец | 6,00 | 1,00 | 78,00 | 0,300 | 0,020 | 14,68 |
| Готовая сталь |
1) – Средний химический состав лома выбираем из интервала значений, %: С=0,2-0,5; Si=0,2-0,4; Mn=0,1-0,5; S=0,030-0,045; P=0,030-0,050.
Таблица 2
Химический состав неметаллической шихты и других материалов, %
| Материал | SiO2 | Al2O3 | MnO | CaO | MgO | P2O5 | S | CaF2 | ∑ΔMпрм | Fe2O3 | FeO | H2O | CO2 |
| Известь | 2,0 | 0,8 | - | 85,0 | 2,0 | 0,1 | 0,1 | - | 90,0 | - | - | 1,0 | 9,0 |
| Плавиковый шпат | 4,5 | 0,9 | - | 7,6 | - | - | - | 81,0 | 94,0 | - | - | - | 2,0 |
| Футеровка | 3,4 | 1,4 | - | 40,3 | 52,8 | - | - | - | 97,9 | 2,1 | - | - | - |
| Загрязнения лома | 68,0 | 24,0 | - | 3,0 | 2,0 | - | - | - | 97,0 | 3,0 | - | - | - |
| Окалина лома | - | - | - | - | - | - | - | - | - | 69,0 | 31,0 | - | - |
| Ковшевой шлак | 47,5 | 6,5 | 8,0 | 16,6 | 4,5 | 0,2 | 0,4 | - | 83,7 | - | 16,3 | - | - |
Для удобства основную часть результатов теоретических расчетов плавки стали (расход материалов и тепла, выход продуктов плавки) целесообразно выражать в килограммах и килоджоулях на 100 кг металлошихты (чугун + лом).
Материалы из малозначащих источников, участвующие в плавке
Такими источниками поступления материалов являются: футеровка конвертера; миксерный и доменный шлак; оксиды железа, кремния и алюминия, попадающие с металлоломом. К этой категории материалов, участвующих в плавке, относят также боксит и плавиковый шпат.
Поскольку все указанные выше материалы поступают из малозначащих источников, их точный качественный учет невозможен. Но их влияние на процесс шлакообразования не вызывает сомнений и поэтому соответствующие данные для таких материалов обычно принимают на основе среднестатистических данных теории и практики плавки.
Принято считать, что количество засорений (мусора) в металлическом ломе составляет 1…3 %, в основном это SiO2=75 % и Al2O3=25 %.
Количество окалины (ржавчины) в металлоломе составляет обычно 1…4 %, главным образом это Fe2O3 – 69 % и FeO – 31 %.
С учетом того, что расход металлического лома в кислородно-конвертерном процессе составляет обычно 20…30 %, можно считать, что количество засорений из металлического лома будет составлять 0,25…0,75 %.
Расход футеровки конвертера принято считать равным 0,7…1,2 кг, боксита – 0,6…1 кг, миксерного шлака – 0,5…1,2 кг.
Таким образом, расход материалов из малозначащих источников, участвующих в образовании шлака, для расчета плавки можно принять:
Футеровка конвертера – 1,0 кг;
Миксерный шлак – 0,8 кг;
Боксит – 0,8 кг;
Засорение лома – 0,4 кг.
6. Порядок расчета
6.1. Определение температуры металла в конце продувки
Требуемую температуру металла в конце продувочной операции находим последовательным расчётом.
Температура плавления (ликвидуса) стали:
tликв = 1539 – 88%С – 16%Si – 3,4%Mn – 1,9%Ni – 1,3%Co – 2,4%Mo – 8,7%Nb – 2,1%V – 1,6%Cr;
или
tликв = 1539 – 88%С – 8%Si – 5%Mn – 4%Ni – 5%Cu – 2%V – 1,5%Cr – 25%Ti – 30%P.
Выбор расчётной формулы производим из условия учёта влияния максимального числа компонентов.
Температура стали в кристаллизаторе:
tкр = tликв + (10÷150C);
Определяем температуру металла в промковше:
tпр.к = tкр + (15÷200C);
Температура металла в стальковше:
tcт.к = tпр.к + (10÷200C);
Необходимая температура металла перед внепечной обработкой:
tвнеп = tcт.к + (10÷200C);
Определяем температуру металла в конверторе по окончании продувки:
tкмет = tвнеп + (30÷400C);
6.2. Расчет материального баланса плавки
Расчет ведется на 100 кг металлошихты (чугун + лом).
Предварительное определение расхода лома
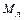 = [(3000
= [(3000 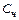 + 6430
+ 6430 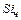 + 1680
+ 1680 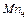 + 4720
+ 4720 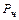 + 21
+ 21 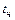 + 4200)– (25,2
+ 4200)– (25,2 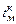 + +2730
+ +2730 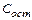 )]/(30
)]/(30 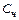 + 64,3
+ 64,3 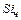 + 16,8
+ 16,8 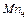 + 47,2
+ 47,2 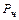 + 0,21
+ 0,21 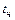 ), кг (1)
), кг (1)
где 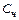 ,
, 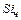 ,
, 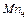 ,
, 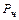 – содержание соответствующих элементов в чугуне, %;
– содержание соответствующих элементов в чугуне, %; 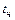 ,
, 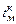 – соответственно температура заливаемого в конвертер чугуна и температура металла в конце продувки,
– соответственно температура заливаемого в конвертер чугуна и температура металла в конце продувки, 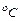 ;
; 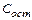 – содержание углерода в металле в конце продувки, % (принимаем равным нижнему пределу в готовой стали).
– содержание углерода в металле в конце продувки, % (принимаем равным нижнему пределу в готовой стали).
Расход чугуна, (кг) 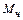 = 100 -
= 100 - 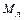 (2)
(2)
Расход миксерного шлака составляет 0,6 – 0,9 % от 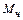 , кг
, кг
Принимаем 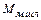 = (0,006 ÷ 0,009)Мч. (3)
= (0,006 ÷ 0,009)Мч. (3)
Для выполнения дальнейших расчетов принимаем:
Количество загрязнений, вносимых ломом, кг
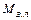 = 0,0065
= 0,0065 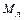 (4)
(4)
Расход плавикового шпата в зависимости от параметров технологии находится в пределах 0,6 – 1,0 кг.
Принимаем 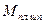 = (5)
= (5)
Расход футеровки составляет 0,7 – 1,2 кг.
Принимаем 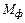 = (6)
= (6)
Количество окалины, внесенной ломом, кг (1-4 % от 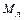 )
)
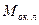 = (7)
= (7)
Количество примесей, внесенных металлошихтой, кг
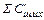 = 0,01(
= 0,01( 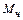 ∙
∙ 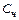 +
+ 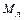 ∙
∙ 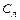 ) (8)
) (8)
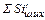 = 0,01(
= 0,01( 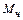 ∙
∙ 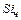 +
+ 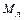 ∙
∙ 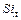 ) (9)
) (9)
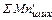 = 0,01(
= 0,01( 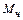 ∙
∙ 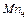 +
+ 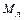 ∙
∙ 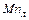 ) (10)
) (10)
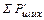 = 0,01(
= 0,01( 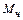 ∙
∙ 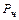 +
+ 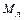 ∙
∙ 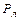 ) (11)
) (11)
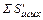 = 0,01(
= 0,01( 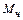 ∙
∙ 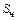 +
+ 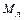 ∙
∙ 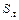 ) (12)
) (12)
где 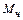 ,
, 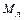 – соответственно масса чугуна и лома, кг;
– соответственно масса чугуна и лома, кг;
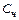 ,
, 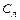 ,
, 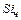 ,
, 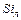 ,
, 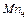 ,
, 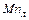 ,
, 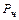 ,
, 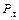 ,
, 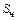 ,
, 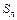 – содержание углерода, кремния, марганца, фосфора, серы соответственно в чугуне и ломе, %.
– содержание углерода, кремния, марганца, фосфора, серы соответственно в чугуне и ломе, %.
Расход извести на плавку ( 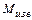 ), кг
), кг
Основность конечного шлака в зависимости от состава чугуна и марки выплавляемой стали (требуемых показателей дефосфорации и десульфурации) находится в пределах 3,0 – 3,6
Принимаем для расчета основность конечного шлака 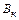 =
=
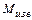 =
= 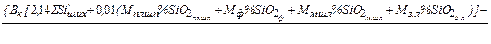
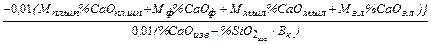 ,кг (13)
,кг (13)
где 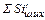 – содержание кремния в металлошихте;
– содержание кремния в металлошихте; 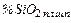 ,
, 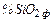 и т.д. – содержание кремнезёма в используемых материалах;
и т.д. – содержание кремнезёма в используемых материалах; 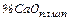 ,
, 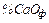 – содержание оксида кальция в используемых материалах (табл.2);
– содержание оксида кальция в используемых материалах (табл.2); 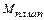 ,
, 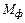 и т.д. – расход материалов.
и т.д. – расход материалов.
Содержание оксидов железа в конечном шлаке:
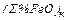 =
= 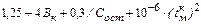 . (14)
. (14)
где 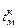 – температура металла в конце продувки,
– температура металла в конце продувки, 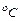 .
.
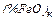 =
= 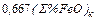 ;
; 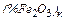 =
= 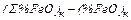 , (предполагаем, что
, (предполагаем, что 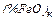 на 2/3 состоит из (%FeO)к и на 1/3 – из
на 2/3 состоит из (%FeO)к и на 1/3 – из 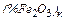 )
)
Ориентировочный выход жидкого металла в конце продувки ( 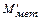 )
)
Принимаем, что за время продувки окисляется весь кремний, 80 % марганца, 90 % фосфора. Потери железа с отходящими газами, выбросами, со шлаком (в виде корольков) превышают количество железа, восстановленного из оксидов, окалины, загрязнений скрапа и других материалов на 3,5 – 4,5 %.
В расчете принимаем эти потери 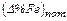 = %.
= %.
Тогда
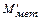 =
= 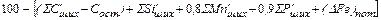 , кг (15)
, кг (15)
где 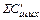 ,
, 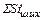 и т.д. – количество примесей, вносимых металлошихтой, кг;
и т.д. – количество примесей, вносимых металлошихтой, кг;
Ориентировочное количество шлака:
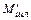 =
= 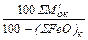 =
= 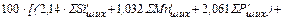
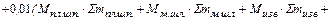
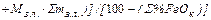 (16)
(16)
где 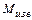 ,
, 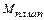 и т.д. – расход материалов;
и т.д. – расход материалов; 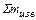 ,
, 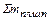 и т.д. – содержание оксидов в материалах.
и т.д. – содержание оксидов в материалах.
Уточнение количества примесей в металле в конце продувки:
Содержание углерода в металле должно соответствовать нижнему пределу его в готовой стали.
Содержание марганца определяем из балансового уравнения распределения марганца между шлаком и металлом:
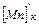 =
= 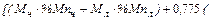
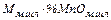 )]/
)]/
/ 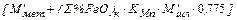 ,% (17)
,% (17)
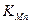 – константа равновесия реакции окисления марганца, определяемая из уравнения: lg
– константа равновесия реакции окисления марганца, определяемая из уравнения: lg 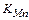 = lg
= lg 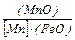 =
= 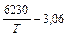 ,
, 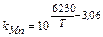
где Т = 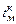 + 273, К.
+ 273, К.
Содержание фосфора:
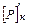 =
= 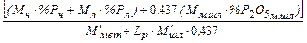 , (18)
, (18)
где 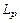 =
= 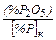 – коэффициент распределения фосфора между металлом и шлаком, определяемый из табл.3
– коэффициент распределения фосфора между металлом и шлаком, определяемый из табл.3
Таблица 3
Значения коэффициента распределения фосфора
| Основность шлака | Lp при содержании (% FeO)к | |||||
| 16 и более | ||||||
| 3,0 | ||||||
| 3,2 | ||||||
| 3,4 | ||||||
| 3,6 |
Содержание серы:
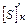 =
= 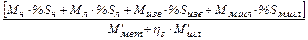 , (19)
, (19)
где 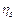 – коэффициент распределения серы металлом и шлаком, принимаемый по табл. 4.
– коэффициент распределения серы металлом и шлаком, принимаемый по табл. 4.
Таблица 4
Значения коэффициента распределения серы
| Основность Вк | 3,0 | 3,2 | 3,4 | 3,6 |
| Коэффициент ηs | 7,2 | 7,8 | 8,3 | 8,7 |
Содержание кремния в металле в конце продувки принимаем равным нулю 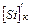 = 0.
= 0.
Уточненный химический состав металла в конце продувки, %:
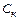 =
= 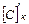 = ;
= ; 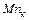 =
= 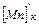 = ;
= ; 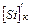 = 0;
= 0; 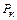 =
= 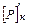 = ;
= ; 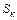 =
= 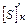 =;
=;
Остается примесей в металле, кг:
Углерода – 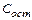 =
= 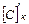 ∙
∙ 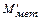 /100 (20)
/100 (20)
Кремния = 0;
Марганца – 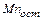 =
= 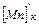 ∙
∙ 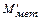 /100 (21)
/100 (21)
Фосфора – 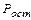 =
= 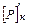 ∙
∙ 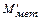 /100 (22)
/100 (22)
Серы – 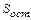 =
= 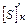 ∙
∙ 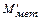 /100 (23)
/100 (23)
Удаляется примесей, кг:
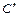 =
= 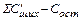 . (24)
. (24)
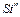 =
= 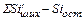 . (25)
. (25)
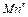 =
= 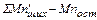 (26)
(26)
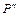 =
= 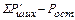 (27)
(27)
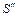 =
= 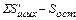 (28)
(28)
Всего окисляется примесей, кг:
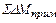 =
= 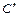 +
+ 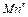 +
+ 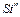 +
+ 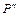 +
+ 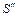 ; (29)
; (29)
Образуется оксидов, кг:
Принимаем, что 90 % углерода окисляется до СО и 10 % до 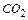 .
.
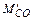 = 2,1∙
= 2,1∙ 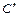 (30)
(30)
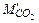 = 0,37∙
= 0,37∙ 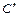 (31)
(31)
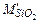 = 2,14∙
= 2,14∙ 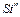 (32)
(32)
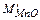 = 1,29∙
= 1,29∙ 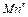 (33)
(33)
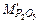 = 2,29∙
= 2,29∙ 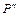 (34)
(34)
Количество шлакообразующих оксидов (кроме оксидов железа и соединений, внесенных металлошихтой и другими материалами), кг:
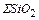 =
= 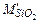 +
+ 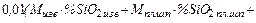
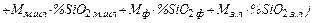 . (35)
. (35)
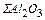 =
= 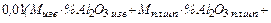
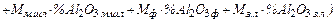 . (36)
. (36)
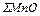 =
= 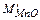 +
+ 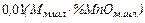 (37)
(37)
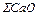 =
= 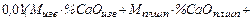
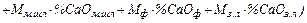 . (38)
. (38)
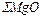 =
= 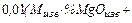
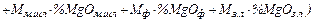 . (39)
. (39)
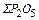 =
= 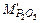 +
+ 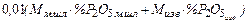 . (40)
. (40)
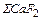 =
= 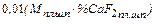 . (41)
. (41)
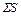 =
= 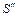 +
+ 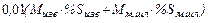 . (42)
. (42)
Общее количество шлакообразующих, оксидов и соединений (кроме оксидов железа), кг:
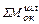 =
= 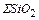 +
+ 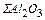 +
+ 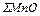 +
+ 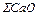 +
+ 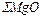 +
+ 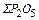 +
+ 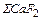 +
+ 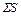 .(43)
.(43)
Уточненное количество конечного шлака, кг:
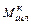 =
= 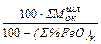 (44)
(44)
Таблица 5
Химический состав конечного шлака, %
| SiО2 | CaO | MgO | MnО | P2О5 | S | Fe2О3 | FeO | Al2O3 | CaF2 | Итого |
| (%Fe2O3) | (%FeO) | 100,0 |
(%CaO) = 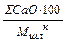
 и т. д.
и т. д.
Фактическая основность шлака по данным табл. 5
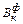 =
= 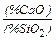 ; (45)
; (45)
Уточненный выход жидкого металла в конце продувки, кг
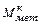 =
= 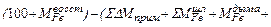
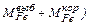 , (46)
, (46)
где 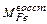 =
= 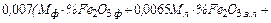 +
+ 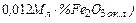
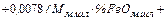
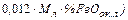 – количество железа, восстановленного из оксидов железа шихты;
– количество железа, восстановленного из оксидов железа шихты;
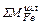 =
= 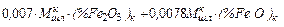 – количество железа, израсходованного на образование оксидов железа шлака;
– количество железа, израсходованного на образование оксидов железа шлака;
Принимаем:
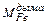 = 1,2кг – угар железа в дым;
= 1,2кг – угар железа в дым;
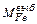 = 0,8кг – потери железа с выбросами;
= 0,8кг – потери железа с выбросами;
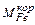 =
= 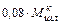 – потери железа в шлаке в виде корольков, кг;
– потери железа в шлаке в виде корольков, кг;
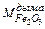 =
= 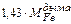 – количество оксидов железа в дыме, кг.
– количество оксидов железа в дыме, кг.
Расход кислорода, кг
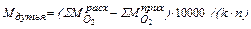 , (47)
, (47)
где k – степень усвоения кислорода ванной (принимаем 97 %); n – чистота кислорода (принимаем 99,5 %);
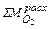 =
= 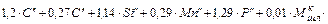
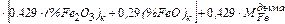 , кг (48)
, кг (48)
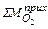 =
= 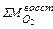 +
+ 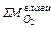 =
=
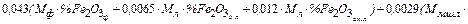
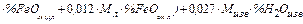 , кг (49)
, кг (49)
Мдутья =
Расход кислорода, нм3
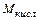 = Мдутья∙ 22,4/32 = 0,7 Мдутья .
= Мдутья∙ 22,4/32 = 0,7 Мдутья .
Определяем продолжительность продувки, мин
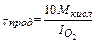 ,
,
где 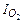 - интенсивность продувки, нм3/(т∙мин) - (задана).
- интенсивность продувки, нм3/(т∙мин) - (задана).
Количество и состав конвертерных газов:
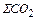 =
= 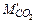 +
+ 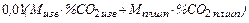 ; кг (50)
; кг (50)
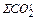 =
= 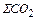 ∙22,4/44; нм3
∙22,4/44; нм3
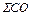 =
= 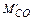 , кг (51)
, кг (51)
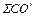 =
= 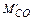 ∙22,4/28; нм3
∙22,4/28; нм3
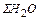 =
= 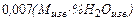 ; кг (52)
; кг (52)
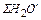 =
= 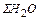 ∙22,4/18; нм3
∙22,4/18; нм3
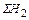 =
= 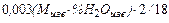 ; кг (53)
; кг (53)
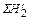 =
= 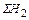 ∙22,4/2 ; нм3
∙22,4/2 ; нм3
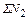 = 0,005∙
= 0,005∙ 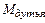 ; кг (54)
; кг (54)
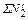 =
= 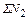 ∙22,4/28; нм3
∙22,4/28; нм3
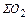 = 0,003∙
= 0,003∙ 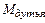 ; кг (55)
; кг (55)
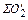 =
= 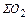 ∙22,4/32; нм3
∙22,4/32; нм3
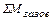 =
= 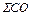 +
+ 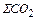 +
+ 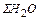 +
+ 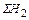 +
+ 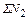 +
+ 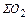 ., кг (56)
., кг (56)
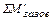 =
= 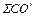 +
+ 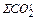 +
+ 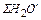 +
+ 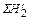 +
+ 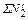 +
+ 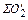 . нм3
. нм3
Таблица 6
Количество и состав газов
| Газ | кг | нм3 | % |
| CO2 CO H2O H2 N2 O2 | ∑CO2 … … … … … | ∑CO2′ … … … … … | |
| Итого: | ∑Мгаз = | ∑Мгаз′ = |
Составляем сводную таблицу материального баланса.
Таблица 7
Материальный баланс плавки (до раскисления)
| Поступило, кг | Получено, кг | ||
| Чугун Лом Миксерный шлак Загрязнения лома Окалина лома Плавиковый шпат Известь Футеровка Дутье | Мч Мл Мм.шл Мз.л Мок.л Мпл.ш Мизв Мф Мдутья | Жидкий металл Шлак Газы Угар железа в дым Выбросы Железо корольков | Мкмет Мкшл ∑Мгаз 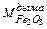 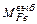 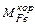 |
| Итого: | Итого: |
Невязка = 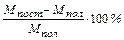 =
=
(допустимая невязка 0,2 %)
6.3. Расчет теплового баланса плавки
Расчет ведется на 100 кг металлошихты.
ПРИХОД ТЕПЛА кДж:
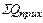 =
= 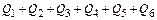 , (57)
, (57)
где 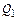 – физическое тепло жидкого чугуна;
– физическое тепло жидкого чугуна; 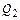 – химическое тепло реакций окисления примесей металлошихты;
– химическое тепло реакций окисления примесей металлошихты; 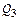 – химическое тепло реакций шлакообразования;
– химическое тепло реакций шлакообразования; 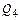 – химическое тепло реакций образования оксидов железа шлака;
– химическое тепло реакций образования оксидов железа шлака; 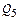 – химическое тепло испарения железа до оксида железа;
– химическое тепло испарения железа до оксида железа; 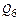 – физическое тепло миксерного шлака.
– физическое тепло миксерного шлака.
Физическое тепло жидкого чугуна, кДж
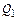 =
= 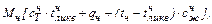 (58)
(58)
где 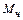 – количество чугуна, кг;
– количество чугуна, кг; 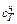 – теплоемкость твердого чугуна (0,755 кДж/(кг · град);
– теплоемкость твердого чугуна (0,755 кДж/(кг · град); 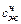 – теплоемкость жидкого чугуна (0,92 кДж/(кг · град);
– теплоемкость жидкого чугуна (0,92 кДж/(кг · град);
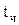 – температура заливаемого в конвертер чугуна,
– температура заливаемого в конвертер чугуна, 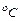 ;
; 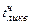 – температура плавления (ликвидуса) чугуна (1150 – 1200
– температура плавления (ликвидуса) чугуна (1150 – 1200 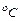 );
); 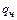 – скрытая теплота плавления чугуна (218 кДж/кг).
– скрытая теплота плавления чугуна (218 кДж/кг).
Химическое тепло окисления примесей металлошихты, кДж
Таблица 8
Химическое тепло окисления примесей
| Элемент-оксид | Окисляется примесей, кг | Тепловой эффект реакции окисления (на 1 кг элемента), кДж | Выделяется тепла, кДж | % от 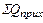 |
| С → СО | 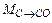 = = 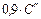 = = | 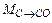 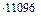 = = | ||
| С → СО2 | 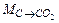 = = 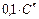 = = | … | ||
| Si → SiO2 | 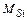 = = 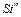 = = | … | ||
| Mn→MnO | 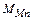 = = 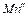 = = | … | ||
| P→P2O5 | 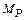 = = 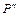 = = | … | ||
| Итого: | Q2= | 100,00 |
Химическое тепло реакций шлакообразования, кДж
Принимаем, что весь SiO2 и P2O5 в шлаке связываются в соединения с оксидом кальция по реакциям:
1. SiO2+ 2СаО = 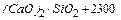 кДж/ кг
кДж/ кг
2. P2O5 + 4СаО = 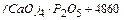 кДж/ кг
кДж/ кг
тогда 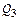 =
= 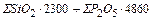 ; (см.(35)и(40)) (59)
; (см.(35)и(40)) (59)
Химическое тепло реакций образования оксидов железа шлака, кДж
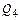 =
= 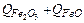 ,
,
где 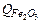 – количество тепла железа, окислившегося до
– количество тепла железа, окислившегося до 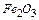 ;
; 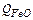 – количество тепла железа, окислившегося до
– количество тепла железа, окислившегося до 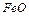 .
.
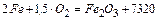 кДж/кг;
кДж/кг;
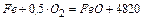 кДж/кг.
кДж/кг.
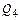 =
= 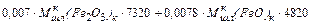 ; (60)
; (60)
(см. табл. 5)
Химическое тепло реакций окисления железа до оксида железа дыма, кДж
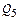 =
= 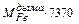 , (61)
, (61)
Физическое тепло миксерного шлака, кДж
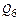 =
= 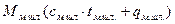 , (62)
, (62)
где 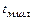 – средняя температура миксерного шлака,
– средняя температура миксерного шлака, 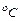 ;
;
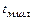 =
= 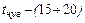 ;
;
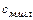 – средняя теплоемкость миксерного шлака, кДж/(кг∙град)
– средняя теплоемкость миксерного шлака, кДж/(кг∙град)
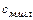 =
= 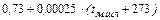 ;
;
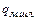 = 210 кДж/кг – скрытая теплота плавления миксерного шлака.
= 210 кДж/кг – скрытая теплота плавления миксерного шлака.
РАСХОД ТЕПЛА, кДж:
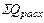 =
= 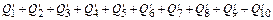 , (63)
, (63)
где 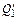 – физическое тепло жидкой стали;
– физическое тепло жидкой стали; 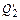 – физическое тепло конечного шлака;
– физическое тепло конечного шлака; 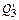 – тепло отходящих газов;
– тепло отходящих газов; 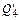 – тепло диссоциации влаги, вносимой шихтой;
– тепло диссоциации влаги, вносимой шихтой; 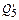 – тепло диссоциации
– тепло диссоциации 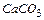 шихтовых материалов;
шихтовых материалов; 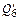 – тепло диссоциации оксидов железа, внесенных шихтой;
– тепло диссоциации оксидов железа, внесенных шихтой; 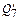 – тепло, уносимое оксидом железа дыма;
– тепло, уносимое оксидом железа дыма; 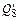 – тепло, уносимое железом выбросов;
– тепло, уносимое железом выбросов; 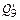 – тепло, уносимое железом корольков;
– тепло, уносимое железом корольков; 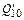 – потери тепла на нагрев футеровки, излучением через горловину, на нагрев воды, охлаждающей фурму и другие неучтенные потери.
– потери тепла на нагрев футеровки, излучением через горловину, на нагрев воды, охлаждающей фурму и другие неучтенные потери.
Физическое тепло жидкой стали, кДж
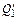 =
= 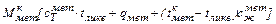 , (64)
, (64)
где 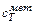 = 0,70 кДж/(кг · град) – теплоемкость твердого металла;
= 0,70 кДж/(кг · град) – теплоемкость твердого металла; 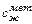 = 0,84 кДж/(кг град) – теплоемкость жидкого металла;
= 0,84 кДж/(кг град) – теплоемкость жидкого металла; 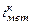 – температура металла в конце продувки;
– температура металла в конце продувки; 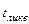 – температура плавления (ликвидуса) металла,
– температура плавления (ликвидуса) металла, 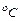 ;(см. раздел 6.1);
;(см. раздел 6.1); 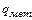 = 285 кДж/кг – скрытая теплота плавления металла.
= 285 кДж/кг – скрытая теплота плавления металла.
Физическое тепло жидкого шлака, кДж
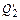 =
= 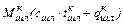 , (65)
, (65)
где 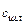 = 0,73 + 0,00025
= 0,73 + 0,00025 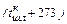 – средняя теплоемкость конечного шлака, кДж/(кг · град);
– средняя теплоемкость конечного шлака, кДж/(кг · град); 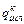 = 210 кДж/кг – скрытая теплота плавления шлака;
= 210 кДж/кг – скрытая теплота плавления шлака; 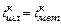 .
.
Тепло, уносимое отходящими газами, кДж
Среднюю температуру отходящих газов принимаем равной средней температуре металла во время продувки:
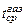 =
= 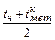
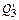 = Σ
= Σ 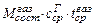 , (66)
, (66)
где 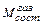 – количество составляющей отходящих газов,
– количество составляющей отходящих газов, 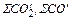 и т.д., нм3 (см. табл. 6);
и т.д., нм3 (см. табл. 6); 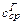 - средняя теплоёмкость газов, кДж/(м3∙град) (из табл. 9 заносим в табл. 10)
- средняя теплоёмкость газов, кДж/(м3∙град) (из табл. 9 заносим в табл. 10)
Таблица 9
Теплоёмкость газов
| Газ | Средняя теплоёмкость, кДж/(м3∙град) при 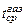 , 0С , 0С | ||||||
| CO2 | 2,26 | 2,28 | 2,30 | 2,32 | 2,34 | 2,36 | 2,38 |
| CO | 1,43 | 1,44 | 1,45 | 1,46 | 1,47 | 1,48 | 1,49 |
| H2O | 1,77 | 1,79 | 1,81 | 1,83 | 1,85 | 1,87 | 1,89 |
| H2 | 1,33 | 1,34 | 1,35 | 1,36 | 1,37 | 1,38 | 1,39 |
| N2 | 1,40 | 1,41 | 1,42 | 1,43 | 1,44 | 1,45 | 1,46 |
| O2 | 1,49 | 1,50 | 1,51 | 1,52 | 1,53 | 1,54 | 1,55 |
Таблица 10
Тепло отходящих газов
| Газ | Количество газов, нм3 | Средняя теплоемкость газов | Уносится тепла, кДж |
| СО2 | ∑СО2′ | ||
| СО | … | ||
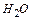 | … | ||
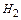 | … | ||
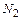 | … | ||
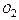 | … | ||
| Итого: | Q3′ |
Тепло диссоциации влаги, вносимой шихтой, кДж
При диссоциации влаги по реакции:
