Исследование электрохимического поведения ниобатов стронция, допированных тяжёлыми металлами
Кадникова Е.Н.,1 Юровская Н.Л.2
1Уральский Федеральный Университет имени первого Президента России Б.Н. Ельцина,
Екатеринбург, Россия.
Студент IV курса.
2Уральский Федеральный Университет имени первого Президента России Б.Н. Ельцина, Екатеринбург, Россия. Студент IV курса.
Научный руководитель: Подкорытов А.Л., Штин С.А.
Одной из важнейших задач современной аналитической химии является количественное определение тяжелых металлов в различных объектах окружающей среды. Для контроля их содержания необходимы точные, чувствительные и экспрессные методы анализа. Одним из таких методов является потенциометрия с использованием ионоселективных электродов. На основе сложнооксидных соединений – Sr4-хCdхNb2O9, (х = 0,1; 0,3; 0,5; 0,7) и Sr4Cu2Nb2O11, Sr3CuNb2O9 изготовлены и апробированы в ионометрии пленочные электроды с твердым контактом (инертные матрицы – полистирол, полиметилметакрилат, поливинилхлорид). В работе изучены основные характеристики ИСЭ: область линейности, крутизна основной электродной функции, рабочая область pH и воспроизводимость этих характеристик (табл. 1, 2).
Таблица 1. Электрохимические характеристики ИСЭ
| Состав мембраны | Матрица | Область линейно- сти моль/л | Крутизна мВ/рМе | Рабочая область рН | Коэффициенты селективности | |||
| K+ | Zn2+ | Ni2+ | Cd2+ | |||||
| Sr4Cu2Nb2O11 | ПС* | 10-5 - 10-1 | -32,7 | 1,6-4,5 | 0,020 | 0,052 | 0,050 | 0,043 |
| ПС | 10-4 - 10-1 | -30,8 | 1,6-4,5 | 0,011 | 0,112 | 0,076 | 0,017 | |
| ПММА* | 10-7 - 10-1 | -38,2 | 3,9-5,0 | 0,012 | 0,113 | 0,724 | 0,271 | |
| ПММА | 10-4 - 10-1 | -29,5 | 3,9-5,0 | 7,9*10-5 | 0,020 | 0,036 | 0,020 | |
| ПВХ | 10-4 - 10-1 | -30,0 | 3,9-5,3 | 7,5*10-6 | 0,017 | 0,032 | 0,023 | |
| Sr3CuNb2O9 | ПВХ | 10-4 - 10-1 | -21,3 | 2,0-4,9 | 0,813 | 0,056 | 0,056 | 0,260 |
*новая конструкция ИСЭ
Таблица 2. Воспроизводимость электрохимических характеристик ИСЭ
| Состав мембраны | Матрица | Результаты | |||
| Весна | Осень 2011 | Весна 2011 | Осень 2011 | ||
| Область линейности, моль/л | Крутизна электродной функции, мВ/рМе | ||||
| Sr3,9Cd0,1Nb2O9 | ПВХ | 10-4 – 10-1 | 10-6 – 10-1 | -12,6 | -14,1 |
| Sr3,9Cd0,1Nb2O9 | ПММА | 10-4 – 10-1 | 10-3 – 10-1 | -14,2 | -15,5 |
| Sr3,7Cd0,3Nb2O9 | ПВХ | 10-4 – 10-1 | 10-5 – 10-1 | -12,1 | -16,9 |
| Sr3,5Cd0,5Nb2O9 | ПВХ | 10-4 – 10-1 | 10-6 – 10-1 | -15,8 | -28,7 |
| Sr3,3Cd0,7Nb2O9 | ПВХ | 10-4 – 10-1 | 10-5 – 10-1 | -17,7 | -24,6 |
| Sr4Cu2Nb2O11 | ПС | 10-4 – 10-1 | 10-4 – 10-1 | -30,8 | -21,2 |
| Sr4Cu2Nb2O11 | ПВХ | 10-4 – 10-1 | 10-4 – 10-1 | -30,0 | -33,2 |
| Sr4Cu2Nb2O11 | ПММА | 10-4 – 10-1 | 10-4 – 10-1 | -29,5 | -29,9 |
Время отклика всех изученных электродов составило от 2 до 5 минут. Для Сu-СЭ электродов проведено комплексонометрическое титрование с потенциометрической индикацией конечной точки титрования. Установлено, что погрешность определения меди не превышает 10 %. Определению не мешают ионы никеля, кадмия, цинка, натрия и калия с концентрацией до 10-2 моль/л. При внесении некоторых конструкционных изменений область линейности основной электродной функции на основе Sr4Cu2Nb2O11 (ПММА) составила 6 порядков: от 10-7 до 10-1 моль/л (рис. 1).
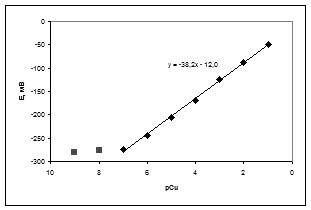
Рис. 1 Градуировочный график для электрода на основе Sr4Cu2Nb2O11 (ПММА) при рН=4,5
Кадмийселективные электроды были испытаны в качестве индикаторных при потенциометрическом титровании кадмийсодержащих объектов растворами ЭДТА и K4[Fe(CN)6]. Удовлетворительные результаты получены при использовании в качестве титранта гексацианоферрата (II) калия. Относительная погрешность определения кадмия не превышает 3%.
НИР выполнена при поддержке Министерства образования и науки в рамках ФЦП «Научные и научно – педагогические кадры инновационной России» на 2009 – 2013 годы (ГК № П984 от 27 мая 2010).
