Приготування розчину соляної кислоти
Концентрована соляна кислота (11-11,7М) – це насичений розчин хлористого водню у воді. При розведенні концентрованого розчину соляної кислоти водою хлористий водень частково летить. Тому приготувати титрований розчин соляної кислоти з концентрованої соляної кислоти неможливо. Спочатку готують розчин приблизної концентрації, а потім точну концентрацію визначають. Для роботи використовують 0,1 М (вони ж 0,1 нормальні) розчини.
Послідовність приготування розчину соляної кислоти.
Ареометром вимірюють густину концентрованої соляної кислоти і за таблицею (довідник з аналітичної хімії) знаходять молярну концентрацію (масову частку) розчину, яка відповідає даній густині.
Розраховують об’єм цієї кислоти, який потрібно для приготування 0,1 М розчину соляної кислоти необхідного об’єму, відміряють його циліндром, розводять дистильованою водою до заданого об’єму і добре перемішують.
Наприклад, густина концентрованої соляної кислоти ρ=1,14 г/см3, за довідником цій густині відповідає концентрація НСl 8,8 моль/л. Необхідно приготувати 1 л (1000 мл) 0,1 М розчину соляної кислоти.
Об’єм концентрованої соляної кислоти, який потрібно взяти для розведення, розраховують із співвідношення
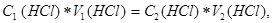 звідси
звідси
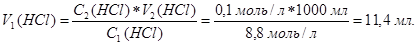
Якщо в довіднику немає молярної концентрації розчину НСl, а є тільки масова частка (w(HCl)=28,18 г в 100 г розчину для густини ρ=1,14 г/см3):
1) розраховують масу кислоти, що міститься в 1000 мл 0,1 М розчину НСl
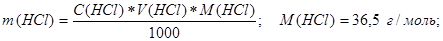
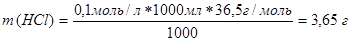 .
.
2) розраховують масу розчину концентрованої НСl, в якому міститься 3,65 г речовини НСl
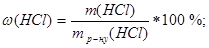
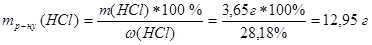 .
.
3) оскільки брати наважку розчину незручно, переходять від маси розчину до об’єму
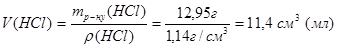 .
.
4) відміряють 11,4 мл концентрованої НСl, розводять дистильованою водою до одного літра, перемішують. Одержаний розчин НСl – 0,1 М.
3.2 Визначення концентрації розчину HCl за титрованим розчином NaOH (Практична робота)
Концентрацію розчину соляної кислоти визначають титруванням розчином вихідної речовини відомої концентрації.
Принцип методу. Точний об’єм розчину гідроксиду натрію відомої концентрації титрують розчином НСl, концентрацію якого необхідно визначити. При титруванні відбувається реакція:
NaOH + HCl → NaCl + H2O.
Стрибок титрування сильних основ (лугів) сильними кислотами великий – від 10 до 4 одиниць рН для 0,1 М розчинів. Це дозволяє застосувати для фіксації точки еквівалентності будь-який рН-індикатор, інтервал переходу якого знаходиться в межах стрибка титрування.
Необхідні реактиви і посуд:
1. Бюретка, 25 мл, 2 шт.
2. Колба для титрування.
3. Титрований розчин NaOH.
4. рН-індикатори.
Хід аналізу
В колбу для титрування відміряють із бюретки 10-20 мл розчину гідроксиду натрію, розбавляють дистильованою водою приблизно до 50 мл, добавляють 1-2 краплі метилового оранжевого і титрують розчином кислоти, концентрацію якого слід визначити, при постійному перемішуванні до зміни забарвлення від жовтого до абрикосового. Записують відлік на бюретці. Титрування проводять не менше трьох разів.
Результати заносять у таблицю. Концентрацію розчину кислоти розраховують за формулою
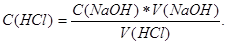
Для ознайомлення з властивостями інших індикаторів проводять ще титрування з метиловим червоним і фенолфталеїном не менше трьох разів. Аналогічно визначають концентрацію розчину лугу за титрованим розчином кислоти.
Контрольні запитання:
1. У чому суть визначення концентрації розчину соляної кислоти за титрованим розчином їдкого натру?
2. Розрахуйте криву титрування 100 мл 0,1 М розчину NaOH 0,1 М розчином HCl. Підберіть індикатор. Вибір індикатора обґрунтуйте.
3. Чому при титруванні розчину сильної основи розчином сильної кислоти краще користуватися метиловим оранжевим, а не фенолфталеїном?
4. Які розходження в об’ємі допускаються між результатами паралельних визначень?
5. Розрахувати T(HCl), T(HCl/NaOH), якщо C(HCl) = 0,1084 моль/л.
3.3. Визначення концентрації розчину НСl за натрій тетраборатом (Практична робота)
Щоб визначити концентрацію розчину кислоти, застосовують такі вихідні речовини: Na2B4O7·10H2O – натрій тетраборат, Na2CO3 – натрій карбонат (сода), KHCO3 – калій гідрокарбонат, KJO3 – калій іодат та ін.
Принцип методу. Для визначення концентрації HCl застосовують метод окремих наважок. При титруванні натрій тетраборату хлороводневою кислотою відбуваються реакції:
Na2B4O7 +7H2O D 2 NaOH + 4 H3BO3,
2 NaOH + 2 HCl ® 2 NaCl + 2 H2O,
__________________________________________
Na2B4O7 + 2 HCl +5 H2O ® 4 H3BO3 + 2 NaCl.
Для визначення точки еквівалентності, застосовують індикатор, показник титрування (рТ) якого близький до рН у точці еквівалентності. У точці еквівалентності розчин містить тільки хлорид натрію (рН=7) та борну кислоту Н3ВО3, яка зумовлює слабокислу реакцію розчину. Значення рН розчину у точці еквівалентності можна розрахувати за формулою для обчислення рН розчинів слабких кислот. Враховуючи те, що борна кислота є слабкою кислотою, дисоціація її здійснюється, головним чином, за першим ступенем:
H3BO3 D H + + H2BO3.-
Константа дисоціації має вигляд:
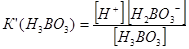 .
.
З рівняння дисоціації кислоти концентрація іонів [Н+] = [Н2ВО3-]. Оскільки Н3ВО3 в розчинах дисоціює мало, то можна вважати, що концентрація молекул кислоти дорівнює загальній концентрації кислоти [Н3ВО3] = С (Н3ВО3). Тоді з виразу константи дисоціації можна вивести таку залежність:
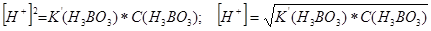 .
.
Розрахунки рН:
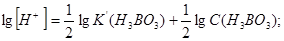


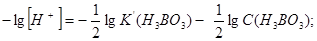
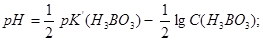
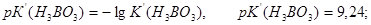
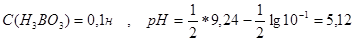 .
.
Титрування буде більш точним тоді, коли застосувати індикатор з показником титрування 5,12 або близьким до цього значення. Таке значення рН у точці еквівалентності відповідає показнику титрування метилового червоного (рТ=5,5).
Обчислення маси наважки
Натрій тетраборат має перевагу, як вихідна речовина, у тому, що має велику молярну масу еквівалента. Згідно з рівнянням реакції
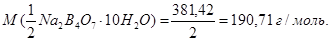
Наважку обчислюють з огляду на рівність кількості моль-еквівалентів реагуючих речовин, а саме:
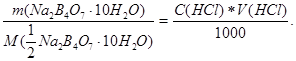
Концентрація кислоти (HCl) приблизно 0,1 М, об’єм кислоти беруть такий, щоб на титрування було достатньо однієї заповненої бюретки. Якщо користуються бюреткою на 25 мл, то для обчислення наважки беруть 20,0 мл:
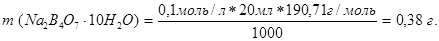

Необхідні реактиви і посуд:
1. Бюретка, 25 мл.
2. Колба для титрування.
3. Лійка.
4. Мірний циліндр, 100 мл.
5. Натрій тетраборат Na2B4O7·10H2O.
6. Індикатор – метиловий червоний.
Хід аналізу
Наважку натрій тетраборату близько 0,38 г зважують на аналітичних терезах, висипають її в колбу для титрування, розчиняють у гарячій воді приблизно 50 мл. Розчин охолоджують до кімнатної температури, добавляють 1-2 краплини метилового червоного і титрують розчином HCl до зміни забарвлення розчину від жовтого до рожевого.
Титрування проводять тричі. Концентрацію хлороводневої кислоти розраховують за формулою
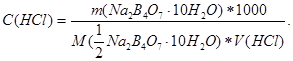
Контрольні запитання:
1. Які вихідні речовини застосовують для визначення концентрації хлороводневої кислоти? Їх переваги і недоліки.
2. Яким методом буде точніше визначена C(HCl) за натрій тетраборатом – методом піпетування чи методом окремих наважок?
3. Розрахуйте наважку Na2B4O7·10H2O для титрування.
4. У чому суть методу визначення C(HCl) за натрій тетраборатом.
5. Розрахуйте рН у точці еквівалентності.
6. Поясніть вибір індикатора.
7. Чи можливе титрування з індикатором фенолфталеїном? Яка помилка?
8. Розрахуйте С(HCl) та Т(HCl) за результатами титрування.
9. Як впливає температура на результати титрування?
10. Які інші методи визначення концентрації HCl вам відомі?
