ДӘРІС 2 Химиялық реакциялардың жылулық эффектісі
Химиялық реакциялардық жылулық эффектісі реакцияға қатысушы заттардың физикалық күйіне байланысты болады. Термохимиялық салыстырмалы есептеулер жүргізу үшін заттардың стандартты күйі алынган.Стандартты күйге P=1атм =1,013*105Па және t=250С (298.15 К)
Стандартты күйдегі термодинамикалық параметрлер былай белгіленеді:Qv298,Qp298, H298, S298 ,G298
Анықтамалық материалдарды,әдебиеттерде стандартты күйдегі термодинамикалық параметрлер көптеп берілген және сол параметрлерді қолдану арқылы көптеген термохимиялық есептеулер жүргізіледі.Есептеулер кезінде мына заңдылықтар сақталуы қажет:
1) Ыдырау реакциясының жылулық эффектісі химиялық қосылыстың түзілуі жылу эффектісінің кері мөлшеріне тең болады.
Qыд= -Qтүз
2) Егер екізаттан екі жолмен бір химиялық қосылыс алынатын болса,онда осы екі заттың бірбіріне айналу жылу эффектісі,олардың ушінші затқа айналу жылу эффектілерінің айырмасы болады.
Q1=Q2+Q3, немесе Q3=Q1-Q2 (14)
3)Егер бір заттан екі химиялық құрамы әртүрлі екі қосылыс алынатын болса, алынған екі қосылыстын бір- біріне айналу жылулық эффектісі тең болады.
Q1
Q1=Q2+Q3, Q3=Q1-Q2 (15)
Термохимиялық есептеулерде негізінен реакцияларды екі жылу эффектісі анықталады:қосылыстардың түзілу жылуы және жану жылуы.
Түзілу жылу деп қосылыстардын жай заттардан стандартты күйдегі түзілгенде бөлінетін жылу эффектісін айтады.Мысалы бензолдын түзілуі;
6Cт + 3Н2т→С6Н6 (16)
бұл жердегі индекстер заттың күйін сипаттайды.
т-қатты, г-газ, ж-сұйық
Термодинамикалық есептерде ішкі энергия мен энтальпияның абсолюттік мәнін анықтамайды,олардың өзгеру шамасы анықтайды.Мысалы анықтамаларды жай заттардың стандартты күйде энтальпиясы нольге тең болады.Оларға атомның немесе молекула түріндегі жай заттар жатады:C,Si,O2,H2,CL2,Ғ2 ж.т.б.
Сондықтан осы заттардан түзілген қосылыстардың энтальпиясы түзілу реакциясының жылулық эффектісіне тең болады.Түзілу жылуы 1кг немесе 1 кмоль қосылысқа анықталады.Анықтамаларға химиялық қосылыстардың түзілу жылуы берілген. Мысалы; (таблицаны 1 көрсету керек)
Жану жылу: Жануы тез жүретін химиялық өзгеріс. Бұл процесс жарық шығаратын белгілі бір мөлшерде жылу бөлу арқылы жүреді. Жану реакциясының жылу эффектісі жану жылуы деп атайды.
Көмір және оның сутегілік қосылыстары жанғанда бөлінетін жылу отынның жану жылуы деп атайды. Жану жылу тотығу реакциясының жылу эффектісі болып саналады.Жылу эффектісін калориметрлік бомба деп аталатын құралдың көмегімен анықталады.(калортметрлік бомбаның сызбасы мен жұмысы.Өзіндік жұмыс студенттерге)
Отынныңжану жылуы дж, кдж өлшенеді.1 кг,масса , 1м3 көлем ,немесе 1 кмоль отын жанғанда бөлінетін жылу мөлшері анықтамаларда беріледі.Жану жылуы жоғарғы және төменгі болып екіге бөлінеді.
Жоғарғы жану жылуы: отын толық жанғанда бөлінетін жылуды айтады.Төменгі жану жылуы отынның жоғарғы жану жылуынан отын құрамындағы судың буға айналу жылуын алғандағы жану мөлшерін айтады.
Жоғарғы және төменгі жану жылулары бір-бірімен былай байланысты:
-Qт=-Qж+R в (9H+W) =-Qж+2,512*106(9H+W)дж/кг
Rв=2,512*106*дж/кг – буға айналудың белгісіз жылуы.
9Н-1кг сутегін жаққанда пайда болатын су мөлшері
W-1кг отындағы ылғал судың мөлшері.
ДӘРІС 3 Гесс заңы
Гесс заңы бойынша реакцияның жылулық эффектісі реакцияға түсуші заттар мен реакциядан түзілген заттардың жану жылуының айырмасына тең:
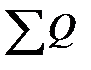 p=
p= 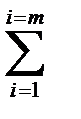 (niQi)исх -
(niQi)исх - 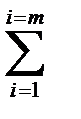 (niQi)пр (17)
(niQi)пр (17)
Мысалы:СО жанып СО2 түзгенде және Н2 жанып Н2О түзгенде жану жылулары 283,01*105 және 214,84*105 дж/кмоль.
Берілген жағдайда СО+Н2О=СО2+Н2+Qр реакциясының жылу эффектісін табыңдар.
Шешуі: Алдымен белгілі реакцияларды жазамыз.
СО+0,5О2=СО2-283,01*105 дж/кмоль
Н2 +0,5О2=Н2О-241,84*105 дж/моль
Екі теңдеуді бір-бірінен алатын болсақ
СО-Н2=СО2-Н2о-41,17*105 дж/моль
СО+Н2О=СО2+Н2- дж/моль
реакцияның жылу эффектісі Qр=41,17*105 дж/моль
