Топша элементтері, сілтілік металдар. Натрий, калий, оның қосылыстары, химиялық қасиеттері, қолданылуы.
Сілтілік металдар ІА топшада орналаскан: литий Li, натрий Na, калий К, рубидий Rb, цезий Cs, франций Fr. Франций - радиобелсенді элемент. Олардың валенттілік электрондарының жалпы формуласы ns1 (n = 2-7). Олардың топтық атауы - сілтілік металдар — сумен әрекеттескенде күшті негіз - сілті түзуіне байланысты қойылған .
Na
Табиғатта таралуы
Табиғатта таралуы бойынша натрий 6-шы орын алады, ол тек қосылыстар күйінде кездеседі: NaNО3 - чили селитрасы; NaCl - галит, ас тұзы; Na2CО3 • 10Н2О - сода; Na2SО4 • 10Н20 – глаубер тұзы; NaCl*KC1 - сильвинит, т.б. Ең маңызды қосылысы NaCl – ас тұзы, тұзды көлдердің негізгі құраушысы (Арал, Балқаш).
Химиялың қасиеттері
Натрий химиялық белсенді элемент, себебі валенттілік электроны ядросымен әлсіз байланысқан, олай болса, валенттілік электронын оңай беріп, тотықсыздандырғыштық қасиет көрсетеді. Сонда мына үдеріс жүреді:
Na0 - е —> Na+
1. Бейметалдармен әрекеттескенде екі түрлі қышкылдың тұзы түзіледі.
2. Қышкылдық және екідайлы оксидтермен тұз және су түзе әрекеттеседі.
3. Қышқылдармен де осы тектес заттар береді;
4. Тұздармен реакцияласуы:
o a) орта тұздармен: 3NaOH + ҒеС13 = NaCl + Ғе(ОН)3У
o ә) қышқыл тұздармен: NaOH + NaHS04 = Na2S04 + Н20
o в) негіздік тұздармен: 2NaOH + А1(ОН)С12 = А1(ОН)3 У+ 2NaCl
Натрийдің қосылыстарының қолданылуы
Натрий ғылым мен техниканың әр алуан саласында қолданылады: ядролық реакторларда жылу тасымалдаушы ретінде, органикалық реакцияларда өршіткі, медицинада радиоактивті изотоп күйінде қолданылады.
Натрий гидроксиді - қағаз, сабын, дәрі-дөрмек, жасанды талшық өндірістерінде, мұнай өнімдерін тазартуда қолданылады
Калий қосылыстары – калий элементін түзетін тұрақты химиялық қосылыстар. Металл күйіндегі калий мен натрий өзара ери араласып, сұйық күйдегі балқыма түзеді, ол атом реакторында жылу тасымалдаушы, титан өндірісінде тотықсыздандырғыш ретінде қолданылады. Калий қосылыстарының арасында тұздары маңызды, бәрі дерлік тыңайтқыш ретінде пайдаланылады. Калий селитрасы KNO3 – өте тиімді тыңайтқыш, жақсы тотықтандырғыш, оқ-дәрі, қопарғыш заттар әзірлеуде пайдаланылады. Бромды калий фотосурет өңдеуде негативті сақтау үшін, йодты калий (KI) медицинада химиялық реактив ретінде, фторлы калий (КҒ) металлургиялық флюс құрамында және органикалық қосылысқа фторды енгізу мақсатында, көмір қышқылды калий (K2CO3) (поташ) шыны мен сабын өндіруде, калий фосфаттары (K4P2O7; K5P3O10) жуғыш зат құрамдасы ретінде, калий хлораты (KCІO3) (бертоле тұзы) сіріңке мен пиротехника өндірісінде, кремний фторлы калий (K2SіF6) минералдардан сирек жер металын алу кезіндегі қоспа ретінде, цианды калий (KCN) алтын өндіруде, калий сілтісі (KOH) таза калийді, оның тұздарын алуда, аккумулятор жасауда қолданылады
Взаимодействие с простыми веществами
Калий при комнатной температуре реагирует с кислородом воздуха, галогенами; практически не реагирует с азотом (в отличие от лития и натрия). При умеренном нагревании реагирует с водородом с образованием гидрида (200—350 °C):
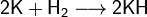 ,
,
с халькогенами (100—200 °C, E = S, Se, Te):
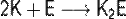 .
.
При сгорании калия на воздухе образуется надпероксид калия KO2 (с примесью K2O2):
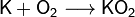
В реакции с фосфором в инертной атмосфере образуется фосфид зелёного цвета (200 °C):
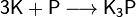
Взаимодействие со сложными веществами
Калий при комнатной температуре активно реагирует с водой, кислотами, растворяется в жидком аммиаке (−50 °C) с образованием тёмно-синего раствора.
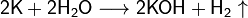
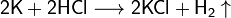
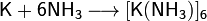
Калий глубоко восстанавливает разбавленные серную и азотную кислоты:
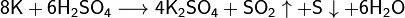
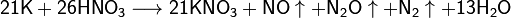
При сплавлении металлического калия со щелочами он восстанавливает водород гидроксогруппы:
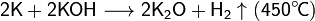
При умеренном нагревании реагирует с газообразным аммиаком с образованием амида (65—105 °C):
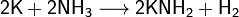
Металлический калий реагирует со спиртами с образованием алкоголятов:
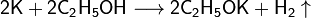
Алкоголяты щелочных металлов (в данном случае, этаноат калия) являются очень сильными основаниями и широко используются в органическом синтезе.
Соединения с кислородом
При взаимодействии калия с кислородом воздуха образуется не оксид, а пероксид и супероксид:
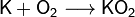
Оксид калия может быть получен при нагревании металла до температуры не выше 180 °C в среде, содержащей очень мало кислорода, или при нагревании смеси супероксида калия с металлическим калием:
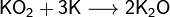
Оксиды калия обладают ярко выраженными основными свойствами, бурно реагируют с водой, кислотами и кислотными оксидами. Практического значения они не имеют. Пероксиды представляют собой желтовато-белые порошки, которые, хорошо растворяясь в воде, образуют щёлочи и пероксид водорода: