УСТАНОВЛЕНИЕ ТОЧНОЙ КОНЦЕНТРАЦИИ И ТИТРА KmnO4 ПО 0,05N РАСТВОРУ ЩАВЕЛЕВОЙ КИСЛОТЫ
Точную концентрацию и титр KmnO4 устанавливают по щавелевой кислоте.
В основе процесса титрования лежит реакция между KmnO4 и Н2С2О4.2Н2О в кислой среде.
KmnO4 + H2SO4 + H2C2O4 ® MnSO4 + K2SO4 + CO2 + H2O
Ход определения
Бюретку промывают 2-3 раза небольшими порциями 0,05 н раствора KmnO4 и заполняют ее этим же раствором. Кончик бюретки должен быть полностью заполнен раствором перманганата. Пипетку вместимостью 5 мл ополаскивают раствором щавелевой кислоты, а затем вносят 5 мл раствора Н2С2О4 в коническую колбу для титрования. Добавляют 2 – 2,5 мл 2н раствора Н2SO4 и нагревают на водяной бане до 70 – 80оС, не допуская кипения раствора. Горячий раствор титруют перманганатом калия, добавляя его по каплям и непрерывно перемешивая. Следующую каплю добавляют после обесцвечивания в растворе предыдущей. Сначала обесцвечивание преманганата происходит медленно, а затем . по мере образования ионов Mn2+, играющих роль катализатора, реакция ускоряется. По достижении точки эквивалентности избыточная капля KmnO4 окрашивает раствор в бледно-розовый цвет, не исчезающий 1 – 2 минуты.
Объем KmnO4, затраченный на титрование отмечают по бюретке по верхнему мениску. Титрование повторяют 3 раза и данные заносят в таблицу 1. По данным титрования рассчитывают точную концентрацию и титр KmnO4.
Табл.1.
| N п/п | VH2C2O4 2H2O | NH2C2O4 2H2O | VKmnO4 | NKmnO4 | TKmnO4 |
| Сред-нее |
Расчет:
N KmnO4 = 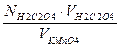
ОПРЕДЕЛЕНИЕ ЖЕЛЕЗА (II) МЕТОДОМ ПЕРМАНГАНАТОМЕТРИИ.
В основе определения лежит окислительно-восстановительная реакция, при которой ион Fe2+ окисляется в Fe3+. В кислой среде окисление протекает быстро по уравнению:
MnO4- + 5Fe2+ + 8H+ ® Mn2+ + 5Fe3+ + 4H2O
MnO4- + 5e + 8H+ ® Mn2+ + 4H2O 2
2Fe2+ - 2e ® 2Fe3+ 5
Исследуемый раствор подкисляют серной кислотой и титруют перманганатом калия до появления в растворе бледно-розовой окраски.
 Ход определения:
Ход определения:
В колбу для титрования вносят пипеткой Мора 5мл полученного раствора соли железа (II) и 2-3 мл раствора H2SO4 (1:4), затем титруют раствором перманганата калия KmnO4 до слабо-розовой окраски. Титрование повторяют 2-3 раза.
Вычисление результатов анализа:
V- Вычисление проводят, пользуясь выражением концентрации через титр по определяемому веществу.
TKmnO4/Fe = 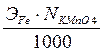
V- Рассчитывают, сколько граммов Fe (II) содержится в 5 мл раствора соли железа (II), взятого для титрования.
MFe = TKmnO4/Fe V1 KmnO4
V1 KmnO4 - объем раствора, пошедшего на титрование 5 мл соли железа (II).
3. Находят количество железа (II) в исследуемом растворе.
PFe = 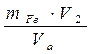
V2 - объем железа (II) приготовленного раствора, мл
Vа - объем аликвоты, взятой на титрование, мл
