Скорость реакции в данный момент времени называется истинной
Математическое выражение скорости представляет собой производную концентрации во времени: υист = ± dc/dτ
Скорость реакции зависит от многих факторов: концентрации, природы и дисперсности реагентов, температуры, катализатора, рН среды и др.
Влияние концентрации на скорость химической реакции выражается законом действующих масс: при постоянной температуре скорость химической реакции прямо пропорциональна концентрации реагирующих веществ:
aА + bВ → dD
υ = k × Са(А) × Сb(B)
где k — константа скорости, указывает долю столкновений, которые приводят к осуществлению реакции;
C(А) и C(В) – молярные концентрации вещества А и В;
а и b – стехиометрические коэффициенты в уравнении реакции.
Число молекул, участвующих в элементарном акте химического взаимодействия, определяет молекулярность реакции.
Порядок реакции — это сумма показателей степеней концентрации веществ в уравнении закона действующих масс.
Так, реакция H2+ I2 = 2HI относится к реакциям второго порядка, так как уравнение закона действующих масс имеет вид υ = k × C(H2) × C(I2).
Время, в течение которого прореагировала половина начального количества вещества, называется временем полураспада и обозначается τ1/2.
Для реакции первого порядка:
τ1/2 = ln 2 / k
Можно рассчитать концентрацию вещества, зная период полураспада. Для реакций первого порядка
C = C0 × e–kt или lnC = lnC0 – kτ
С – концентрация вещества в данный момент времени,
С0 – исходная концентрация вещества,
е – экспонента,
k – константа скорости,
τ – время протекания реакции.
Зависимость скорости реакции от температуры выражается в приближенной форме правилом Вант-Гоффа: при повышении температуры на каждые 10° скорость реакции увеличивается примерно в 2-4 раза.В биологических системах скорость возрастает в 7-9 раз.
k2 = k1· γ (Δt/10)
Избыточная энергия, которой должны обладать молекулы для того, чтобы их столкновение могло привести к образованию нового вещества, называетсяэнергией активации.
Правило Вант-Гоффа не применимо для реакций в живом организме. Для этого используют уравнение Аррениуса
k = A × e–Ea/RT
в этом уравнении константа скорости k связана с экспоненциальным выражением e–Ea/RT
R – универсальная газовая постоянная, 8,314 Дж/моль·К;
Т – температура по шкале Кельвина;
Еа – энергия активации, которая обычно предполагается постоянной величиной, не зависящей от температуры;
А – предэкспоненциальный множитель.
Уравнение Аррениуса позволяет рассчитать константы скорости реакций при различных температурах:
ln 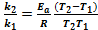
а так же при изменении энергии активации
ln 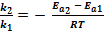
Скорость химических реакций может возрастать не только при увеличении концентрации реагирующих веществ или при увеличении температуры системы, но и под влиянием катализаторов.
