Основы атомно-молекулярного учения
При рассмотрении этой темы основное внимание уделить разделам:
1. Газовые законы;
2. Закон эквивалентов.
Усвоить основные понятия: моль, молярная масса, молярный объем газа, эквивалент, молярная масса эквивалента, молярный объем эквивалента вещества.
1. Состояние газа характеризуется его температурой T, давлением P и объемом V. Нормальные условия для газов P  = 101,3 кПa = 1 атм = 760 мм. рт.ст., T
= 101,3 кПa = 1 атм = 760 мм. рт.ст., T  = 00С = 273 K.
= 00С = 273 K.
Закон Авогадро: В равных объемах различных газов при одинаковых условиях содержится одинаковое число молекул.
Следствия из закона Авогадро:
I. Одинаковое число молекул различных газов при одинаковых физических условиях (T, P) занимает одинаковый объем.
Если число молекул равно числу Авогадро N 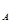 = 6,02∙10
= 6,02∙10 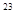 (1 моль газа), то при нормальных условиях они занимают объем 22,4 л (
(1 моль газа), то при нормальных условиях они занимают объем 22,4 л ( 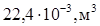 )
)
V 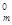 = 22,4 л/моль.
= 22,4 л/моль.
Плотность любого газа можно рассчитать по формуле 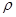 =
= 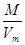 ,
,
где М - молярная масса газа (г/моль);
V 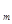 - молярный объем газа (л/моль).
- молярный объем газа (л/моль).
II. Относительная плотность одного газа (1) по другому (2) равна отношению их молярных масс при заданном давлении и температуре:
D 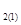 =
= 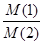
Относительная плотность газа по водороду D 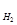 (Х) =
(Х) = 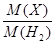 .
.
М (Х) = D 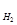 (Х) ∙ М (Н
(Х) ∙ М (Н  ) =
) = 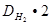
Относительная плотность газа по воздуху D воздух (Х) = 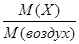 .
.
М (Х) = D 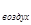 (Х)∙М (воздуха) = D воздух∙29
(Х)∙М (воздуха) = D воздух∙29
При низких температурах и высоких давлениях газы неидеальны и не подчиняются закону Авогадро.
Объединенный газовый закон:Для данной массы газа произведение давления на объем, деленное на абсолютную температуру, есть величина постоянная. 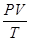 = const или
= const или 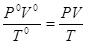
P0, V0, T0- соответственно давление, объем и температура данной массы газа при н. у.
Уравнение Менделеева – Клапейрона: PV = 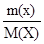 RT
RT
P- давление газа; T- температура (К); V- объем газа; М(Х)- молярная масса газа (г/моль); m(х)- масса газа (г); R- универсальная газовая постоянная = 8,314 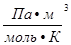 = 8,314
= 8,314 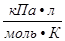 = 8,314
= 8,314 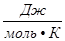 = 8,314 ∙10
= 8,314 ∙10 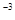
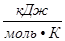 = 0,082
= 0,082 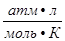 = 62,36
= 62,36 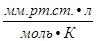 = 1,986
= 1,986 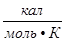 .
.
Закон Дальтона: Общее давление смеси газов, химически не взаимодействующих друг с другом, равно сумме давлений газов, составляющих смесь: P = p 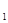 + p
+ p  + p
+ p  +… + p n,
+… + p n,
где P- общее давление; p 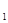 ,p
,p  ,p
,p  ,…,p n- парциальные давления газов 1,2,3,…,n.
,…,p n- парциальные давления газов 1,2,3,…,n.
Парциальным давлением газа в смеси называется давление, которое производил бы данный газ, если бы он один занимал весь объем, занимаемый смесью газов, при данной температуре.
Пример 1. Какой объем при н.у. занимают: а) 0,5 моль водорода; б) 32 г оксида азота (II)?
Решение: а) V 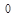 (H
(H  ) = n(H
) = n(H  )∙V
)∙V 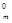 (H
(H  )
)
V  (Н
(Н  ) = 0,5моль∙22,4 л/моль = 11,2 л
) = 0,5моль∙22,4 л/моль = 11,2 л
б) n (NO) = 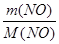 ; n (NO) =
; n (NO) = 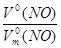 ;
;
 ; V
; V 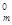 (NO) = 22,4 л/моль
(NO) = 22,4 л/моль
 M (NO) = 30 г/моль
M (NO) = 30 г/моль
V 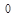 (NO) =
(NO) = 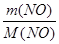 V
V 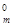 (NO)
(NO)
V  (NO) =
(NO) = 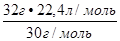 = 23,9 л
= 23,9 л
Ответ: V0(H2) = 11,2 л; V0(NO) = 23,9 л.
Пример 2. Вычислить объем, занимаемый 7 г оксида углерода (II) при 70C и 103974 Па.
Решение: Воспользуемся уравнением Менделеева – Клапейрона
P 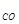 V
V 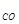 =
= 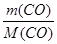 RT.
RT.
Откуда V 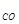 =
= 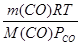 =
= 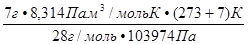 =0,0056 м
=0,0056 м 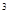 = 5,6 л
= 5,6 л
Ответ: VСО = 5,6л.
Пример 3. При температуре 27  С и давлении 2,5 атм газообразное вещество занимает объем 4,2 л. Вычислить объем газа при нормальных условиях.
С и давлении 2,5 атм газообразное вещество занимает объем 4,2 л. Вычислить объем газа при нормальных условиях.
Решение: Используем уравнение объединенного газового закона 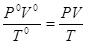 , откуда V
, откуда V  =
= 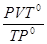 =
= 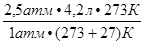 = 9,56 л.
= 9,56 л.
Ответ: V = 9,56 л.
Пример 4. Определить парциальные давления азота и кислорода в смеси объемом 7л, если общее давление в смеси равно 8,2МПа, а объемы смешиваемых газов равны 2л и 5л соответственно.
Решение:Объемные доли газов в смеси составляют 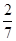 для азота и
для азота и 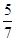 для кислорода. Следовательно, на долю азота приходится
для кислорода. Следовательно, на долю азота приходится 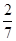 общего давления или 8,2 ∙
общего давления или 8,2 ∙ 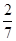 = 2,34 МПа, на долю кислорода- 8,2 ∙
= 2,34 МПа, на долю кислорода- 8,2 ∙ 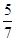 = 5,86 МПа, что и является их парциальными
= 5,86 МПа, что и является их парциальными  давлениями в смеси.
давлениями в смеси.
Ответ: P (N2) = 2,34 MПа, P (O2) = 5,86 МПа.
Пример 5. При некоторой температуре приготовили 8 л газовой смеси из 4 л оксида серы (IV), находившегося под давлением 720 мм. рт. ст., 6 л азота, находившегося под давлением 640 мм. рт. ст. и 3 л кислорода, находившегося под давлением 816 мм. рт. ст.. Определить парциальные давления газов в смеси и общее давление газовой смеси.
Решение: Находим, что объем оксида серы увеличился в 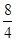 =2 раза, объем азота – в
=2 раза, объем азота – в 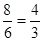 раза, объем кислорода – в
раза, объем кислорода – в 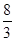 раза. Во столько же раз уменьшилось давление этих газов по сравнению с теми значениями, которые были до смешения. Находим парциальные давления газов в смеси:
раза. Во столько же раз уменьшилось давление этих газов по сравнению с теми значениями, которые были до смешения. Находим парциальные давления газов в смеси:
Р 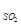 =720 мм. рт. ст. :2 = 360 мм. рт. ст.
=720 мм. рт. ст. :2 = 360 мм. рт. ст.
Р 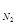 = 640 мм. рт. ст. :
= 640 мм. рт. ст. : 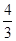 = 640 мм. рт. ст. ∙
= 640 мм. рт. ст. ∙ 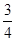 = 480 мм. рт. ст.
= 480 мм. рт. ст.
Р 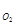 = 816 мм. рт. ст. :
= 816 мм. рт. ст. : 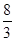 = 816 мм. рт. ст. ∙
= 816 мм. рт. ст. ∙ 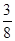 = 306 мм. рт. ст.
= 306 мм. рт. ст.
По закону парциальных давлений находим давление газовой смеси:
P (cмеси) = Р 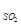 +P
+P 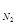 +P
+P 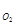 = 360+480+306 = 1146 мм. рт. ст.
= 360+480+306 = 1146 мм. рт. ст.
Ответ: Рсмеси = 1146 мм. рт. ст.
Закон эквивалентов
Эквивалент f 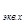 Х - некая реальная или условная частица вещества Х, которая может присоединять или высвобождать один ион водорода в кислотно-основных реакциях или один электрон в окислительно-восстановительных реакциях.
Х - некая реальная или условная частица вещества Х, которая может присоединять или высвобождать один ион водорода в кислотно-основных реакциях или один электрон в окислительно-восстановительных реакциях.
Фактор эквивалентности f 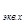 - число, показывающее какая доля реальной или условной частицы вещества Х эквивалентна одному иону водорода в кислотно-основных реакциях или одному электрону в окислительно-восстановительных реакциях.
- число, показывающее какая доля реальной или условной частицы вещества Х эквивалентна одному иону водорода в кислотно-основных реакциях или одному электрону в окислительно-восстановительных реакциях.
f 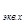 =
= 
 , где z- либо число ионов водорода, участвующих в реакции (для кислот); - либо число гидроксогрупп, участвующих в реакции (для оснований); - либо число ионов водорода, способных заместиться катионами, входящими в состав соли (для солей); - либо число, принятых или отданных электронов в окислительно-восстановительной реакции.
, где z- либо число ионов водорода, участвующих в реакции (для кислот); - либо число гидроксогрупп, участвующих в реакции (для оснований); - либо число ионов водорода, способных заместиться катионами, входящими в состав соли (для солей); - либо число, принятых или отданных электронов в окислительно-восстановительной реакции.
Эквивалент и фактор эквивалентности зависят от реакции, в которой участвует соединение.
H 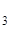 PO
PO 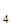 +3NaOH = Nа3PO
+3NaOH = Nа3PO 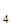 +3H
+3H  O – кислотно-основная реакция
O – кислотно-основная реакция
f 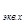 :
: 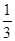

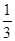
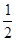 ;
;
H 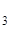 PO
PO 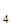 +2NaOH = Na
+2NaOH = Na  HPO
HPO 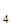 +2H
+2H  O – кислотно-основная реакция
O – кислотно-основная реакция
f 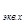 :
: 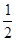

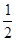
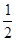 ;
;
H 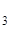 PO
PO 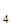 +NaOH = NaН2PO
+NaOH = NaН2PO 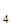 +H2O – кислотно-основная реакция
+H2O – кислотно-основная реакция
f 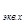 :
: 


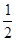 ;
;
Zn + 2HCl = ZnCl2 + H2 - окислительно-восстановительная реакция
f 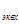 :
: 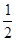

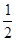
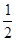
Zn – 2e =Zn 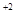 - окисление, Zn -восстановитель
- окисление, Zn -восстановитель
2H+1 +2e = H2 – восстановление, 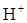 - окислитель;
- окислитель;
S + O2 = SO2 - окислительно-восстановительная реакция
f 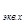 :
: 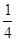
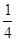
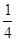
S – 4e = S 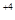 - окисление, S - восстановитель
- окисление, S - восстановитель
O2+ 4e = 2O 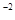 - восстановление,
- восстановление, 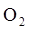 - окислитель.
- окислитель.
Молярный объем эквивалента вещества Х: V 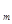 (
(  Х) – это объем одного моль эквивалента газообразного вещества Х: V
Х) – это объем одного моль эквивалента газообразного вещества Х: V 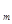 (
(  Х) =
Х) =  V
V 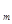 (Х).
(Х).
Молярная масса эквивалента вещества Х: М (  Х) – это масса одного моль эквивалента вещества Х, равная произведению фактора эквивалентности
Х) – это масса одного моль эквивалента вещества Х, равная произведению фактора эквивалентности  на молярную массу этого вещества: М (
на молярную массу этого вещества: М (  Х) =
Х) =  М (Х).
М (Х).
Количество вещества эквивалента n (  Х) – это число моль вещества эквивалента: n (
Х) – это число моль вещества эквивалента: n (  Х) =
Х) = 
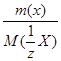 .
.
Закон эквивалентов: Вещества взаимодействуют друг с другом в строго эквивалентных количествах. n (  Х) = n (
Х) = n (  У)
У)
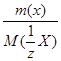 =
= 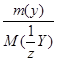 или
или 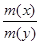 =
= 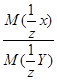 ,
,
где m(х), m(y) – массы взаимодействующих без остатка веществ;
M (  Х), M(
Х), M(  Y) –соответствующие молярные массы эквивалентов.
Y) –соответствующие молярные массы эквивалентов.
Для веществ, взаимодействующих в растворе, закон эквивалентов может иметь вид С (  Х) ∙V(Х) = С (
Х) ∙V(Х) = С (  Y) ∙V(Y),
Y) ∙V(Y),
где: С(  Х) – молярная концентрация эквивалента вещества Х; C(
Х) – молярная концентрация эквивалента вещества Х; C(  Y) – молярная концентрация эквивалента вещества Y; V(X), V(Y) – объемы соответствующих растворов.
Y) – молярная концентрация эквивалента вещества Y; V(X), V(Y) – объемы соответствующих растворов.
Пример 1. Вычислите молярную массу эквивалента серной кислоты в следующих реакциях: а) 8HJ + H2SO4 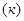 = 4J
= 4J 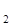 + H
+ H  S +4H
S +4H 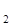 O;
O;
б) H 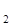 SO4+ 2NaOH = Na
SO4+ 2NaOH = Na 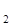 SO4 +2H
SO4 +2H 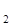 O.
O.
Решение: Молярная масса эквивалента серной кислоты рассчитывается по формуле M(  H
H  SO
SO 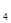 ) =
) =  М (H
М (H  SO
SO 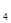 ), где z- либо число ионов водорода H
), где z- либо число ионов водорода H 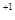 , участвующих в кислотно-основной реакции; - либо число электронов, участвующих в окислительно-восстановительной реакции.
, участвующих в кислотно-основной реакции; - либо число электронов, участвующих в окислительно-восстановительной реакции.
а) Реакция 8HJ + H2SO4 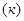 = 4J2+ H2S +4H2O относится к окислительно-восстановительным реакциям, т.к. в ходе реакции элементы меняют степень окисления.
= 4J2+ H2S +4H2O относится к окислительно-восстановительным реакциям, т.к. в ходе реакции элементы меняют степень окисления.
 4 2J
4 2J 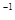 - 2e = J
- 2e = J  - окисление
- окисление
в-ль
S 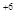 + 8e = S
+ 8e = S 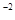 - восстановление
- восстановление
ок-ль
 |
8J 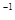 + S
+ S 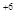 = 4 J
= 4 J  + S
+ S 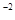
H2SO4 в данной реакции окислитель и фактор эквивалентности серной кислоты f 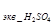
 =
= 

 =
= 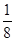 , где z- число электронов принятых окислителем в данной реакции. М (H2SO4) = 2+32+64 = 98 г/моль; M (
, где z- число электронов принятых окислителем в данной реакции. М (H2SO4) = 2+32+64 = 98 г/моль; M (  H2SO4) =
H2SO4) = 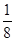 М (H2SO4) =
М (H2SO4) = 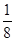 98 = 12,25 г/моль.
98 = 12,25 г/моль.
б) Реакция H 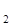 SO
SO 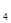 + 2NaOH = Na
+ 2NaOH = Na 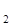 SO
SO 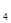 +2H
+2H 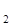 O относится к кислотно-основным реакциям (степени окисления элементов не изменяются).
O относится к кислотно-основным реакциям (степени окисления элементов не изменяются).
f 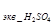
 =
= 

 =
= 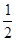 , где z- число ионов водорода Н+1 вступивших в реакцию.
, где z- число ионов водорода Н+1 вступивших в реакцию.
M (  H2SO4) =
H2SO4) = 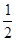 М (H2SO4) =
М (H2SO4) = 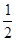 98 = 49 г/моль.
98 = 49 г/моль.
Ответ: а) М( 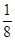 H2SO4) = 12,25 г/моль; б) М(
H2SO4) = 12,25 г/моль; б) М( 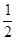 H2SO4) = 49 г/моль.
H2SO4) = 49 г/моль.
Пример 2. 0,604 г двухвалентного металла вытеснили из кислоты 581 мл водорода, собранного над водой при 18  С и давлении 105,6 кПа. Давление насыщенного водяного пара при 18
С и давлении 105,6 кПа. Давление насыщенного водяного пара при 18  С составляет 2,1 кПа. Найдите молярную массу эквивалента металла, укажите металл.
С составляет 2,1 кПа. Найдите молярную массу эквивалента металла, укажите металл.
Решение:
1 способ. Ме +2HCl = MeCl2+ H2
Me – 2e = Me 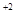 - окисление
- окисление
2Н 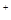 +2e=H2 - восстановление
+2e=H2 - восстановление
f 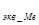 =
= 

 =
= 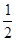 f
f 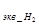 =
=  =
= 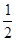
M ( 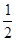 H2) =
H2) = 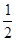 M (H2) =
M (H2) = 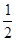 2
2 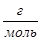 = 1
= 1 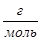
Используя уравнение Менделеева-Клапейрона, находим массу, выделившегося водорода:
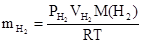
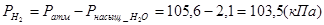
M( 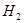 )=2 г/моль, V(
)=2 г/моль, V( 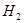 )=581мл=0,581л
)=581мл=0,581л
T=18 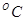 +273=291K
+273=291K
R=8,314 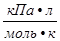
m( 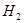 )=
)= 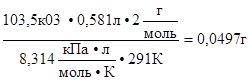
Исходя из закона эквивалентов 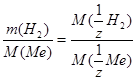 , рассчитываем молярную массу эквивалента металла М (
, рассчитываем молярную массу эквивалента металла М (  Ме) =
Ме) = 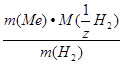 =
= 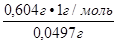 = =12,15г/моль. Зная, что металл двухвалентный находим молярную массу металла М (Ме) = z∙М (
= =12,15г/моль. Зная, что металл двухвалентный находим молярную массу металла М (Ме) = z∙М (  Ме) = 2∙12,15г/моль = 24,3г/моль.
Ме) = 2∙12,15г/моль = 24,3г/моль.
Ответ: искомый металл – магний Mg.
2 способ. Используя уравнение объединенного газового закона 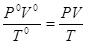 , находим объем выделившегося водорода при н.у. (Р
, находим объем выделившегося водорода при н.у. (Р  =101,3 кПа, T
=101,3 кПа, T  = 273 K):
= 273 K):
V  ( H
( H  ) =
) = 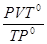 =
= 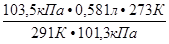 = 0,557л.
= 0,557л.
Согласно закону эквивалентов 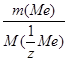 =
= 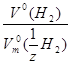 молярная масса эквивалента металла М (
молярная масса эквивалента металла М (  Ме) =
Ме) = 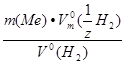 =
= 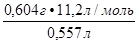 = 12,15г/моль, где V
= 12,15г/моль, где V 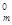 (
(  H
H  ) =
) =  V
V 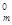 (H
(H  ) =
) = 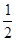 ∙22,4 л/моль = 11,2 л/моль.
∙22,4 л/моль = 11,2 л/моль.
Отсюда молярная масса металла М (Ме) = z∙М(  Ме) = 2∙12,15г/моль = =24,3г/моль.
Ме) = 2∙12,15г/моль = =24,3г/моль.
Ответ: Искомый металл – магний Mg.
Пример 3. При сжигании 1,635г цинка в струе кислорода получено 2,035г оксида цинка. Вычислите молярную массу эквивалента цинка.
Решение: Находим массу присоединенного кислорода
m(O) = m(ZnO) – m(Zn) = 2,035г – 1,635г = 0,4 г.
Согласно закону эквивалентов 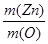 =
= 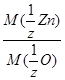 .
.
Зная, что М(  О) =
О) = 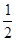 М(О) =
М(О) = 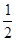 ∙16г/моль = 8 г/моль, находим молярную массу эквивалента цинка М(
∙16г/моль = 8 г/моль, находим молярную массу эквивалента цинка М(  Zn) =
Zn) = 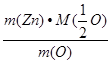 =
= 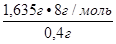 = 32,7 г/моль.
= 32,7 г/моль.
Ответ: М(  Zn) = 32,7 г/моль.
Zn) = 32,7 г/моль.
Пример 4. За 10 мин из раствора нитрата платины ток силой 5 А выделил 1,517г платины. Определите молярную массу эквивалента платины и степень окисления платины в исходной соли.
Решение: Количество электричества, прошедшее через раствор за 10 мин, находится по формуле Q = I∙t = 5А∙ 60∙10с = 3000 Кл.
При прохождении 96500 Кл электричества выделяется 1 моль эквивалентов платины. Находим молярную массу эквивалента платины.
При прохождении 3000 Кл выделилось 1,517 г Pt,
при прохождении 96500 Кл выделилось M(  Pt).
Pt).
M(  Pt) =
Pt) = 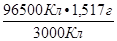 = 48,8 г/моль
= 48,8 г/моль
M(  Pt) =
Pt) =  ∙M(Pt)
∙M(Pt)
z = 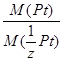 =
= 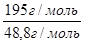 = 4
= 4
Степень окисления платины в исходной соли +4.
Ответ: М( 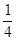 Pt) = 48,8 г/моль.
Pt) = 48,8 г/моль.
Контрольные вопросы:
1. Какие величины характеризуют газовое состояние вещества?
2. Каковы единицы измерения массы, объема, давления и температуры?
3. Что называется парциальным давлением газа? Как формулируется закон парциальных давлений Дальтона?
4. Что называется идеальным газом? При каких условиях газовые законы, выведенные для идеальных газов, могут быть без большой погрешности применены к реальным газам?
5. Если масса газа остается постоянной, какая зависимость существует между объемом, занимаемым данной массой газа, температурой и давлением?
6. Что называется универсальной газовой постоянной? Каков ее физический смысл? В каких единицах она измеряется?
7. Что называется абсолютной и относительной плотностью газа?
8. Какова зависимость между молекулярной массой газа и его относительной плотностью по водороду?
9. Что называется эквивалентом вещества? Что называется фактором эквивалентности вещества?
10. Является ли эквивалент постоянной характеристикой элемента?
12. Что называется моль вещества?
13. Перечислите методы определения молярной массы эквивалента.
14. Как вычислить молярную массу эквивалента сложного вещества (кислоты, основания, соли, оксида) в кислотно-основных реакциях?
15. Как вычислить фактор эквивалентности вещества, участвующего в окислительно-восстановительной реакции?
16. Дать формулировку закона эквивалентов и привести его математическое выражение.
Задания для самостоятельного решения:
1. Вычислить объем газа при нормальных условиях, если:
1. при 200С и 104,430 кПа объем газа равен 0,48 м 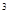 ;
;
2. при – 230С и 97,3 кПа объем газа равен 375 мл;
3. при 170С и 1,3 атм объем газа равен 1,1м 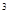 ;
;
4. при 910С и 98,65 кПа объем газа равен 608 мл;
5. при 250С и 102 425 Па объем газа равен 0,67 л;
6. при 300К и 101,3 кПа объем газа равен 1080 л;
7. при – 30С и 1,02 атм объем газа равен 320 м 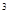 ;
;
8. при 150С и 81 313 Па объем газа равен 0,68 л;
9. при 250С и 85,3 кПа объем газа равен 820 мл;
10. при – 1000С и 100 000 Па объем газа равен 3 м 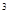 .
.
2. Вычислить массу газа:
1. при 800С и 98 642 Па 450 мл SO  ;
;
2. при 200С и 99,9 кПа 1л Ar;
3. при 900С и 101,3 кПа 0,25 л He;
4. при 650С и 78,5 кПа 300 мл СО;
5. при – 30С и 1 атм 1,2 л H  ;
;
6. при 26 К и 80,5 кПа 344 м 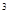 О
О  ;
;
7. при 00С и 102,320 кПа 15 л NH  ;
;
8. при 293 К и 1,7 атм 1л Cl  ;
;
9. при – 150С и 0,8 атм 500 л NO;
10. при 273 К и 8,11 МПа 20 л N  ;
;
11. при – 1200С и 100,3 кПа 0,5 л F 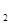 ;
;
12. при 500С и 1,12 атм 300 мл CH 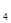 ;
;
13. при 303 К и 102 375 Па 1 м 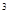 СО
СО  ;
;
14. при 173 К и 0,3 атм 250 мл N  O;
O;
15. при 298 К и 104,5 кПа 1,7 м 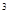 HCl.
HCl.
3. Определите парциальные давления газов в следующих смесях и общее давление газовых смесей:
Смешиваемые V, л P V  , л
, л
газы
1. N  0,5 105,3 кПа 3
0,5 105,3 кПа 3
H  2,5 93,7 кПа
2,5 93,7 кПа
2. СО  2 101,3 кПа 7,6
2 101,3 кПа 7,6
N  5,6 96,9 кПа
5,6 96,9 кПа
3. О  4 840 мм. рт. ст. 12
4 840 мм. рт. ст. 12
H  8 840 мм. рт. ст.
8 840 мм. рт. ст.
4. СО 4 750 мм. рт. ст. 3
СО  5 780 мм. рт. ст.
5 780 мм. рт. ст.
5. Ne 10 1 атм 5
Ar 2 1 атм
4. Рассчитать:
а) молярные массы эквивалентов веществ, участвующих в данных реакциях;
б) массу (или объем) продуктов реакции, если прореагировало указанное количество одного из веществ, при нормальных условиях.
| Номер варианта | Реакции | Количество (моль) исходного вещества |
K  СО СО 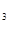 +2 H +2 H  PO PO 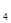 = 2КН = 2КН  РО РО 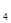 +Н +Н  О+СО О+СО  2Н 2Н  +О +О  = 2Н = 2Н  О О | 0,2 моль Н 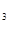 РО РО 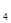 | |
К  СО СО  + H + H  PO PO 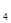 = K = K  HPO HPO 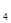 +H +H  O+CO O+CO  2SO 2SO  + O + O  = 2SO = 2SO  | 0,3 моль О  | |
СоCl  + 2NaOH = Co(OH) + 2NaOH = Co(OH)  + 2 NaCl 4 NH + 2 NaCl 4 NH  + 3O + 3O  = 2 N = 2 N  +6 H +6 H  O O | 0,5 моль NaOH | |
Аl(OH)  + 3H + 3H  SO SO 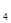 = Al(HSO = Al(HSO 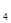 ) )  + 3H + 3H  O CO + H O CO + H  O = CO O = CO  + H + H  | 4 моль H  SO SO 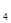 | |
FeCl  + 3NaOH = Fe(OH) + 3NaOH = Fe(OH)  + 3NaCl SO + 3NaCl SO  + 2 H + 2 H  = S + 2 H = S + 2 H  O O | 0,6 моль SO  | |
MnSO 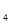 + 2 KOH = Mn(OH) + 2 KOH = Mn(OH)  + K + K  SO SO 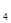 H H  + Cl + Cl  = 2 HCl = 2 HCl | 3 моль Cl  | |
К  СО СО  +2 HJ = H +2 HJ = H  CO CO  + 2 KJ Zn + 2 HJ = ZnJ + 2 KJ Zn + 2 HJ = ZnJ  + H + H  | 1,5 моль Zn | |
H  SO SO 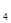 + 2 KOH = K + 2 KOH = K  SO SO 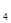 + 2 H + 2 H  O 2Al +6NaOH+6H O 2Al +6NaOH+6H  O=2Na O=2Na  [Al(OH) [Al(OH) 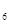 ]+ 3H ]+ 3H  | 0,2 моль Al | |
Cu(OH) 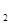 +HCl = CuOHCl + H +HCl = CuOHCl + H  O N O N  + О + О  = 2 NO = 2 NO | 5 моль N  | |
4 NH  + 5 O + 5 O  = 4 NO + 6 H = 4 NO + 6 H  O Bi(OH) O Bi(OH)  +3 HCl = BiCl +3 HCl = BiCl  + 3 H + 3 H  O O | 2 моль O 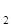 | |
3К  СО СО  +2H +2H  PO PO 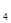 = 2K = 2K  PO PO 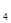 +3H +3H  O+3CO O+3CO  2 Mn + О 2 Mn + О  = 2 MnO = 2 MnO | 0,4 моль К  СО СО  | |
2 PbS + 3 О  = 2 PbO + 2 SO = 2 PbO + 2 SO  BaCl BaCl  + Na + Na  СО СО  = BaСО = BaСО  +2 NaCl +2 NaCl | 0.1 моль О 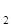 | |
Cu(OH)  + 2 HCl = CuCl + 2 HCl = CuCl  + 2 H + 2 H  O 2 C + О O 2 C + О  = 2 CO = 2 CO | 0,5 моль HCl | |
CuO + H  = Cu + H = Cu + H  O Na O Na  СО СО  + SiO + SiO  = Na = Na  SiO SiO  + CO + CO  | 3 моль CuO | |
2 ZnS +3 О  = 2 ZnO + 2 SO = 2 ZnO + 2 SO  Na Na  O + SiO O + SiO  = Na = Na  SiO SiO  | 0,75 моль О  |
5. Определите молярную массу эквивалента металла, если:
1. 0,162 г металла образуют 0,174 г его оксида;
2. при сгорании 1,5 г металла получилось 2,1 г оксида металла;
3. 1,4 г железа вытесняет из кислоты 0,05 г водорода;
4. 1,63 г цинка вытесняет из кислоты 0,05 г водорода;
5. 1,2 г магния вытесняет из кислоты 0,1 г водорода;
6. 0,9 г металла вытесняет из кислоты 0,1 г водорода;
7. 1,12 г кадмия вытеснили из кислоты 0,02 г водорода;
8. 1,2 г титана вытеснили из кислоты 0,075 г водорода;
9. 0,0873 г металла вытеснили из кислоты 35 мл водорода (н.у.);
10. 1 г металла вытесняет из кислоты 0,921 л водорода (н.у.);
11. 2 г металла соединяются с 1,39 г серы, M(  S)= 16 г/моль;
S)= 16 г/моль;
12. в оксиде свинца содержится 7,17 % кислорода по массе;
13. хлорид цинка содержит 47,9 % цинка по массе, M(  Cl) = 35,5 г/моль;
Cl) = 35,5 г/моль;
14. его соединение с йодом содержит 94,8 % йода по массе,
M(  J) = 126,9 г/моль;
J) = 126,9 г/моль;
15. его сульфид содержит 77,85 % металла по массе, M(  S)= 16 г/моль.
S)= 16 г/моль.
6. Определить металл и его молярную массу эквивалента, если:
1. 1,37 г двухвалентного металла вытесняют из кислоты 0,5 л водорода при 18  С и 101325 Па;
С и 101325 Па;
2. 0,00336 кг трехвалентного металла вытесняют из раствора щелочи 4,244 л водорода при 0  С и 99,8 кПа;
С и 99,8 кПа;
3. 2,2 г двухвалентного металла вытесняют из кислоты 0,81 л водорода при 22  С и 101,9 кПа;
С и 101,9 кПа;
4. 1,2 г металла вытесняют из раствора кислоты при 20  С и 101100 Па 442 мл водорода;
С и 101100 Па 442 мл водорода;
5. 0,527 г металла вытесняют из кислоты 0,2 дм 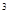 водорода, измеренного при 18
водорода, измеренного при 18  С и 98 658,5 Па;
С и 98 658,5 Па;
6. при нагревании 4,3 г оксида металла было получено 0,58 дм 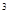 кислорода (при 17
кислорода (при 17  С и 113,324 кПа);
С и 113,324 кПа);
7. 0,5 г металла вытесняют из раствора кислоты 198 мл водорода, собранного и измеренного над водой при 298 К и 99,3 кПа. Давление насыщенного пара воды при данной температуре составляет 23,5 кПа;
8. 13,43 г двухвалентного металла вытесняют из раствора кислоты 5 л водорода, собранного и измеренного при температуре 291 К и 101,3 кПа. Давление насыщенного пара воды при данной температуре составляет 2,07 кПа;
9. при электролизе расплава хлорида металла (ток силой 5А, время процесса 10 мин) было выделено 0,378 г металла;
10. для выделения 1,97 г которого из раствора его соли потребовалось пропускать в течение 36 мин ток силой 3А. Валентность металла равна двум;
11. выделение 0,16 г металла при электролизе раствора его соли потребовало пропускания тока силой 1,8 А в течение 11,8 мин;
12. при пропускании через раствор его соли тока силой 2 А в течение 3 ч выделилось 12,56 г металла;
13. для выделения 2,57 г металла через раствор его соли был пропущен ток силой 3,6 А в течение 30 мин. Валентность металла равна трем;
14. ток силой 2,5 А в течение 15 мин выделяет из раствора соли 0,46 г металла;
15. ток силой 5 А в течение 20 мин выделяет из раствора соли 6,441 г металла.
