Краткие теоретические сведения. Высокочастотное титрование – вариант бесконтактного кондуктометрического метода анализа, в котором анализируемый раствор подвергают действию электрического
Высокочастотное титрование – вариант бесконтактного кондуктометрического метода анализа, в котором анализируемый раствор подвергают действию электрического поля высокой частоты (порядка нескольких мегагерц). При таких частотах в растворе начинают играть роль эффекты молекулярной, или деформационной, и ориентационной поляризации. Под действием электрического поля электроны любой молекулы будут оттягиваться в сторону поглотительного электрода, а ядра – в сторону отрицательного электрода. Это явление получило название молекулярной или деформационной поляризации. Полярные молекулы в электрическом поле обладают также ориентационной поляризацией, стремящейся ориентировать дипольные молекулы вдоль поля. В результате таких поляризационных эффектов возникают кратковременные токи, изменяющие электропроводность, диэлектрические свойства и магнитную проницаемость растворов. Измеряемая в этих условиях полная электропроводность высокочастотной кондуктометрической ячейки λ складывается из активной составляющей λакт – истинной проводимости раствора и реактивной составляющей λреакт – мнимой электропроводности, зависящей от частоты и типа ячейки:
λ = λакт + 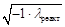 .
.
Высокочастотное титрование проводят в электролитических ячейках, в которых исследуемый электролит не имеет прямого контакта с электродами и связан с измерительной цепью индуктивно или через емкость.
Бесконтактные электролитические ячейки, используемые для высокочастотного титрования, могут быть двух типов (рис. 19).
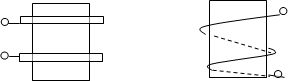 |
а) б)
Рис. 19. Ячейки для высокочастотного титрования: а – ёмкостная (С-ячейка); б – индуктивная (L-ячейка)
С-ячейки применяют для анализа растворов с низкой электропроводностью, L-ячейки применяют для анализа растворов с высокой электропроводностью.
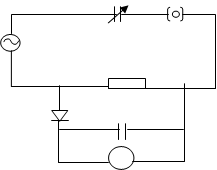
В лабораторной практике используют высокочастотные титраторы марки ТВ-6Л1 с емкостной ячейкой (рис. 20).
 2 3
2 3
мкА
Рис. 20. Блок-схема высокочастотного титратора ТВ-6Л1: 1 – генератор высокой частоты; 2 – регулируемый конденсатор; 3 – емкостная ячейка; 4 – образцовый резистор; 5 – выпрямительный диод; 6 – конденсатор-фильтр; 7 – микроамперметр
Р а б о т а 19
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ЖЕЛЕЗА (III)
В РАСТВОРЕ МЕТОДОМ ВЫСОКОЧАСТОТНОГО
ТИТРОВАНИЯ
1. Цель работы: получить общие сведения о высокочастотном титровании, практически ознакомиться с реакциями комплексообразования в методе высокочастотного титрования; определить содержание железа (III) в исследуемом растворе.
Сущность метода
В определении железа (III) лежит реакция комплексообразования. В качестве титранта применяют этилендиаминтетраацетат натрия (ЭДТА – трилон Б – комплексон III) Na2H2Y.
При титровании ионов Fe3+ раствором ЭДТА протекает реакция
Fe3+ + Na2H2Y = NaFeY + 2H+ + Na+
Ионы Fe3+ образуют устойчивые комплексные соединения с трилоном Б при рН = 2-3 и могут быть определены методом высокочастотного титрования.
На кривой титрования наблюдается два излома: первый соответствует количественному связыванию ионов Fe3+ комплексоном, второй указывает на завершение кислотно-основного взаимодействия.
Приборы и реактивы
1) Приборы: титратор высокочастотный лабораторный ТВ-6Л1, стержень-мешалка, пинцет, фильтры беззольные бумажные «синяя лента»; 2) посуда стеклянная:микробюретка вместимостью 5 см3, пипетка Мора вместимостью 5 см3, стакан химический для титрования вместимостью 100 см3, воронка стеклянная; 3) растворы: трилон Б с молярной концентрацией эквивалентов c[(1/2) Na2H2Y] = 0,1 моль/дм3, раствор, содержащий ионы Fe3+.
Алгоритм определения
Из мерной колбы отбирают пипеткой Мора 5 см3 исследуемого раствора в стакан для титрования. Сухой снаружи стакан помещают в ячейку, доливают дистиллированную воду на 3-5 мм выше верхнего электрода датчика.
Заполняют микробюретку 0,01 Н раствором трилона Б. Опускают в стакан стержень-мешалку, переводят тумблер «Мешалка» в положение «Включено» и ручкой «Перемешивание» регулируют скорость вращения. Ручками «Грубо» и «Точно» устанавливают стрелку прибора на 30 - 40 делений.
Записывают первоначальное показание прибора. Затем порциями по 0,2 см3 прибавляют из микробюретки раствор титранта в стакан для титрования, записывая показания прибора после внесения каждой порции раствора. Экспериментальные данные заносят в табл. 28.
Титрование продолжают, пока не будут получены 8 - 10 измерений после максимального значения. По полученным данным строят кривую титрования «сила тока – объем титранта» I = f [V(Na2H2Y)]. По излому на кривой (рис. 21) определяют объем трилона Б Vэ(Na2H2Y), см3, затраченный на титрование ионов Fe3+.
За результат анализа принимают среднее арифметическое двух параллельных определений.
Таблица 28
