- Сутек, табиғатта кездесуі, жалпы сипаттамасы. Алу тәсілдері мен қолданылуын сипаттаңыз
- Сутектің физикалық және химиялық қасиеттерін сипаттаңыз
- Гидридтер, физикалық және химиялық қасиеттері, қолданылуын сипаттаңыз
- Су, агрегаттық күйі, табиғатта кездесуі, құрылымы, қолданылуын сипаттаңыз
- Сутек пероксиді, физикалық және химиялық қасиеттері, қолданылуын сипаттаңыз
- Оттек, табиғатта кездесуі, жалпы сипаттамасы. Алу тәсілдері мен қолданылуын сипаттаңыз
- Оксидтер, физикалық және химиялық қасиеттерін сипаттаңыз
- Пероксидтер, супероксидтер, озонидтерді сипаттаңыз
- Күкірттің табиғатта кездесуі, жалпы сипаттамасы. Алу тәсілдері мен қолданылуын сипаттаңыз
- Фтордың физикалық және химиялық қасиеттерін сипаттаңыз
- Хлордың физикалық және химиялық қасиеттерін сипаттаңыз
- Хлорсутек және хлоридтер, химиялық қасиеттері, қолданылуын сипаттаңыз
- Хлордың оксидтері, химиялық қасиеттерін сипаттаңыз
- Хлордың оттекті қышқылдары және олардың тұздары, қоданылуын сипаттаңыз
- Бром топшасы элементтерінің физикалық және химиялық қасиеттерін сипаттаңыз
- Бром топшасы элементтерінің оттекті қышқылдары және олардың тұздары, химиялық қасиеттерін сипаттаңыз
- Фтор мен хлордың табиғатта кездесуі, жалпы сипаттамасы. Алу тәсілдері мен қолданылуын сипаттаңыз
- Күкірттің табиғатта кездесуі, жалпы сипаттамасы. Алу тәсілдері мен қолданылуын сипаттаңыз
- Күкірттің физикалық және химиялық қасиеттерін сипаттаңыз
- Күкірттің оттекті қышқылдары және олардың тұздары, химиялық қасиеттерін сипаттаңыз
- Селен топшасы элементтерінің галогенидтері және олардың туындылары, химиялық қасиеттерін сипаттаңыз
- Азоттың сутекті қосылыстары және олардың туындылары, химиялық қасиеттері. Алу тәсілдері мен қолданылуын түсіндіріңіз
- Азоттың оттекті қышқылдары және олардың тұздары, химиялық қасиеттері. Алу тәсілдері, қолданылуын түсіндіріңіз
- Фосфор, табиғатта кездесуі, жалпы сипаттамасы. Алу тәсілдері, қолданылуын түсіндіріңіз
- Фосфордың оксидтері және сульфидтері, химиялық қасиеттері. Алу тәсілдері, қолданылуын түсіндіріңіз
- Фосфор қышқылдары, химиялық қасиеттері. Алу тәсілдері, қолданылуын түсіндіріңіз
- Мышьяк топшасы элементтерінің оттекті қосылыстары және гидроксидтері, химиялық қасиеттері. Алу тәсілдерін түсіндіріңіз
- Көміртектің оксидтері, химиялық қасиеттері. Алу тәсілдерін түсіндіріңіз
- Көмір қышқылы, оның тұздары және туындылары, химиялық қасиеттері. Алу тәсілдері, қолданылуын түсіндіріңіз
- Кремнийдің физикалық және химиялық қасиеттерін түсіндіріңіз
- Кремнийдің оксидтері және қышқылдары, тұздары, химиялық қасиеттері. Алу тәсілдері мен қолданылуын түсіндіріңіз
- Германий топшасы элементтерінің оксидтері, физикалық және химиялық қасиеттері. Қорғасынды аккумулятордың жұмысын түсіндіріңіз
- Борандар және тетрагиридобораттар, химиялық қасиеттерін түсіндіріңіз
- Бор оксиді, бор қышқылдары және бораттар, химиялық қасиеттері, қолданылуын түсіндіріңіз
- Алюминийдің физикалық және химиялық қасиеттерін түсіндіріңіз
- Алюминий оксиді, гидроксиді және тұздары, химиялық қасиеттері, қолданылуын түсіндіріңіз
- Сілтілік және сілтілікжер элементтерінің табиғатта кездесуі, оларды өндірісте алу жолдарын түсіндіріңіз
- Сілтілік және сілтілікжер элементтерінің оксидтері мен гидроксидтері, физикалық және химиялық қасиеттері, алынуы, қолданылуын түсіндіріңіз
- Сілтілік және сілтілікжер элементтерінің тұздары, табиғатта кездесуі, алынуы, қолданылуын түсіндіріңіз
| V1 | Қышқылдар (HClO, HClO3,HClO4) ангидридтері |
| | Cl2O |
| | Cl2O7 |
| | Cl2O5 |
| V1 | Йод әрекеттеседі: |
| | конц. HNO3 |
| | конц. H2SO4 |
| | H2O |
| V1 | Суда аз еритін қосылыс: |
| | күміс хлориді; |
| | күміс бромиді; |
| | күміс иодиді; |
| V1 | Қосылыстардағы галогендердің тотығу дәрежелері (F-дан басқа): |
| | -1; |
| | +1; |
| | +5; |
| V1 | Mn- Tc – Re жай заттар қатарының |
| | жалпы химиялық активтілігі төмендейді; |
| | сұйытылған күкірт және тұз қышқылымен тек қана Mn әрекеттеседі; |
| | кернеу қатарында барлық металдар сутекке дейін орналасқан; |
| V1 | Фтор: |
| | атомның электрондық конфигурациясы 1s22s22p5; |
| | р-элемент; |
| | электртерістілігі ең күшті элемент; |
| V1 | F2 – Cl2 – Br2 – J2 қатарындағы |
| | ең берік молекула Cl2 |
| | тотықсыздандырғыштық активтігі жоғарылайды; |
| | тек қана F2 суды тотықтырады; |
| V1 | Cl2 –ды әрекеттестіру арқылы алуға болады: |
| | MnO2 + HCl (конц.)→ |
| | KMnO4 + HCl (конц.)→ |
| | K2Cr2O7 + HCl (конц.)→ |
| V1 | HF – HCl – HBr – HJ қатарында |
| | молекула беріктігі төмендейді; |
| | тотықсыздандырғыш қасиеті күшейеді; |
| | тек қана балқытқыш қышқыл қышқылдық тұз түзеді; |
| | |
| V1 | Хлор сілтімен (KOH) әрекеттескенде түзілуі мүмкін: |
| | калий гипохлориті; |
| | калий хлораты; |
| | калий хлориді; |
| V1 | Жағдайға байланысты HClO –ның айырылу теңдеулері: |
| | HClO → HCl + O; |
| | HClO → Cl2O + H2O; |
| | HClO → HClO3 +HCl; |
| V1 | HClO–HСlO2 – HСlO3- HClO4 қышқылдар қатарында: |
| | қышқылдық қасиеттері күшейеді; |
| | молекуланың тұрақтылығы жоғарылайды; |
| | тотықтырғыштық активтігі төмендейді; |
| V1 | Хлорлы қышқылдың қасиеті: |
| | түссіз, ауада түтінденетін сұйық; |
| | оңай ыдырайды; |
| | ең күшті минералдық қышқыл; |
| V1 | Натрий гипохлоритімен Ni(OH)2 тотығу өнімі: |
| | NiO(OH); |
| | NaCl; |
| | H2O; |
| V1 | Калий манганаты (VI) этил спиртімен әрекеттескенде түзіледі: |
| | марганец (1V) оксиді; |
| | CH3COH; |
| | KOH; |
| V1 | Платиналық металдарға жатады: |
| | Rh; |
| | Pd; |
| | Pt; |
| V1 | Калий перманганаты мен натрий сульфитінің қышқылдық ортада (H2SO4) ерітіндісімен әрекеттескенде түзілетін өнімдер: |
| | калий сульфаты; |
| | марганец (II) cульфаты; |
| | натрий сульфаты; |
| V1 | Калий перманганатын термиялық айыруда түзілетін өнім: |
| | калий манганаты; |
| | марганец (IV) оксиді; |
| | O2; |
| V1 | Тотығу дәрежесі жоғары фосфор қышқылдары: |
| | H3PO4; |
| | HPO3; |
| | H4P2O7; |
| V1 | Галогендердің реттік нөмірі артқан сайын : |
| | атомдық радиустары артады; |
| | бейметалдық қасиеті төмендейді; |
| | тотықтырғыштық қабілеті төмендейді; |
| V1 | Хлор әгі … |
| | хлорид пен кальций гипохлоритінің қоспасы; |
| | формуласы - CaOCl2; |
| | күшті тотықтырғыш; |
| V1 | Иодсутек пен азотты қышқыл әрекеттескенде түзіледі: |
| | азот (II) оксиді; |
| | J2; |
| | су; |
| V1 | Күкірттің аллотропиялық түр өзгерістері: |
| | ромбалық күкірт - S8; |
| | моноклиндік күкірт - S8; |
| | пластикалық күкірт - S∞; |
| V1 | Сульфандар – бұл… |
| | көпкүкіртті сутекті қосылыс; |
| | H2S3; |
| | H2S5; |
| V1 | Натрий дисульфиді тұз қышқылымен әрекеттескенде түзіледі: |
| | натрий хлориді; |
| | күкіртті сутек; |
| | бос күкірт; |
| V1 | Өндірістік жағдайда SO2 – нің SO3 –ке тотығуының негізгі әдістері: |
| | нитрозды, NO2-ні қолданады; |
| | контактты: tº = 400-600º C; катализатор. |
| | контактты:tº = 400-600º C; катализаторсыз. |
| V1 | Күкірт пероксоқышқылдары: |
| | H2SO5; |
| | H2S2O8; |
| | Қышқылдар және олардың тұздары – күшті тотықтырғыш; |
| V1 | VI–А негізі топ эленттерінің жоғарыдан төмен қарай |
| | атом радиустары артады; |
| | металдық қасиеттері күшейеді; |
| | төменгі оң тотығу дәрежесіндегі қосылыстарының тұрақтылығы артады; |
| V1 | Хлорлы, хлорлылау және күкіртті қышқылдардың тұздарының атауы: |
| | хлориттер; |
| | хлораттар; |
| | сульфиттер; |
| V1 | Суда жақсы ериді: |
| | Na2S; |
| | CaS; |
| | BaS; |
| V1 | Тұз қышқылында ериді: |
| | FeS; |
| | MnS; |
| | ZnS; |
| V1 | Күкірт, селен және теллур оксидтері: |
| | SO3; |
| | SeO2; |
| | TeO2; |
| V1 | Күшті қышқылдар: |
| | күкірт; |
| | селенді; |
| | бромдысутек; |
| V1 | Күкіртсутек - |
| | жағымсыз иісі бар газ; |
| | өте улы; |
| | күшті тотықсыздандырғыш; |
| V1 | H2S тотыққанда түзілетін өнім болуы мүмкін: |
| | S |
| | SO2 |
| | H2SO4 |
| V1 | Күкіртсутек қышқылы: |
| | әлсіз қышқыл; |
| | күшті тотықсыздандырғыш; |
| | 2 қатарда тұз түзеді: қышқылдық және орта; |
| V1 | Пирит: |
| | оны SO2 –ні жағу арқылы алады ; |
| | сутек дисульфид тұзы; |
| | темірдің тотығу дәрежесі: +4 |
| V1 | Калий нитритін калий дихроматының қышқыл (H2SO4) ерітіндісінде әрекеттескендіргенде түзіледі: |
| | калий нитраты; |
| | хром (III) сульфаты; |
| | калий сульфаты; |
| V1 | Сутек - … |
| | ең жеңіл газ; |
| | суда аз ериді; |
| | қосылыстарда көрсететін тотығу дәрежесі: +1 және -1 |
| V1 | Галогендердің физикалық қасиеттері: |
| | хлор – оңай сығылатын газ; |
| | бром – сұйық; |
| | йод – қатты зат; |
| V1 | Әлсіз қышқыл: |
| | селенді; |
| | теллурлы; |
| | ортофосфор; |
| V1 | Қосылыстарда күкірттің тотығу дәрежесі: |
| | -2; |
| | +4; |
| | +6; |
| V1 | Олеумның құрамында бар: |
| | H2S2O7; |
| | H2S3O10; |
| | H2S4O13; |
| V1 | -S-S-S- гомотізбегі мына қосылыстарда кездеседі: |
| | сульфандарда; |
| | полисульфидтерде; |
| | политион қышқылдарында; |
| V1 | Аллотропты модификация түзуші элемент: |
| | фосфор; |
| | күкірт; |
| | оттек; |
| V1 | Күкірт атомының тотығу дәрежесі төмен болатын қосылыстар: |
| | Na2S; |
| | BaS; |
| | SnS; |
| V1 | Калий перманганаты калий сульфитімен сілтілік (KOH) ортада әрекеттескенде түзіледі: |
| | калий сульфаты; |
| | калий манганаты; |
| | су; |
| V1 | Концентрлі күкірт қышқылы тотықсызданғанда түзіледі: |
| | SO2; |
| | H2S; |
| | S; |
| V1 | Күкірт қышқылы – |
| | күшті қышқыл; |
| | ылғал тартқыштық қасиеті бар; |
| | тек қана сұйытылған күйде тотықтырғыш қасиет көрсетеді; |
| V1 | Балқытқыш қышқыл -.. |
| | күші орташа қышқыл; |
| | шынымен әрекеттеседі; |
| | әлсіз қышқыл; |
| V1 | Аммоний дихроматын термиялық айыруда түзіледі: |
| | хром (III) оксиді; |
| | азот; |
| | су; |
| V1 | Азотты-сутек қоспасынан аммиакты алу үдерісі - … |
| | қайтымды үдеріс; |
| | экзотермиялық; |
| | гетерогенді-катализдік; |
| V1 | Төменгі азоттың тотығу дәрежесі: |
| | Аммиак; |
| | аммоний сульфаты; |
| | аммоний хлориді; |
| V1 | S → Se → Te → Po қатарында: |
| | тотықтырғыштық қасиет төмендейді; |
| | тотықсыздандарғыштық қабілеті күшейеді; |
| | металдық сипаты жоғарылайды; |
| V1 | Элементтік күкірт төмендегідей реакцияға түсуге қабілетті: |
| | тотығу; |
| | тотықсыздану; |
| | диспропорциялану; |
| V1 | Фосфордың аллотропиялық түр өзгерістері: |
| | ақ фосфор; |
| | қызыл фосфор; |
| | қара фосфор; |
| V1 | Хлордың оттекті қышқылдары: |
| | HClO; |
| | HClO3; |
| | HClO4; |
| V1 | Калий перманганаты қышқылдық (H2SO4) ортада күкіртті сутекпен әрекеттескенде түзіледі: |
| | марганец (II) cульфаты; |
| | калий сульфаты; |
| | күкірт; |
| V1 | Күкірт қышқылы қолданылады: |
| | мұнайды тазартуда; |
| | тыңайтқыш өндірісінде; |
| | қопарылғыш заттар өндірісінде; |
| V1 | Күкірттің қосылыстарда көрсететін тотығу дәрежелері: |
| | -2-ден +6-ға дейін; |
| | +4; |
| | +6; |
| V1 | Купорос: |
| | FeSO4∙ 7 H2O; |
| | CuSO4∙5 H2O; |
| | ZnSO4∙ 7H2O; |
| V1 | SO2 түзетін реакциялар: |
| | S + O2 → |
| | S +H2SO4(конц.) → |
| | Ag + H2SO4 (конц.) → |
| V1 | Гидролизі қайтымсыз, аяғына дейін жүретін сульфидтер: |
| | Al2S3; |
| | Cr2S3; |
| | Fe2S3; |
| V1 | Металл сульфидін алуға болады: |
| | Алмасу реакциясы арқылы; |
| | жай заттардан; |
| | көміртекті қыздыру арқылы сульфатты тотықсыздандыру; |
| V2 | Жер қыртысында ең көп таралатын элементтер |
| | Оттек |
| | Кремний |
| | Темір |
| V2 | 8 электрондық ішкі қабаты бар атомдар немесе иондар: |
| | С-4 |
| | N-3 |
| | V+5 |
| V2 | Кремнийді қайсысында ерітуге болады? |
| | HF+HNO3қоспасында |
| | Ұзақ уақыт бойы су буымен |
| | КОН |
| V2 | SiO2 құрамды жартылай асыл тастар |
| | Сутас (Горный хрусталь) |
| | Жылтыр тас (Опал) |
| | Яшма |
| V2 | Екідайлы қасиет көрсететін электролиттер |
| | Al(OH)3 |
| | Zn(OH)2 |
| | Cr(OH)3 |
| V2 | Әлсіз электролиттер |
| | NH4 OH |
| | H2 CO3 |
| | Al(OH)3 |
| V2 | Төменде келтірілген қышқылдардың ең күштілері |
| | HNO3 |
| | H 2SO4 |
| | НСlO4 |
| V2 | IVA топшасының элементтеріне тән тотығу дәрежелері |
| | +4 |
| | +2 |
| | -4 |
| V2 | IVВ топшасының элементтеріне тән тотығу дәрежелері |
| | +4 |
| | +2 |
| | -4 |
| V2 | VВ топшасының элементтеріне тән тотығу дәрежелері |
| | +3 |
| | -3 |
| | +5 |
| | +1 |
| | -1 |
| | |
| | +2 |
| | -2 |
| V2 | VA топшасының элементтеріне тән тотығу дәрежелері |
| | +3 |
| | -3 |
| | +5 |
| V2 | IІІA топшасының элементтеріне тән тотығу дәрежелері |
| | +3 |
| | +1 |
| | +2 |
| V2 | IІІ В топшасының элементтеріне тән тотығу дәрежелері |
| | +3 |
| | +1 |
| | +2 |
| V2 | Қай металдарды концентрлі күкірт қышқылы пассивтендіреді |
| | Al |
| | Cr |
| | Fe |
| V2 | Гидразин – бұл .... |
| | Бифункциональдық негіз |
| | Сілтілік ерітінділердегі күшті тотықсыздандырғыш |
| | Ауа құрамындағы оттекте оңай тотығатын азот бар қосылыс |
| V2 | Азоттың табиғатта бос күйінде кездесетін қосылыстары |
| | NH3 |
| | NO2 |
| | N 2O5 |
| V2 | Төмен температураларда сұйытылған азот қышқылымен әрекеттесетін металдар |
| | Mg |
| | Cu |
| | Zn |
| V2 | Мына N2+ 3H2 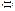 2NH3+ Q реакция бойынша аммиактың шығымын жоғарылатуға әсер ететін дәйектер 2NH3+ Q реакция бойынша аммиактың шығымын жоғарылатуға әсер ететін дәйектер |
| | Температура |
| | Қысым |
| | Өршіткі |
| V2 | Күкірт молекуласының қалыпты жағдайдағы және 800оС-ден 1000оС-ге дейін қыздыру кезіндегі құрамы |
| | S |
| | S2 |
| | S8 |
| V2 | Табиғатта халькогендер әдетте мына қосылыстар түрінде кездеседі: |
| | оксидтер ЭО2 |
| | FeS2 |
| | хлоридтер ЭСl2 |
| V2 | Кеңістікте құрылымы тетраэдр болып келетін, фосфор элементімен полимерлі бинарлы қосылыс түзе алатын элементтер |
| | O |
| | N |
| | S |
| V2 | СО2 -ны зертханада алу реакциясы |
| | MgСО3 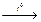 |
| | СаСО3+ HCl 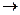 |
| | MgСО3+ HCl 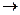 |
| V2 | Көміртектің тотықсыздандырғыштық қасиет көрсететін қосылыстары |
| | CO |
| | НСООН |
| | КСN |
| V2 | Силан, силицид, германидтің химиялық формулалары |
| | Cа2Si |
| | SiH4 |
| | Mg2Ge |
| V2 | Кремний және германий диоксидтері - бұл.... |
| | Ақ түсті заттар |
| | Кристалдық заттар |
| | Көптеген полиаморфтық модификацияларға ие заттар |
| V2 | Сулы ерітіндіде бор элементі келесі қосылыстар түрінде бола алады.... |
| | B(ОН) 3 |
| | (В4О7)2- құрамды оксоиондар |
| | B(ОН)4- |
| V2 | SiO2 –ны ерітетін заттар |
| | HF |
| | КОНсұйық |
| | Na2CO3 балқыма |
| V2 | Төменде келтірілген бинарлы қосылыстардың қайсысын боридтар деп атауға болады |
| | Mg3B2 |
| | Ве4В |
| | TiB |
| V2 | Борды қыздырғанда мына заттармен әрекеттеседі: |
| | S |
| | N2 |
| | C |
| V2 | Көміртек мен концентрлі азот қышқылының әрекеттесуі барысында мына зат бөлінеді. |
| | су |
| | Көміртек диоксиді |
| | Азот диоксиді |
| V2 | AgNO3 + H3PO2+ H2O 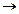 реакциясы барысында мыналар бөлінеді реакциясы барысында мыналар бөлінеді |
| | Ag |
| | H3PO4 |
| | HNO3 |
| V2 | Конденсирленген фосфаттарының құрылымы мынадай болуы мүмкін |
| | Тізбекті құрылымды |
| | Циклдық құрылымды |
| | Аралас құрылымды |
| V2 | "Ақ күшән" – бұл ... зат |
| | As2 O3құрамды |
| | Ақ түсті |
| | Суда нашар еритін |
| V2 | Алюминийдің сұйытылған азот қышқылымен қыздыру кезінде әрекеттесуі барысында мыналар түзіледі. |
| | Алюминий нитраты |
| | Аммоний нитраты |
| | Су |
| V2 | Бураның "Қанатшалары" - бұл: |
| | Ауыр металдардың полиметабораттары |
| | Алуан түрлі түстерге ие заттар |
| | Аналитикалық практикада d-элементтерді анықтау үшін қолданылады |
| V2 | ns2 (n-1)d3 электрондық конфигурацияға тән атомдар |
| | V |
| | Nb |
| | Ta |
| V2 | ns2(n-1)d2 электрондық конфигурацияға тән атомдар |
| | Ti |
| | Zr |
| | Hf |
| V2 | ns2(n-1)d1 электрондық конфигурацияға тән атомдар |
| | Sc |
| | Y |
| | La |
| V2 | Қыздыру кезінде азот бөлетін заттар |
| | (NH4)2 Cr2 O7 |
| | NH4 NO2 |
| | N2H4+ KMnO4 |
| V2 | Сумен әрекеттестіру арқылы қыздыру кезінде аммиак бөлетін заттар |
| | Li3N |
| | Mg3N2 |
| | Cl3N |
| V2 | NO алуға болатын реакция теңдеулері |
| | Cu + HNO3сұй 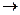 |
| | NH3+ O2 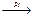 (өршіткі қатысында) (өршіткі қатысында) |
| | HNO2 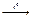 (қыздыру және жарық түсіру) (қыздыру және жарық түсіру) |
| V2 | NO2 алуға болатын реакция теңдеулері |
| | Cu + HNO5конц 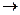 |
| | N2 O3 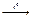 |
| | HNO3 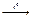 (қыздыру және жарық түсіру) (қыздыру және жарық түсіру) |
| V2 | Концентрлі азот қышқылы қандай металдарды пассивтендіреді |
| | Al |
| | Cr |
| | Fe |
| V2 | Фосфинді РН3алудың мүмкін болатын реакциялары |
| | Pақ+ KOHконц 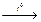 |
| | Mg3P2+H2O= |
| | Ca3P2+ HCl 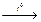 |
| V2 | Р2О5ыстық суда еріткенде түзілетін қышқылдар |
| | H3(PO3)3 |
| | H3 PO4 |
| | H4 P2O7 |
| V2 | Фосфордың маңызды тыңайтқыштарына жатады |
| | Суперфосфат |
| | Қос суперфосфат |
| | Преципитат |
| V2 | Фосфордың биологиялық жүйелердегі маңызы қандай? |
| | Р-О-Р фосфатты топтар РНҚ құрамына кіреді |
| | Р-О-Р фосфатты топтар ДНҚ құрамына кіреді |
| | Фосфор қосылыстары биогенді заттарға жатады, ал фосфор -биогенді элемент |
| V2 | Көміртек – шексіз көп органикалық қосылыстарды түзуге бейім. Оның себебі мынада,.... |
| | С-С байланысы осы топша элементтерінің екі атомы арасындағы байлансықа қарағанда әлдеқайда берік |
| | Көміртек атомының гибридтелуге қабілеті жоғары |
| | Көміртек атомының кіші мөлшеріне байланысты оның қатысымен түзілетін байланыстар аса берік |
| V2 | Минералдық тыңайтқыштар былай жіктеледі.... |
| | жай |
| | Күрделі |
| | Аралас |
| V2 | С-Si-Ge-Sn-Pb қатарында бейметаллдық қасиеттердің металдыққа ауысуы анық байқалғанымен, бұл бағытта элементтердің қасиеттері бірқалыпты өзгермейді. Атап айтсақ.... |
| | Көміртектен қалайыға қарай иондану энергиясы кемиді, бірақ қорғасында сәл артады |
| | Көміртектің балқу температурасы максималды, кремнийде 2 есе кемиді, кейін германий мен қалайыда төмендейді де, қорғасында сәл артады |
| | Топ номеріне сәйкес келетін валенттік (4) көміртек мен кремнийге тән және оның ролі қалайы мен қорғасынға қарай төмендейді (В=2) |
| V2 | Қыздыру кезінде кремний мынадай заттармен әрекеттеседі... |
| | NaOHконц |
| | Mg |
| | HNO3+ HF |
| V2 | Көміртектің аллотроптық түрөзгерістері |
| | Алмас |
| | Графит |
| | Карбин |
| V2 | Германий кремнийге ұқсас, бірақ көміртектен өте ерекшеленеді, атап айтсақ... |
| | Кристаллдық германий атомдары sp3 –гибридтелген алмас құрылымына ие |
| | Германийдін электрөткізгіштігі топшаның алдынғы элементтеріне қарағанда аса жоғары |
| | Бөлме температурасында германий жартылайөткізгіш болып табылады |
| V2 | Бос күйінде борды алудың химиялық реакция теңдеулері |
| | B2 O3+ Mg 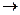 |
| | ВI3 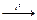 |
| | B2H6 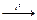 |
| V2 | Қалыпты жағдайда борды ерітетін қышқылдар |
| | H2 SO4 сұйыт. |
| | HNO3 |
| | НСl+3 HNO3 |
| V2 | Металдық кальцийді аса сұйытылған азот қышқылында еріткенде түзілетін қосылыстар |
| | Ca(NO3)2 |
| | H2O |
| | NH4NO3 |
| V2 | Ерімейтін анодтарды қандай материалдардан жасап шығарады |
| | көмір |
| | графит |
| | платина |
| V2 | Сурик тұз қышқылын тотықтырады, соның нәтижесінде мынадай қосылыстар түзіледі... |
| | PbCl2 |
| | H2O |
| | Cl2 |
| V2 | Bi(OH)3 мен Na2SnO2 әрекеттесуі кезінде мынадай қосылыстар түзіледі... |
| | Bi |
| | Na2SnO3 |
| | H2O |
| V2 | Аммиак синтезінің барлық өнеркәсіптік құрылғылары циркуляция ұстанымын қолдану арқылы жұмыс жасайды: |
| | Реакциядан кейін газдар қоспасы суытылады |
| | Газдар қоспасының құрамындағы аммиак конденсацияланады және бөлініп алынады |
| | Әрекеттеспей қалған азот пен сутек жаңа газ қоспасымен араластырылып, катализаторға қайта жіберіледі |
| V2 | S пен HNO3 әрекеттесуі кезінде мынадай қосылыстар түзіледі... |
| | H2SO4 |
| | NO2 |
| | H2O |
| V2 | NaOH мен NO2 әрекеттесуі кезінде мынадай қосылыстар түзіледі... |
| | NaNO3 |
| | NaNO2 |
| | H2O |
| V2 | Висмут (III) сульфидін концентрлі азот қышқылында еріткенде түзілетін заттар: |
| | Bi(NO3)3 |
| | NO |
| | S |
| V2 | Пероксокүкірт қышқылдарының құрамы: |
| | Н 2SО5 |
| | Н2 S2О8 |
| | Н2 S3 О11 |
| V2 | К3AsO3, K2Cr2O7 және күкірт қышқылы ерітінділерінің әрекеттесуі нәтижесінде түзілетін қосылыстар |
| | К3AsO4 |
| | Cr2(SO4)3 |
| | K2SO4 |
| V2 | Алюминийдің қасиеттері |
| | Амфотерлі қасиеттер көрсетеді |
| | Қосылыстарда катионның құрамында кездесуі мүмкін |
| | Қосылыстарда анионның құрамында кездесуі мүмкін |
| V2 | Алюминий сұйытылған азот қышқылымен қарқынды әрекеттесіп, мынадай қосылыстар түзіледі... |
| | Al(NO3)3 |
| | N2O |
| | H2O |
| V2 | Алюминий өзінің қасиеттері бойынша бордан күрт ерекшеленеді. Атап айтсақ.... |
| | Атомный үлкен мөлшерімен |
| | электрондардың бос d-деңгейге өте алу мүмкіндігі электрондардың еркіндігін, делокализациялану дәрежесін арттырады |
| | Жоғары электро- және жылуөткізгіштікке ие |
| V2 | АlCl3 ерітіндісіне қосылған зат оның гидролизін арттырады |
| | Na2CO3 |
| | NaОН |
| | КОН |
| V2 | АlCl3 ерітіндісіне қосылған зат тұздың гидролизін төмендетеді |
| | НСl |
| | Н2SO4 |
| | HBr |
| V2 | Құрамында мынадай бөлшектер бар ерітінділердің электролизі кезінде су молекулалары анодта тотығатын болады |
| | SO4 2-, SO3 2- |
| | NO3-, PO43- |
| | СО32 |
| V2 | Электролиздеу арқылы тұздарының сулы ерітінділерінен алуға мүмкін емес металдар |
| | Натрий |
| | Барий |
| | Алюминий |
| V2 | Еритін анод ретінде қолдануға болатын металдар |
| | Zn |
| | Sn |
| | Pb |
| V2 | Қорғасын аккумуляторының негізін құрайтын химиялық қосылыстар (ең қарапайым түрде) |
| | Pb |
| | PbO2 |
| | H2SO4 |
| V2 | Қорғасынды аккумуляторды зарядтау кезінде мынадай заттардың түзілуімен үдеріс жүреді: |
| | Pb |
| | PbO2 |
| | H2SO4 |
| V2 | Кобальтті көміртек (ІІ) оксиді атмосферасында 150-200°С температура және 250 атм. қысым кезінде суда ерімейтін, бірақ органикалық еріткіштерде еритін карбонил типті қосылыстар түзіледі. Бұл қосылыстардың құрамы мен байланыс түрі мынандай ... |
| | Органикалық еріткіштерде қосылыс димер Со2(СО)8 түрінде кездеседі |
| | Со және СО арасындағы байланыс донорлы – акцепторлы механизм бойынша, екі кобальт атомдарының бос электрондардың жұптасуы арқылы түзіледі |
| | Карбонилдарда кобальт атомының валенттігі 0 тең |
| V2 | Германий топшасының Ge – Sn – Pb қатарындағы элементтер жай заттарының химиялық активтігінің өзгеруін сипаттаңыз |
| | Германий топшасының элементтерінің металдық қасиеттері артады |
| | Ge – Sn – Pb қатарында металдық активтілік (электрондарды беру қабілеті) жалпы заңдылық бойынша артады |
| | Сәйкесінше, аталған қатарда химиялық активтілік артады |
| V2 | Қышқылдардың сұйытылған сулы ерітінділерінде сутек иондарымен, тотығатын германий топшасының элементтері |
| | Ge – Sn – Pb қатарында металлдық қасиеттері артады, сондықтан осы қатардағы активтігі төменірек германий сутек иондарымен тотығады |
| | Ge – Sn – Pb қатарында металлдық қасиеттері артады, сондықтан осы қатардағы активтігі жоғары қалайы сутек иондарымен тотығады |
| | Ge – Sn – Pb қатарында металлдық қасиеттері артады, сондықтан осы қатардағы активтігі жоғары қорғасын сутек иондарымен тотығады |
Наши рекомендации
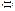 2NH3+ Q реакция бойынша аммиактың шығымын жоғарылатуға әсер ететін дәйектер
2NH3+ Q реакция бойынша аммиактың шығымын жоғарылатуға әсер ететін дәйектер 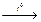
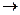
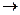
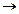 реакциясы барысында мыналар бөлінеді
реакциясы барысында мыналар бөлінеді 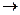
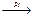 (өршіткі қатысында)
(өршіткі қатысында)  (қыздыру және жарық түсіру)
(қыздыру және жарық түсіру) 
 (қыздыру және жарық түсіру)
(қыздыру және жарық түсіру)