Промышленное применение электролиза
Электролизимеет ряд важных промышленных применений. Они включают извлечение и очистку металлов, нанесение гальванических покрытий, а также анодирование и получение различных химических веществ.
Извлечение металлов
Извлечение металлов первой и второй групп периодической системы осуществляется с помощью электролиза из расплавленных галогенидов этих металлов. Например,натрийполучают электролизом расплавленного хлорида натрия в электролизере Даунса.Магнийполучают электролизом хлорида магния, который в свою очередь получают из доломита и морской воды.
Очистка металлов
Очистка таких металлов, какмедьицинк, может осуществляться с помощью электролиза с растворимым анодом. Очистка металлов называется рафинированием. На рис. 7.10 схематически изображен процесс очистки меди. Неочищенная медь играет в этом процессе роль анода, а очищенная медь - роль катода; в качестве электролита может использоваться раствор сульфата меди.
На аноде протекает полуреакция
Cu0- 2 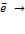 Cu2+.
Cu2+.
Примеси, высвобождаемые при растворении неочищенноймедина аноде, опускаются на дно электролизера, образуя так называемый анодный ил. Этот ил может содержать драгоценные металлы, например золото и серебро. Переходящие в раствор ионы меди разряжаются и осаждаются на чистом медном катоде. Эта полуреакция описывается уравнением
Cu2++ 2 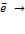 Cu0.
Cu0.
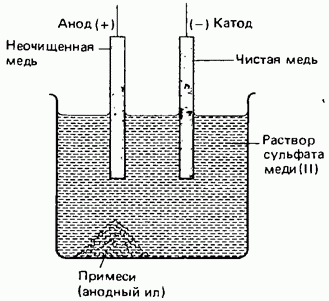
Рис. 7.10. Рафинированиемеди.
Нанесение гальванических покрытий (гальваностегия)
В этом процессе нанесение покрытия (электроосаждение) осуществляется на катоде. Катод погружают вэлектролит, который содержит ионы электроосаждаемого металла. В качестве анода используется пластина или стержень из того металла, которым наносят покрытие. Для успешного проведения электроосаждения следует тщательно контролировать силуэлектрическоготока, концентрацию электролита и температуру. Кроме того, необходимо предварительно подвергнуть очистке катод.
Нанесение гальванического покрытия может включать целый ряд стадий. Например, покрытие железа хромом включает четыре стадии:
1. Очистка железного предмета, играющего роль катода, при помощи серной кислоты с последующей промывкой деионизированной водой.
2. Покрытие железного катода медью.
3. Последующее покрытие катоданикелемс целью предотвращения коррозии.
4. Окончательное покрытие предмета хромом.
Гальванопластика.Это электролитическое осаждение металла на поверхности какого-либо предмета для воспроизведения его формы. Для этого с предмета сначала снимают слепок (из воска или гипса) и покрывают его токопроводящим слоем, например, слоем графита. Подготовленный таким способом предмет помещают в качестве катода в ванну с раствором соли соответствующего металла. При включении тока металл из электролита оседает на поверхности предмета. Гальванопластику используют для изготовления неограниченного числа точных копий того изделия, с которого был снят слепок.
Гальванополировка
Если резное металлическое изделие поместить в раствор электролита и включить ток, то наиболее сильное электрическое поле образуется у микроскопических выступов на поверхности этого изделия. Если оно подключено к «+» источника тока, то наиболее интенсивно ионы металла будут «вырываться» именно из выступов, и поверхность металла выровняется.
Анодирование
Так называется процесс покрытия алюминиевых предметов оксидом алюминия. В этом процессе покрываемый предмет играет роль анода, а в качестве электролита используется разбавленная сернаякислота. Покрытие изоксидаалюминияпредохраняет предмет от коррозии.
