Квантово – механическая модель атома
Вскоре было установлено, что представление об электроне как частице, подчиняющейся законам классической механики, является ошибочным. Изучение природы и распространения света показало, что он обладает как корпускулярными, так и волновыми свойствами. На первые указывает явление фотоэффекта, на вторые – явления интерференции и дифракции света.
В 1924 г. Луи де Бройль распространил идею о двойственности природы света на вещество, предположив, что поток материальных частиц должен обладать и волновыми свойствами, однозначно связанными с массой и энергией.
Корпускулярные свойства электрона выражаются в его способности проявлять свое действие как целого. Волновые свойства электрона проявляются в особенностях его движения, в дифракции и интерференции электронов.
Электрон в атоме и молекуле обладает как свойствами частицы, так и волновыми свойствами. Частицы, размер которых соизмеримы с их длинной волны или меньше, называются микрочастицами и микрообъектами.
В 1927 г. В. Гейзинберг (Германия) постулировал принцип неопределенности, согласно которому положение и импульс субатомной частицы (микрочастицы) принципиально невозможно определить в любой момент времени с абсолютной точностью. В связи с этим в квантовой механике состояние микрочастицы полностью описывается не ее координатой и скоростью, а некоторой функцией. Эта функция носит вероятностный характер и обозначает греческой буквой «пси» ψ.
Функция ψ, описывающая состояние электрона в атоме или молекуле и являющаяся обычной математической функцией, часто называется волновой функцией или орбиталью.
Величина ψ2 всегда положительна. ψ2*ΔV – мера вероятности нахождения электрона в элементе пространства ΔV.
В наиболее простом случае эта функция зависит от трех координат и называется орбиталью. В соответствии с определением ψ, орбиталью называется область околоядерного пространства, в которой наиболее вероятно нахождение электрона.
Представление об электроне, как о материальной точке не соответствует его истиной физической природе. Поэтому орбиталь правильнее рассматривать как схематическое изображение электрона, «размазанного» по всему объему атома в виде так называемого электронного облака. Иначе говоря, плотность электронного облака пропорциональна квадрату волновой функции.
Движение электрона и других микрочастиц описывают квантово-механические законы, в частности уравнение Шредингера.
При решении уравнения Шредингера, можно найти, что распределение электрона по энергиям и в пространстве определяется волновой функцией ψ, зависящей от сферических координат электрона и от трех параметров (n, l, ml).
Параметры n, l, ml – называются квантовыми числами. В простейших приложениях квантовой механики иногда удобно вместо самой волновой функции пользоваться квантовыми числами, представляющими ее.
Главное квантовое число n – определяет энергию и размеры электронных орбиталей. Главное квантовое число принимает значения 1, 2, 3, 4 и т.д., и характеризует оболочку или энергетический уровень. Чем больше n, тем выше энергия. Оболочки (уровни) имеют буквенные обозначения: K (n=1), L (n=2), M (n=3), N (n=4), переходы электронов с одной оболочки на другую сопровождаются выделением кванта энергии, которые могут проявиться в виде линий спектров. Главное квантовое число n эквивалентно квантовому числу в теории Бора.
En =–(2π2me4Z2)/(n2h2) = –13,6 эВ* Z2/n2,
где Z – заряд ядра.
Допустимые значения:
| n = 1, 2, 3, 4, 5,.. |
| K L M N O,.. |
Орбитальное квантовое число l определяет орбитальный момент количества движения электрона и характеризует форму электронного облака. Каждому n соответствует определенное число значений l, то есть энергетический уровень представляет собой совокупность энергетических подуровней, несколько различающихся по энергиям. Число подуровней, на которое расщепляется энергетический уровень, равно номеру уровня (то есть численному значению n).Орбитальное квантовое число также характеризует энергетические подуровни в электронной оболочке атома.Орбитальные квантовые числа принимают целочисленные значения от 0 до (n-1).
Исторически первые четыре значения имеют буквенные символы, произошедшие от спектроскопических терминов, использованных в 1890-е годы при описании спектров щелочных металлов: 0 – s (sharp – резкий); 1 – p (principal – главный); 2 – d (diffuse – диффузный); 3 – f (fundamental – фундаментальный). Эти буквы не являются сокращениями слов, описывающих «форму» орбитали. Изображаемые в учебниках «формы» орбиталей представляют собой графики функций, изображающие области математического пространства, где нахождение электрона данной орбитали наиболее вероятно. Эта область определяется квадратом соответствующей волновой функции. (Следует учитывать, что изображаемые в учебниках «орбитали» – графики математической функции для решения уравнения Шредингера в одноэлектронном приближении, но ни в коем случае не физический (материальный) объект. Орбитали – математический уровень описания микрообъектов)
«Формы» орбиталей, соответствующие различным значениям l, приведены на следующем рисунке (рис 1.2):
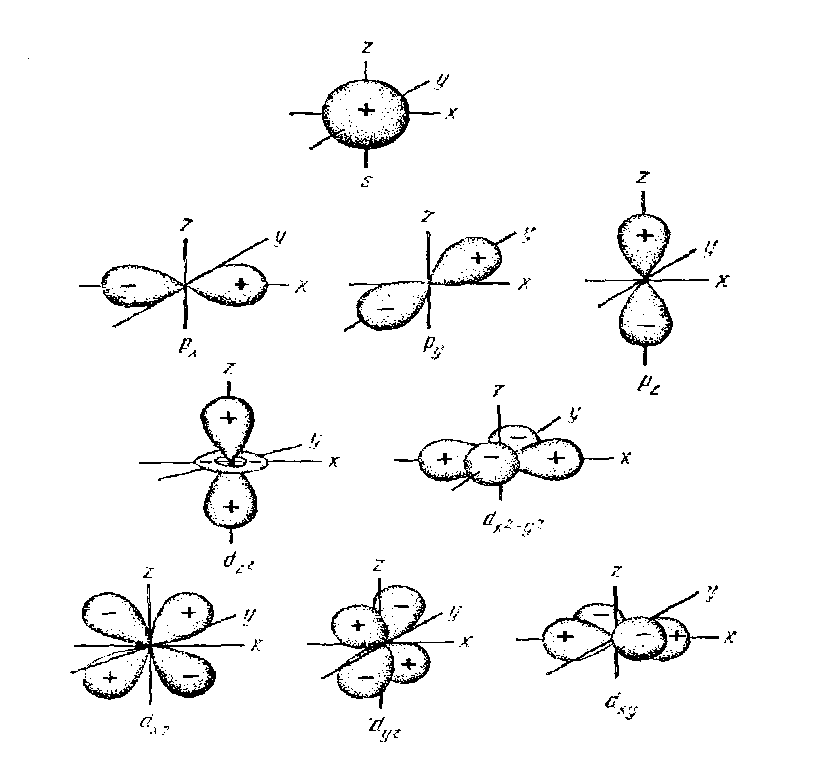
Рис. 1.2 – Форма и пространственная ориентация электронных облаков
s-, p- и d-орбиталей
В одном и том же уровне энергия подуровней возрастает в ряду: Es<Ep<Ed<Ef
Магнитное квантовое число ml определяет значение составляющей проекции момента количества движения электрона на выделенное направление в пространстве. Характеризует ориентацию орбиталей в пространстве. В отсутствие внешнего магнитного поля электроны на орбиталях с одинаковым значением орбитального квантового числа l энергетически равноценны (т.е. их энергетические уровни вырождены). Однако в постоянном магнитном поле некоторые спектральные линии расщепляются. Это означает, что электроны становятся энергетически неравноценными. Например, p-состояния в магнитном поле принимают 3 значения вместо одного, d-состояния – 5 значений. Допустимые значения ml от –l до +l, включая 0.
В общем виде любому значению l соответствует (2l+1) значений магнитного квантового числа, то есть (2l+1) возможных расположений электронного облака данного типа в пространстве. Следовательно, можно говорить, что число значений mlуказывает на число орбиталей с данным значением l.
Каждая электронная орбиталь в атоме может характеризоваться тремя квантовыми числами n, l, ml. Общее число орбиталей, из которых состоит любой энергетический уровень (слой), равно n2, а число орбиталей, составляющих подуровень – (2l+1).
