Поступление и выведение ксенобиотиков
Пассивный транспорт
При простой диффузии ксенобиотики проходят через мембрану в результате случайного молекулярного движения, и величина потока линейно зависит от концентрации и коэффициента проницаемости мембраны для данного вещества.
Биологические мембраны, как известно, представляют собой мозаичную структуру, состоящую из липидов, структурных белков, белков-ферментов и других компонентов. «Сердцевина» мембраны представляет собой в основном гидрофобную область, поэтому неполярные вещества сравнительно легко проникают в клетки. Гидрофобные группы способствуют увеличению проникающей способности, полярные – ее уменьшению.
Так, например, пропиловый спирт проникает в эритроциты в 3 раза быстрее, бутиловый в 10 раз быстрее, чем этиловый. С другой стороны, проникающая способность бутанола резко уменьшается при введении в его молекулу дополнительных полярных ОН-групп.
Различие в проницаемости зависит от скорости диффузии через мембрану, причем уменьшение скорости диффузии для разветвленной углеводородной цепи обусловлено стерическими факторами. Проницаемость неэлектролитов зависит также и от липидного состава мембраны.
В качестве количественного параметра проникновения любого вещества в клетку вводится коэффициент проницаемости. В этом случае скорость переноса определяют с помощью закона Фика:
1 dS (Cн – Cв)
–– ––– = –DKр –––––––––, (7.1)
A dt Dx
где D – коэффициент диффузии; А – площадь поверхности; Cн, Cв – концентрация снаружи и внутри соответственно; Кр – коэффициент распределения, представляющий отношение концентрации растворенного вещества в мембране к концентрации вне мембраны; Dx – расстояние, преодолеваемое соединением при прохождении через мембрану.
Так как молекуле, возможно, приходится преодолевать путь Dx, не обязательно равный толщине мембраны, то этот путь трудно измерить непосредственно. Коэффициент распределения обычно определяют, используя в качестве липидной фазы оливковое масло, а не истинные липиды, что вводит некоторую неопределенность в величину К. Зависимость D от x также неизвестна ни для какой мембраны. Поэтому Р = DKр/Dx (коэффициент проницаемости) является единственной измеряемой величиной, характеризующей мембрану и переносимое растворенное вещество, которую легко вычислить, используя выражение:
dS/dt = PA(Cн – Cв) , (7.2)
где размерность Р – длина в единицу времени (т. е. скорость), см/с.
Во всех случаях прохождения растворенных веществ через плазматическую мембрану обнаруживается тесная связь между проницаемостью и коэффициентом распределения для системы масло–вода. Чем выше липофильность вещества, тем выше коэффициент распределения.
Для различных веществ способность проникать через мембрану определяется, как уже отмечалось, и коэффициентом распределения. Отношение концентраций какого-либо вещества, состоящего из простых молекул, в двух находящихся в равновесии фазах имеет постоянное значение и называется константой распределения Кр:
Кр = С2/С1, (7.3)
где С1 – водная фаза, С2 – неводная фаза (масло, липид).
Это соотношение получено в предположении, что в системе нет заметных взаимодействий между молекулами растворенного вещества или сильных специфических взаимодействий между растворенным веществом и растворителем, которые могли бы повлиять на процесс распределения.
Коэффициент распределения некоторого вещества зависит от способности его молекул к образованию водородных связей. Кроме того, для соединений с одинаковым коэффициентом распределения в системе липид–вода скорость диффузии через мембрану может значительно варьировать в зависимости от пространственной структуры молекул.
Пассивный перенос – это движение вещества по градиенту электрохимического потенциала без затраты энергии, т. е. движущей силой пассивного транспорта веществ служит градиент электрохимического потенциала. Электрохимический потенциал (`m) характеризуется свободной энергией некоторого вещества j.
Химический потенциал, так же как и другие виды потенциальной энергии, является относительной величиной, т. е. он определяется каким-то условным уровнем энергии (вводится константа аддитивности или стандартный член `m*):
`mj = `mj* + RTlnCj + ZjFY. (7.4)
В случае переноса через мембрану незаряженных частиц уравнение (5.4) упрощается и химический потенциал вещества можно выразить как функцию его концентрации (точнее активности):
`mj = `mj* + RTlnCj . (7.5)
Здесь `mj – энергия на единицу количества вещества (Дж/моль); Cj – концентрация вещества; Zj – заряд; Y – электрический потенциал; R – газовая постоянная; Т – абсолютная температура.
Фактор RT, на который умножается величина lnCj, необходим для перевода активности в единицы энергии на 1 моль.
Если рассмотреть систему в состоянии равновесия, когда электрохимический потенциал вещества одинаков по обеим сторонам мембраны, то:
mjв = `mjн . (7.6)
В этом случае нет градиента электрохимического потенциала и никакая движущая сила не действует на переносимый ксенобиотик; он проходит в результате беспорядочного теплового движения, но при этом два противоположно направленных потока сбалансированы. В этом случае
RTlnCjн + ZjFYн = RTlnCjв + ZjFYв , (7.7)
и соотношение для разности электрических потенциалов (DYр = Yв–Yн) будет иметь вид:
RT Cjн
DYр = ¾¾¾ ln ¾¾. (7.8)
ZjF Cjв
Величину DYр называют потенциалом Нернста. Экспериментально измерив мембранный потенциал и концентрацию ионов по обе стороны мембраны, на основании выражения (7.8) можно предсказать направление пассивного переноса ксенобиотика.
Проницаемость мембран для некоторых малых молекул оказывается более высокой, чем это можно было бы ожидать на основании данных об их растворимости в липидах. В частности, хорошо проникают через мембраны такие гидрофильные вещества, как глицерин, мочевина и др., радиус молекул которых не превышает 0,3 нм. Предполагают, что эти молекулы проходят через особые участки мембраны, так называемые «поры» (каналы). Аналогично считают, что заряженные частицы (ионы) движутся через ионные каналы.
Через ионные каналы осуществляется не только транспорт веществ, они также непосредственно участвуют в передаче сигнала возбудимым клеткам (генерация потенциала действия). Существуют хемовозбудимые (рецепторы ацетилхолина, g-АМК, глутамата, глицина и др.) и электровозбудимые (натриевые, калиевые, хлорные и др.) каналы.
Довольно подробно изучены ацетилхолиновый, натриевый и другие каналы мембран различных клеток. Схематическое строение одиночного ионного канала представлено на рис. 7.1.
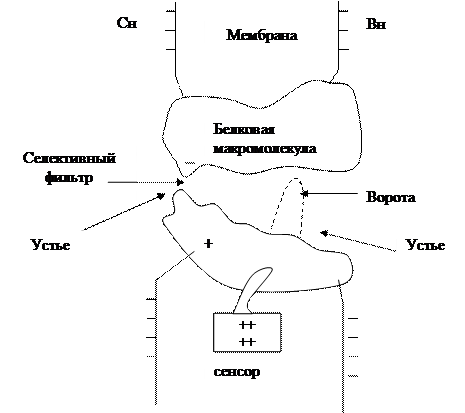 |
| Рис. 7.1. Схема строения потенциалуправляемого ионного канала |
Канал – это белковая макромолекула, субъединицы которой образуют в мембране пору через бислой липидов. В поре имеется узкий селективный фильтр вблизи наружной поверхности мембраны и воротное устройство вблизи ее внутренней поверхности. Пространство между селективным фильтром и воротами получило название туннеля. Сенсор напряжения, расположенный в липидном слое, управляет открытием ворот под влиянием внутримембранного поля. Расширенные части канала у наружной и внутренней поверхности образуют устья (или вестибюли).
Облегченная диффузия. Вещества, нерастворимые в липидах, с размером молекулы более 0,3–0,4 нм, не диффундируют через мембраны. Так, шестиатомные спирты с диаметром молекул 0,42 нм не проникают в большинство клеток. Однако глюкоза и некоторые другие моносахариды с такими же размерами молекул, как правило, хорошо проникают в клетку. Для объяснения высокой проницаемости клеточных мембран по отношению к сахарам, аминокислотам и некоторым другим соединениям была выдвинута концепция «переносчиков», связывающихся с транспортируемым веществом и таким образом «облегчающих» их прохождение через мембрану. Такая облегченная диффузия происходит по градиенту концентрации без затрат энергии и относится к пассивному транспорту.
В основе механизма облегченной диффузии лежит обратимое соединение транспортируемого вещества со специфическим переносчиком, и образующийся комплекс вещество–переносчик диффундирует внутри мембраны от наружной поверхности к внутренней, где комплекс диссоциирует с высвобождением вещества внутрь клетки. Свободный же переносчик диффундирует назад к наружной поверхности мембраны, где соединяется с новой молекулой вещества, и цикл повторяется (рис. 7.2, а, б).
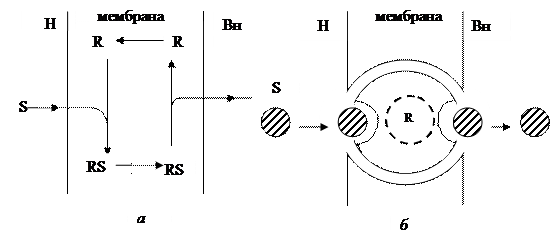 |
| Рис. 7.2. Схема транспорта веществ с участием подвижного (а) и фиксированного (б) переносчиков |
Развивается также тетрамерная модель облегченного переноса. Согласно этой модели транспорт осуществляется не в результате присоединения переносимого субстрата к подвижному переносчику, а путем «внутреннего» переноса субстрата через белковый тетрамер, встроенный в мембрану (фиксированный переносчик). Тетрамер состоит из симметрично расположенных субъединиц, две из которых характеризуются высоким сродством к субстрату, а две – низким. Тетрамер может существовать в одной из двух энергетически эквивалентных конформаций, переход между которыми происходит только в том случае, когда молекула субстрата присоединяется к одной из субъединиц. Этот конформационный переход и является непосредственной причиной переноса субстрата через мембрану (рис. 7.2, б).
Можно отметить ряд характерных отличий между облегченной и простой диффузией.
1. При простой диффузии поток вещества пропорционален внешней концентрации и все время возрастает с увеличением последней. При облегченной диффузии кривая, описывающая поток веществ через мембрану, стремится к насыщению при концентрациях, обеспечивающих связывание всех молекул переносчика.
2. Наличие специфических переносчиков, взаимодействующих с веществами определенного строения, обусловливает резко выраженную зависимость проникающей способности вещества от его химической структуры и, в частности, от пространственной конфигурации его молекул.
3. Облегченная диффузия, в отличие от простой, может ингибироваться некоторыми соединениями (иногда в весьма малых концентрациях), которые блокируют переносчик.
Процесс переноса веществ через мембраны с помощью переносчика описывается в рамках кинетики Михаэлиса – Ментен (рис. 7.3).
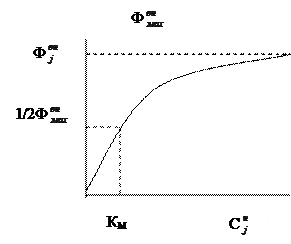 |
| Рис. 7.3. Соотношение между концентрацией растворенного вещества в наружной среде и скоростью поступления внутрь (кинетика Михаэлиса–Ментен) |
Скорость переноса пропорциональна концентрации вещества в интервале низких концентраций, а затем снижается по мере ее роста и в конце концов приближается к максимуму (происходит насыщение) (рис. 7.3.), поток вещества, например, внутрь клетки Фjв, в этом случае описывается соотношением:
С 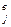 Ф
Ф 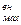
Фjвн = ¾¾¾¾¾, (7.9)
Кj + С 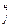
где Ф 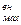 – максимальная скорость переноса; j-ксенобиотика; Кj – константа, характеризующая сродство вещества к переносчику; С
– максимальная скорость переноса; j-ксенобиотика; Кj – константа, характеризующая сродство вещества к переносчику; С 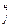 – концентрация веществ в наружной среде.
– концентрация веществ в наружной среде.
При Кj = Сj поток становится равен половине максимального потока. Поэтому и графическое определение константы сводится к определению полумаксимальной величины потока и экстраполяции на точки пересечения оси абсцисс (см. рис. 7.3): чем ниже величина Кj, тем выше сродство транспортируемого вещества к переносчику.
В плазматических мембранах многих животных клеток существуют, как минимум, пять различных белков-переносчиков аминокислот, которые действуют как системы симпорта, перенося одновременно ионы Na+, причем каждый из этих белков специфичен для группы родственных аминокислот. Градиент концентрации Na+ может также приводить в действие системы антипорта. Например, в оплодотворенном яйце морского ежа значительное повышение внутриклеточного рН активирует синтез белков и ДНК; это изменение рН вызывается потоком Н+ из клетки, возникающим благодаря потоку Na+ в клетку.
У бактерий и растительных клеток большинство систем активного транспорта, приводящихся в действие ионными градиентами, используют в качестве котранспортируемого ион Н+, а не Na+. Например, хорошо изучен трансмембранный белок-переносчик лактозы (пермеаза или М-белок), функционирующий в бактериальной мембране. Белок состоит из одной полипептидной цепи (30 000 дальтон) и осуществляет Н+-зависимый симпорт: с каждой транспортируемой в клетку молекулой лактозы переносится один протон. Не исключено и наличие переносчиков определенных видов ксенобиотиков.
Для регуляции переноса веществ используются ионофоры. Ионофоры – это небольшие гидрофобные молекулы, которые растворяются в липидных бислоях и повышают их проницаемость для ионов. Большинство ионофоров синтезируется микроорганизмами (вероятно, в качестве биологического оружия против своих конкурентов); некоторые из них используются как антибиотики. Ионофоры широко применяются для повышения проницаемости мембран по отношению к определенным ионам. Существуют два класса ионофоров – подвижные переносчики ионов и каналообразующие ионофоры. Ионофоры обоих типов действуют, экранируя заряд транспортируемого иона так, чтобы последний мог пройти гидрофобную внутреннюю область липидного бислоя. Поскольку ионофоры не связаны ни с каким источником энергии, они лишь позволяют ионам двигаться по электрохимическим градиентам.
Примером каналообразующего ионофора является грамицидин А. Он представляет собой линейный пептид, состоящий из 15 аминокислот; все они имеют гидрофобные боковые цепи. Вероятно, в бислое две молекулы грамицидина объединяются и образуют трансмембранный канал, позволяющий моновалентным катионам передвигаться по электрохимическим градиентам. При наличии большого электрохимического градиента грамицидин А может пропустить 2×107 катионов в расчете на один открытый канал за 1 с, что в 1000 раз больше, чем может перенести за это же время одна молекула подвижного переносчика.
В расчете на один открытый канал за 1 с, что в 1000 раз больше, чем может перенести за это же время одна молекула подвижного переносчика.
Подвижный переносчик (ионофор) валиномицин осуществляет перенос ионов калия через мембраны. Он представляет собой полимер и имеет кольцеобразную структуру. Наружная гидрофобная часть его молекулы состоит из боковых цепей валина и контактирует с углеводородной сердцевиной липидного бислоя. Во внутренней полярной области как раз может поместиться один ион калия ( рис. 7.4).
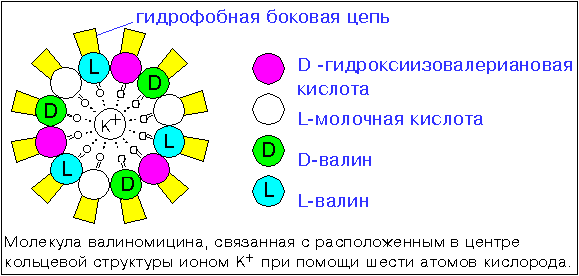
Валиномицин переносит ионы калия по его электрохимическому градиенту ; он захватывает этот ион с одной стороны мембраны, диффундирует с ним через бислой и высвобождает на его на другой стороне. Такой перенос совершается в обоих направлениях, поэтому суммарный эффект будет иметь место только в том случае, если при движении переносчика в каком-то одном направлении с ним будет связываться больше ионов калия, чем при движении в другом.
Активный транспорт
Как мы уже отмечали, активный транспорт веществ либо осуществляется за счет сопряжения электрохимических градиентов, либо выполняется молекулярными машинами (АТФазами). Активный перенос происходит с затратой энергии и идет против градиента электрохимического потенциала.
Следует различать первичный и вторичный (или сопряженный) активный транспорт.
Первичный активный транспорт – трансмембранный векторный перенос веществ осуществляется непосредственно в ходе реакции энергетического преобразования в АТФазных системах или ОВЦ, т. е. используется энергия либо АТФ, либо энергия ОВ реакций. Он подразделяется на:
а) электрогенный активный транспорт – первичный активный перенос веществ через мембрану во время АТФазной или окислительно-восстановительной (ОВ) реакциях, сопровождаемых генерацией электрического потенциала;
б) электронейтральный активный транспорт – первичный активный перенос веществ во время АТФазной или ОВ реакциях, не сопровождающихся генерацией электрического потенциала (стехиометрия обмена 1:1).
Вторичный активный перенос совершается, когда в качестве энергетических источников используются градиенты электрохимических потенциалов других ионов. Например, электрохимический градиент ионов Н+для сопряженного транспорта анионов, сахаров, аминокислот и других веществ в клетку (симпорт или котранспорт) или, напротив, для вывода ионов Na+ из клетки (антипорт или противотранспорт).
Согласно классической модели активного переноса, растворенная молекула соединяется с носителем. По одну сторону мембраны носитель в результате химической реакции, протекающей с поглощением метаболической энергии, например в форме АТФ, видоизменяется таким образом, что он приобретает сильное сродство к подлежащей переносу молекуле и присоединяет ее к себе (активация). Образовавшийся комплекс носителя с этой молекулой проходит через мембрану (переориентируется). Затем происходит вторая химическая реакция, в результате которой сродство носителя к транспортируемой молекуле уменьшается; она высвобождается и выделяется внутрь (релаксация). Затем цикл повторяется. Процессом, идущим с потреблением энергии, является модифицирование структуры носителя (рис.7.4).
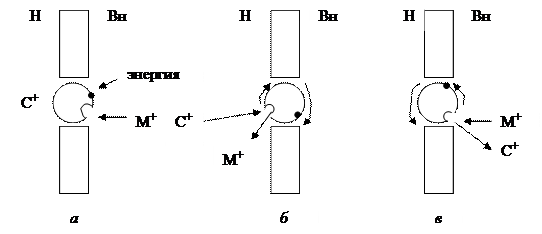 |
| Рис. 7.4. Схематическое представление функционирования электронейтрального ионного насоса: а – активация; б – переориентация; в – релаксация |
Наиболее широко в живых системах распространены и изучены Na+/K+-АТФаза (животные клетки и гликофиты, морские водоросли) и Н+-АТФаза, которые могут работать в режиме переноса Н+ и Н+/K+ обмена на плазматических мембранах растительных клеток, митохондрий. Все Na+/K+-АТФазные системы и их препараты имеют ряд общих свойств. Так, для их активации необходим Mg2+, константа КМ составляет ~ 10 мМ для Na+ и 1 мМ для K+; вероятно, в системе имеется два центра связывания катионов – один из них расположен внутри клетки и связывает Na+, а другой – снаружи и связывает K+; оптимум рН составляет ~ 7,5; все эти АТФазы ингибируются различными гликозидами (например, уабаин подавляет активность фермента на 50 % в концентрации 10–7– 10–4 М). В оптимальных условиях при расщеплении одной молекулы АТФ происходит перенос ионов со стехиометрией 3 Na+/2K+ (натрий наружу, калий внутрь).
Согласно традиционной точке зрения, для каждого вещества имеется свой носитель, который модифицирует свою структуру, взаимодействуя с АТФ при участии фермента, специфичного для данного носителя. Таким образом, сколько транспортируемых веществ, столько и механизмов активного транспорта.
В настоящее время все большую популярность завоевывает точка зрения, согласно которой меняется один универсальный механизм энергообеспечения активного переноса различных соединений как заряженных, так и нейтральных – электрохимические потенциалы ионов натрия или протонов, которые образуются благодаря работе Na+/K+-зависимой АТФазы (животные клетки), Н+-АТФазы (растительные и др.). В этом случае создаются электрический и концентрационный градиенты, определяющие движение веществ. Проиллюстрируем это положение на работе Н+-АТФазной помпы плазмалеммы растительных клеток (рис. 7.5).
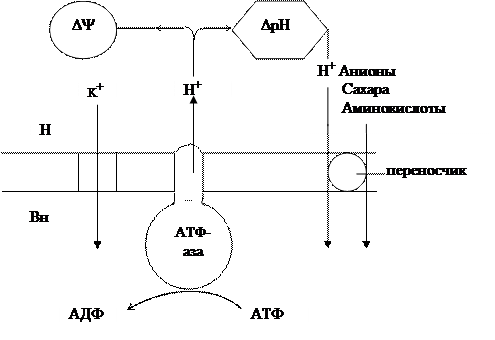 |
| Рис. 7.5. Вторичный активный транспорт (на примере функционирования Н+-АТФазной помпы) |
Выход протонов из клетки сопряжен с работой Н+-АТФазы плазмалеммы и является активным процессом, в результате которого на мембране создается электрохимический градиент D`mн. Электрохимический градиент любого вещества включает электрическую и концентрационную составляющие. В случае переноса положительно заряженной частицы наружу на мембране устанавливается более высокий по абсолютной величине потенциал DY (внутренняя сторона заряжена отрицательно по отношению к наружной) и изменяется разность концентраций переносимого иона, в данном случае DрН. Создавшаяся ситуация приводит к тому, что калий (или другой положительно заряженный катион) по градиенту электрохимического потенциала, а протон по градиенту концентрации входят в клетку. При своем движении внутрь клетки протон активирует переносчик, транспортирующий либо анион, либо аминокислоты, либо другие соединения.
Вторичный активный транспорт приводится в действие за счет энергии, запасенной в градиентах веществ, а не путем прямого гидролиза АТФ. Все они работают как котранспортные системы: одни функционируют по принципу симпорта, а другие – по принципу антипорта. В животных клетках котранспортируемым ионом обычно оказывается Na+. Например, активный транспорт некоторых сахаров и аминокислот внутрь животных клеток обусловливается градиентом Na+ через плазматическую мембрану. Всасывание глюкозы в клетки кишечника и почек достигается с помощью системы симпорта, в которой глюкоза и ионы Na+ связываются с различными участками на белке-переносчике глюкозы; Na+ стремится войти в клетку по своему электрохимическому градиенту и активирует переносчик, перемещающий глюкозу внутрь. Чем выше градиент Na+, тем больше скорость всасывания глюкозы. Наоборот, если концентрация Na+ во внеклеточной среде заметно уменьшается, транспорт глюкозы останавливается. Ионы Na+, проникающие в клетку вместе с глюкозой, выкачиваются обратно Na+/К+-АТФазой, поддерживающей градиент концентрации Na+.
Среди многих систем, с помощью которых осуществляется транспорт веществ против градиента химического (электрохимического) потенциала, вторичные механизмы занимают столь важное место, что некоторые исследователи сомневаются в существовании истинных первичных механизмов активного транспорта неэлектролитов. Действительно, клетки получают большие преимущества, если в качестве источника энергии могут использовать градиент электрохимического потенциала ионов. Однако при рассмотрении механизмов сопряжения потоков ионов и неэлектролитов (нейтральных молекул) необходимо помнить, что если выделяемые из клетки ионы (Н+ или Na+) способствуют транспорту углеводов, аминокислот, сахаров и др. веществ, то для каждой такой системы требуется отдельный переносчик, узнающий специфический субстрат.
Отметим, что энергетическое сопряжение селективной диффузии с каким-либо термодинамическим градиентом, создаваемым за счет расхода метаболической энергии, придает пассивной (облегченной) диффузии все черты активного транспорта. Поэтому между облегченной диффузией и активным транспортом нет непроходимой границы: в зависимости от наличия или отсутствия энергетического сопряжения один и тот же механизм транспорта веществ может иметь черты как активного, так и пассивного.
Очень важный механизм транспорта из ксенобиотиков (выведения из клетки) - функционирование Р-гликопро-теина, являющегося транспортной АТФазой (рис. 7.6). Когда гидрофобное вещество, в том числе противораковое лекарство, проникает в клетку, то оно удаляется из нее Р-гликопротеином за счет энергии гидролиза АТФ. Это снижает эффективность химиотерапии рака.
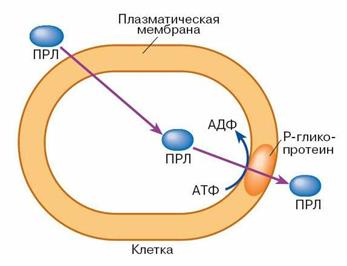 |
| Рис.7.6. Функционирование Р-гликопротеина. ПРЛ – противораковое лекарство (гидрофобное вещество) (Кулинский, 1999) |
В переносе веществ через мембраны принимают участие редокс-цепи мембран, т. е. окислительно-восстановительные реакции (например, ОВ дыхательной цепи). Исходным звеном РЦ выступают восстановленные пиридиннуклеотиды, а конечным акцептором электронов является О2.
Например, имеется множество данных о существовании тесного сопряжения между процессом окисления D-лактата и транспортом сахаров, аминокислот и т. д.
К субстратам, которые могут с той или иной эффективностью использоваться в РЦ, относятся также a-глицерофосфат, значительно реже L-лактат, DL-a-оксибутират и др.
По данному механизму транспортируются такие сахара, как галактоза, арабиноза, глюкоза-6-фосфат, глюконат и глюкуронат, большинство природных аминокислот, за исключением глутамина (и, возможно, аспарагина), аргинина, метионина и орнитина.
Предполагаемый механизм переноса условно изображен на рис. 7.7:
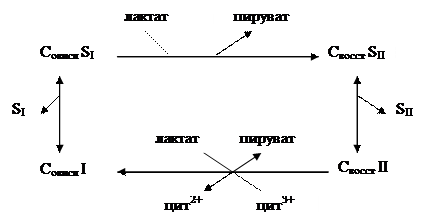 |
| Рис. 7.7. Схема переноса веществ при участии окислительно-восстановительных систем |
В теории транспорта с участием ОВ систем имеются свои проблемы, связанные, в частности, с тем, что окисление разных транспортируемых веществ должно идти разными путями. С другой стороны, многие факты, рассматриваемые как аргументы в пользу ОВ транспорта, можно объяснить в рамках другого механизма (например, протон-движущей силы).
Пиноцитоз и фагоцитоз
И наконец, следует отметить попадание в клетку веществ с помощью пиноцитоза и фагоцитоза. Транспортные белки (переносчики, АТФазы) способствуют проникновению через клеточные мембраны многих полярных молекул небольшого размера, однако они не способны транспортировать макромолекулы, например белки, полинуклеотиды, полисахариды, а также твердые частицы. Тем не менее в большинстве клеток указанные вещества проходят в обоих направлениях через плазматические мембраны. Механизмы, с помощью которых осуществляются эти процессы, сильно отличаются от механизмов, опосредующих транспорт небольших молекул и ионов. При переносе макромолекул или твердых частиц происходит инвагинация (впячивание) мембраны с последующим образованием пузырьков (везикул). Например, для того чтобы секретировать инсулин, клетки, индуцирующие этот гормон, упаковывают его во внутриклеточные пузырьки, которые сливаются с плазматической мембраной и отрываются во внеклеточное пространство, высвобождая при этом инсулин. Подобный процесс называется экзоцитозом. Во всех эукариотических клетках имеются и другие пузырьки, переносящие посредством аналогичного процесса от аппарата Гольджи к плазматической мембране новосинтезируемые компоненты.
Клетки способны также поглощать макромолекулы и частицы и в обратном направлении. Этот процесс называется эндоцитозом (внутрь клетки).
Хотя ясно, что быстрое и повсеместное образование и слияние пузырьков – это фундаментальная особенность всех эукариотических клеток, молекулярные механизмы, обеспечивающие приведение в действие и направление этого транспорта по специфическим путям, требуют дальнейшего изучения.
Тем не менее каждый пузырек сливается только со специфическими мембранными структурами, что гарантирует правильный перенос макромолекул и их распределение между внеклеточным пространством и внутренностью клеток.
В эукариотических клетках секреция макромолекул и твердых частиц почти всегда происходит за счет экзоцитоза. Одни секретируемые молекулы адсорбируются на поверхности клетки и становятся частью клеточной оболочки, другие включаются в межклеточный матрикс, а третьи попадают в интерстициальную жидкость и (или) в кровь, где они служат для других клеток в качестве питательных веществ или каких-то сигналов.
Оба процесса – и экзоцитоз, и эндоцитоз – представляют собой локальные ответные реакции плазматической мембраны и находящейся под ней цитоплазмы.
Пиноцитоз подразделяется на несколько этапов:
1) адсорбция на мембране молекул вещества; 2) впячивание или выпячивание (инвагинация) мембраны, образование пиноцитозного пузырька и отрыв его от мембраны с затратой энергии АТФ; 3) миграция пузырька внутрь протопласта, органеллы или наружу; 4) растворение мембраны пузырька (при действии фермента) или просто ее разрыв.
Исходя из функционирования транспортных механизмов на мембранах, последние делят на четыре типа.
К первому типу относят мембраны, через которые транспорт веществ осуществляется путем простой диффузии, а скорость переноса прямо пропорциональна разности концентраций по обеим сторонам мембраны. Они препятствуют прохождению ионов и пропускают нейтральные молекулы. Через такие мембраны быстрее всего диффундируют молекулы веществ с высоким коэффициентом распределения в системе масло–вода, т. е. веществ, обладающих выраженными липофильными свойствами.
Мембраны второго типа характеризуются наличием в них специфического переносчика, обеспечивающего облегченную диффузию и способствуют всасыванию ряда веществ, плохо проникающих через мембраны первого типа из-за высокой степени ионизированности или высокой гидрофильности. Транспортируемая молекула в мембране обратимо соединяется с переносчиком. Из-за малой толщины мембраны при связывании молекул снаружи и высвобождения внутри клетки переносчик может испытывать лишь незначительные конформационные изменения, поэтому даже простого изменения заряда может оказаться достаточным для того, чтобы молекула высвободилась.
Иллюстрацией может служить транспорт глюкозы в эритроциты человека. Показано, что кроме Д-глюкозы, переносчик транспортирует Д-маннозу, Д-ксилозу, несколько менее активно Д-арабинозу, а также некоторые синтетические неметаболизирующиеся сахара. Для фруктозы, например, существует свой переносчик.
Особый интерес представляет облегченная диффузия в клетку молекулы холина. Простая диффузия ионизированной гидрофильной молекулы холина невозможна, однако специфический переносчик быстро доставляет его в эритроциты и другие клетки.
Мембраны третьего типа (наиболее сложные из всех) способны при необходимости переносить вещества против градиента концентрации. Эта так называемая система активного транспорта требует затраты энергии, высокочувствительна к изменениям температуры.
Примерами, иллюстрирующими проницаемость мембран третьего типа, могут служить: а) транспорт Na+ и K+ в клетки млекопитающих, перенос Н+ и K+ в клетках растений и т. д.; б) всасывание и выведение различных ионизированных и неионизированных веществ почечными канальцами и в меньшей мере через мембраны эпителия желудочно-кишечного тракта; в) захват бактериями неорганических ионов, сахаров и аминокислот; г) накопление ионов йода щитовидной железой; д) накопление K+, Na+, Са2+ и Mg2+ против градиента электрохимического потенциала в митохондриях.
Часто мембраны второго и третьего типов бывают вкраплены в мембрану первого типа.
Мембраны четвертого типа отличаются от первого типа наличием пор (каналов), диаметр которых можно оценить по размерам самых больших молекул, проникающих через них. Один из наиболее изученных примеров мембран четвертого типа представлен почечным клубочком в капсулах Боумана. Клубочки пропускают все молекулы, меньшие по размеру, чем молекулы альбумина (ОММ 70000). Размеры пор составляют 3 нм, и инсулин (ОММ 5000), например, проникает в них с легкостью.
Мембраны четвертого типа встречаются в основном в капиллярах млекопитающих и в паренхиме почек
Таким образом, можно отметить, что наличие определенных транспортных систем определяет и структурно-функциональные особенности биологических мембран различных клеток.
Поступление и выведение ксенобиотиков
На организменном уровне
Организм представляет собой сложную гетерогенную систему, состоящую из большого числа компартментов (отделов): кровь, ткани, внеклеточная жидкость, внутриклеточное содержимое, с различными свойствами, отделенных друг от друга биологическими барьерами. К числу барьеров относятся клеточные и внутриклеточные мембраны, гистогематические барьеры (например, гематоэнцефалический), покровные ткани (кожа, слизистые оболочки).
Находясь во внешней среде, ксенобиотики взаимодействуют с различными организмами (микроорганизмы, растения, животные). В организм человека и животных они поступают из воды, воздуха или с продуктами питания. По имеющимся оценкам из регулярно поступающих в организм токсикантов до 70 % человек получает с пищей, 20 % – из воздуха, 10 % – с водой.
Ксенобиотик, который тем или иным образом попадает в организм, чаще всего подвергается метаболическому превращению с последующим его выведением.
Этапы движения и превращения ксенобиотиков можно представить в виде схемы (рис. 7.8).
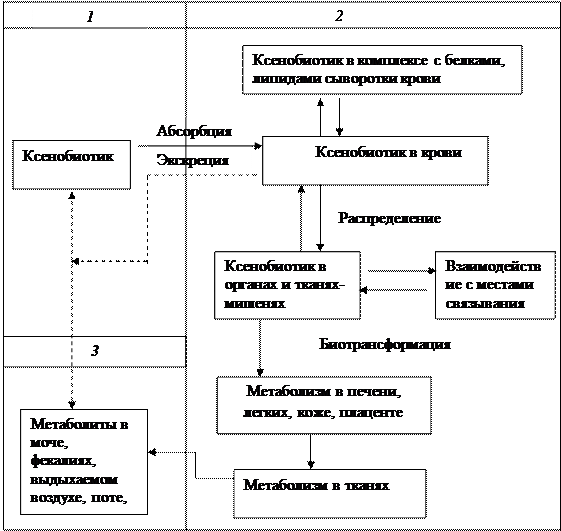 |
| Рис. 7.8. Схема поступления и превращения ксенобиотика в организме: превращения в пищеварительном тракте (1); в крови, органах, тканях (2); метаболиты во внешней среде (3) (Губский, Долго-Сабуров, Храпак, 1993) |
Основные пути поступления ксенобиотиков (промышленные яды, пестициды и др.) в организм животных и человека – это органы дыхания, кожа, пищеварительный тракт.
Поступление через органы дыхания.Ингаляционным путем в организм проникают аэрозоли и газообразные вещества. Например, при проведении дезинфекции, дезинсекции, отравлении угарным газом.
Поступление через кожу.Морфология, биохимия кожи препятствуют резорбции большинства ксенобиотиков. Для водорастворимых веществ кожа представляет непреодолимый барьер. Через кожу проникают преимущественно липофильные вещества, находящиеся в жидком или газообразном состоянии при непосредственном контакте (например, для зомана, фосфорилтиохолинов, иприта, люизита, тетраэтилсвинца и т. д.). Возможны два способа прохождения ксенобиотика через кожу: трансэпидермальный (через клетки эпидермиса) и трансфолликулярный (через волосяные фолликулы).
Помимо способности растворяться в липидах, на скорость поступления веществ через кожу влияет:
- агрегатное состояние,
- дисперсность (размер частиц аэрозолей),
- площадь и область кожных покровов, на которую нанесен ксенобиотик,
- интенсивность кровотока в кожных покровах.
Механические повреждения, мацерация кожи, раздражение, сопровождающиеся усилением кровотока, усиливают процесс резорбции веществ. Некоторые органические растворители, разрушающие липидный слой кожи, могут также усиливать кожную резорбцию.
Поступление через желудочно-кишечный тракт (ЖКТ).Следующий по значимости путь поступления чужеродных веществ – всасывание из пищеварительного тракта непосредственно токсикантов или зараженных продуктов, воды. Участок всасывания (слизистая оболочка желудка, тонкой или толстой кишки) определяется физико-химическими свойствами ксенобиотика, его способностью к ионизации, взаимодействию с мембранами эпителиацитов.
Проникновение ксенобиотиков через слизистую оболочку пищеварительного тракта наблюдается при аварийных ситуациях в результате заглатывания распыленных в воздухе токсических аэрозолей, при применении отравляющих веществ, при поступлении отравленных пищи и воды и т. д.
Энтеральное поступление предполагает хотя бы минимальную растворимость ксенобиотика в содержимом ЖКТ. Слизистая желудочно-кишечного тракта в силу особенностей строения приспособлена для быстрой резорбции веществ. Поскольку сосудистая сеть желудочно-кишечного тракта развита хорошо, резорбция здесь не лимитирована фактором кровоснабжения. Закономерности резорбции аналогичны во всех отделах желудочно-кишечного тракта. Таким образом, проникая через биологические мембраны в сосудистое русло, ксенобиотик далее попадает в ткани к клеточным мишеням. В случае липофильных ксенобиотиков, не являющихся аналогами метаболитов, в качестве мишени выступает сама внутриклеточная среда, т. е. плазматические и внутриклеточные мембраны, элементы хроматинового аппарата, с которыми взаимодействует ксенобиотик. Для промышленных ядов наиболее распространенный путь поступления в организм – всасывание из легких.
Распределение ксенобиотиков внутри организма человека и животного в значительной мере определяется их способностью к абсорбции и участию механизма активного транспорта или связано с функционированием переносчиков. При этом, если в первые минуты и часы после проникновения ксенобиотика-неэлектролита в организм преимущественное значение для его накопления в органах и тканях имеет их кровоснабжение, то с течением времени все большую роль в их распределении играют сорбирующие свойства тканей.
Существенным фактором, влияющим на распределение ксенобиотиков и их способность к дальнейшей биотрансформации и экскреции, как мы уже неоднократно упоминали, является растворимость в липидах (коэффициент распределения).
На поступление ксенобиотиков внутрь тканей и, следовательно, на их токсическое действие значительное влияние оказывает связывание с белками крови, в частности с сывороточным альбумином (СА). Для многих ксенобиотиков их обратимое взаимодействие с СА препятствует проникновению во внутриклеточную среду. Комплексообразование с СА оказывает неоднозначное влияние на скорость метаболизма и экскрецию ксенобиотиков.
Необходимо помнить и о возможности связывания некоторых ксенобиотиков с жировой и мышечной тканью. Исследования в этом направлении показали, что количество ксенобиотика, связанного с тканью мышц человека, может варьировать от 13 до 98 %, при этом наблюдается корреляция между количеством связанного соединения и его липофильностью.
В организме высших млекопитающих при попадании ксенобиотика происходит его распределение с участием циклических механизмов, определяющих, по каким путям (органам и тканям) движется вещество. Циркулирующее в крови вещество (лекарственный препарат) по печеночной артерии и портальной вене попадает в печень. Из обеих долей печени вещество (или его метаболит) вместе с желчью попадает в желчный пузырь. Через определенные промежутки времени желчь поступает в дистальную часть двенадцатиперстной кишки по желчному протоку (двенадцатиперстная кишка представляет собой трубку длиной около 30 см, соединяющую желудок с малым кишечником). Некоторые препараты всасываются в воротную вену и с током крови попадают в печень, а оттуда с желчью снова в тонкий кишечник. В зависимости от вида препарата он может проходить дополнительный цикл: кишечник – легкие – бронхи – трахея – глотка – кишечник. Затем он выводится из организма (моча, кал, отхаркивание).
Экскрецияксенобиотиков и их метаболитов через различные выделительные системы – заключительный этап в процессе поступления и трансформации. Экскреция осуществляется через легкие, почки, печень, кожу, кишечник, слюнные, потовые, слезные, сальные железы, а также молочные железы при лактации.
Экскреция ксенобиотиков легкими. Через легкие удаляются в основном летучие и газообразные вещества, например ингаляционные наркотики и их метаболиты, промышленные газы, а также продукты печеночной биотрансформации многих токсических веществ, в том числе хлорированных углеводородов, этанола и т. д.
Отметим, что продукты метаболических превращений ксенобиотиков могут выделяться без дальнейших изменений либо экскретироваться в виде конъюгатов.
Почечная экскреция ксенобиотиков – основной путь удаления из организма ксенобиотиков и продуктов их биотрансформации. В основе почечной экскреции лежат следующие биологические процессы: клубочковая фильтрация, канальцевая секреция, канальцевая реабсорбция.
В клубочках почечного тельца фильтрации подвергаются вода, глюкоза, аминокислоты, белки с молекулярной массой менее 60 кД и ксенобиотики-неэлектролиты. Канальцевая секреция – активный процесс, осуществляемый с помощью ферментных систем мембранного транспорта преимущественно в проксимальных участках канальцев нефрона. Этим путем в мочу попадают химические вещества, являющиеся органическими кислотами или органическими основаниями.
Канальцевая реабсорбция – процесс обратного всасывания метаболитов и ксенобиотиков в канальцах нефрона. Кроме реабсорбции путем активного транспорта, в проксимальных и дистальных канальцах нефрона неионизированные формы веществ подвергаются реабсорбции и экскреции путем пассивной диффузии.
Экскреция ксенобиотиков печенью. Выделение метаболитов или конъюгатов из гепатоцитов происходит главным образом через систему желчных ходов или после обратного всасывания в синусоиды – через почки. Считается, что поверхность гепатоцитов, обращенная к желчным капиллярам, высокопроницаема для макромолекул большинства органических веществ, вследствие чего многие вещества содержатся в желчи в концентрациях, близких таковым в крови. Однако для многих полярных ксенобиотиков (метаболитов, конъюгатов) выделение в желчь из гепатоцитов осуществляется путем активного транспорта против градиента электрохимического потенциала. Интенсивность желчной экскреции зависит также от соотношений между константами связывания ксенобиотиков с белками гепатоцитов и плазмой крови.
Большинство ксенобиотиков, как отмечалось, в результате метаболизма становятся более гидрофильными, поступают в плазму крови, откуда они удаляются почками с мочой. "Кооператив" печень - почки играет важнейшую роль в обезвреживании и выведении из организма большинства ксенобиотиков. Вещества более гидрофобные или с большой молекулярной массой (>300) чаще выводятся с желчью в кишечник и затем удаляются с калом (рис. 7.9).
Скорость выведения определяет распределение ксенобиотика. Например, распределение метилртути в организме происходит значительно быстрее, чем ее выведение. Это приводит к длительному удерживанию в мозге и соответственно длительному нарушению деятельности ЦНС.
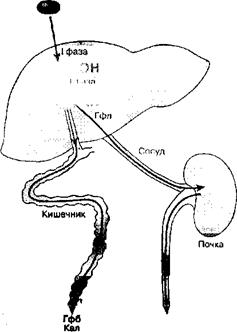 |
| Рис. 7.9. Метаболизм и выведение ксенобиотиков из организма: КсБ- ксенобиотик; R-радикал, ис-пользуемый при конъюгации {глутатион, глюкуро-нил идр,}; Гфб-гидрофобные и Гфл-гидрофиль-ные метаболиты ксенобиотиков, М - молекуляр-ная масса |
У растений нет специализированных путей поступления и выведения ксенобиотиков. Поступление чужеродных веществ в растения происходит главным образом через корни и листья. Особенности строения корня определяют пути и механизмы поступления ксенобиотиков в растения.
Поступление в корни органических ксенобиотиков из водных растворов, как правило, происходит в две фазы: первая фаза – это быстро протекающая диффузия в апопласт; вторая – медленное продолжительное поступление, при котором количество накапливаемого ксенобиотика прямо пропорционально времени экспозиции. Однако накопление в тканях органических ксенобиотиков регулируется их метаболическим превращением, поэтому процессы поступления ксенобиотиков имеют более сложный вид, чем это следует из вышесказанного.
В корневую систему растений поступает весьма широкий спектр гидрофильных и липофильных органических молекул ксенобиотиков (алифатические, ароматические и гидроароматические углеводороды, спирты, фенолы, амины, гетероциклические соединения и др.); причем отмечается поступление даже таких чужеродных соединений, которые обладают исключительно низкой растворимостью в воде, например полициклических углеводородов.
Весьма значительная часть ксенобиотиков поступает в растение через листья. Экзогенные соединения, содержащиеся в атмосфере или атмосферных осадках, в первую очередь контактируют с листвой растений. Более того, обработка растений различными пестицидами, регуляторами роста и т. д. зачастую производится путем опрыскивания или опыливания, т. е. в первую очередь происходит их контакт с листьями.
Ксенобиотик проникает в ткань листа через устьица или кутикулу. Через кутикулу соединения диффундируют медленнее, чем через устьица. Однако из водных растворов поступление ксенобиотиков через устьица, по мнению ряда исследователей, неэффективно, поскольку высокое поверхностное натяжение воды приводит к образованию у входа в устьичную щель выпуклого мениска, что препятствует поступлению экзогенного соединения.
Если в вопросе о проницаемости устьиц для водных растворов ксенобиотиков имеются разногласия, то поступление их через кутикулу сомнений не вызывает. Хотя кутикула проницаема и для гидрофильных молекул, но, являясь гидрофобной, она лучше пропускает липофильные ксенобиотики.
В последующем распределении ксенобиотиков в тканях и органах растений большую роль играют сосуды ксилемы и флоэмы. Ксенобиотики, переносимые по сосудам ксилемы (например, ряд гербицидов), поступая в корни растений, быстро создают фитотоксические концентрации в наземных органах растений. В то же время очень редко отмечается аккумуляция флоэмнобильных ксенобиотиков в корнях при поступлении их через листья. Такая ситуация обусловлена главным образом экскрецией чужеродных веществ в ризосферу.
Выделение ксенобиотиков через листья – довольно редкое явление, что, возможно, объясняется низкой экскретируемой их концентрацией в филлосфере; последнее затрудняет их достоверное количественное определение. В качестве примера можно назвать выделения фенола листьями растений Scirpus lacustris.
