Задания на контрольную работу
Таблица 1
| Код специальности | № заданий |
| CиУН: 270102 ; 270104 ; 270105; 270106 ; 270115 | 1-20; 41-60; 61-80; 81-100; 121-140; 141-160 |
| 161-180; 181-200; 221-240; 241-260; 281-300 | |
| КТАС: 220201 | 1-20; 41-60; 61-80; 121-140; 141-160; 181-200; 201-220; 241-260; 281-300 |
| МА и ТБ: 220301 | 1-20; 41-60; 61-80; 121-140; 141-160; 161-180; 181-200; 201-220; 281-300 |
| МА и ТБ: 151001; 151002; 190601;190603 140401;140504 | 1-20; 41-60; 61-80; 101-120; 121-140; 141-160; 181-200; 201-220; 241-260; 281-300 |
| МА и ТБ: 260601 | 1-20; 41-60; 61-80; 121-140; 101-120; 141-160; 181-200; 201-220; 241-260; 281-300 |
| Э и УБ: | 1-20; 21-40; 41-60; 61-80; 81-100; 101-120; 121-140; 141-160; 181-200; 221-240; 241-260; 281-300 |
| ХНСК: | 1-20; 21-40; 41-60; 61-80; 81-100; 121-140; 141-160; 181-260 |
| Выполняется по му[10]. Весь комплект заданий включает: зад.1 (в.1.1-1.9), зад. 2 (в. 2.1-2.5), зад. 3 (в. 3.1-3.4) Варианты заданий выдаются преподавателем! | |
| НГ и Э: | 1-20; 20-41; 41-60; 61-80; 181-200; 221-240; 241-260; 261-280; 281-300 |
| НГ и Э: 140101; 140104 | 1-20, 21-40, 41-60, 61-80, 81-100, 101-120, 121-140, 141-160; 161(а)-180(б), 181-200, 201-220, 221-240, 241-260, 261-280, 281-300 |
| НГ и Э: 130503; 130501; 130504; 130602 (студенты ЗиДО и 2 высшее образование) | Выполняется по настоящему му (ч. I): 1-20; 21-40; 41-60; 61-80; 81-100; 101-120; 161-180 |
| Выполняется по настоящему МУ, ч. I: 121-140; 141-160; 181-200; 221-240; 241-260 и по МУ, ч. II [9]: 1-6 Варианты заданий выдаются преподавателем! | |
| НГ и Э: 130503; 130501; 130504;130602 (студенты МИППС) | Выполняется по настоящему му, ч. I: 1-20; 21-40; 41-60; 61-80;81-100; 101-120; 121-140; 141-160; 161-180;181-200; 201-220; 221-240; 241-260; 280-300 |
Задания 1-20 (таблица 2)
Тема 1. Периодические закон и система элементов Д.И. Менделеева
Пример.
Составьте электронную и электронно-графическую формулу, укажите валентные электроны, определите степени окисления серы и напишите возможные соединения этого элемента с водородом и кислородом.
Решение. Напишем электронно-графические формулы для атома серы в нормальном и возбужденном состояниях: S, порядковый номер 16, третий период, шестая группа, главная подгруппа.
1) Электронная формула: 16S 1s2 2s22p63s23p4
(…3s23p4 - валентные электроны)
2) Электронно-графическая формула.
S s p d В=II
| ↑↓ | ↑↓ | ↑ | ↑ |
Степень окисления +2 и –2.
S* s p d В=IV
| ↑↓ | ↑ | ↑ | ↑ | ↑ |
Степень окисления +4
S* s p d В=VI
| ↑ | ↑ | ↑ | ↑ | ↑ | ↑ |
Степень окисления + 6
Таким образом сера может проявлять степени окисления 0, (+2), +4, +6, -2.
С кислородом сера образует кислотные оксиды состава: S+4O2-2,
S+6O3-2. С водородом: H2+1S-2.
Контрольные задания.
Для указанных в таблице 2 элементов составьте электронные и электронно-графические формулы. Укажите валентные электроны и степени окисления. Напишите формулы возможных соединений этих элементов с кислородом и водородом. Укажите характер оксидов, уравнениями реакций докажите их важнейшие химические свойства и изобразите их графические формулы.
Таблица 2
| № | Элементы | Поясните, |
| Ca, Sc | почему эти элементы расположены в одном периоде, в разных группах и подгруппах? | |
| Si, Ti | почему эти элементы стоят в разных периодах, в одной группе, но в разных подгруппах? | |
| P, Al | почему эти элементы стоят в одном периоде, в разных группах, но в одних подгруппах? | |
| Р, V | почему эти элементы стоят в разных периодах, в одной группе, но в разных подгруппах? | |
| Fe, Сr | у оксида железа (II) или у оксида хрома(II) сильнее выражен основной характер? | |
| Fe, Cr | у какого оксида и почему сильнее выражены кислотные свойства: FeO3 и CrO3? | |
| S, Se | почему эти элементы стоят в разных периодах, в одной группе и подгруппе? | |
| C, Si | У какого элемента и почему энергия ионизации больше? | |
| Ge, Zr | у какого оксида и почему сильнее выражены основные свойства: GeO2 и ZrO2? | |
| Mg, P, Al | как и почему изменяются кислотно-основные свойства высших оксидов в ряду магний, алюминий, фосфор? | |
| S, Al | y какого оксида и почему сильнее выражены кислотные свойства: SO2 и Al2O3? | |
| Al, S | у какого оксида и почему сильнее выражены кислотные свойства Al2O3 и SO3? | |
| Mn, Cl | почему эти элементы стоят в разных периодах, в одной группе, но в разных подгруппах? | |
| Ga, As | у какого оксида и почему сильнее выражены основные свойства: Ga2O3 и As2O3? | |
| Ti, Ge | у какого оксида и почему сильнее выражены основные свойства: TiO и GeO? | |
| Ti, Hf | укажите, у какого оксида и почему сильнее выражены основные свойства: Ti2O3 и Hf2O3? | |
| №15 и №28 | объясните, почему фосфор проявляет отрицательную степень окисления, а никель нет? | |
| №21 и №31 | укажите, к какому семейству они относятся, и объясните, почему они стоят в одном периоде, в одной группе, но в разных подгруппах? | |
| №33 и №23 | объясните, почему мышьяк образует газообразное водородное соединение, а ванадий не образует? | |
| №34 и №74 | почему эти элементы стоят в разных периодах, в одной группе, но в разных подгруппах? |
Тема 2. Химическая связь и строение молекул
Задания 21-40 (таблица 3)
Пример:
Определите тип химических связей в молекулах Br2, HBr, KBr. Приведите схемы перекрывания электронных орбиталей при образовании ковалентных связей в указанных молекулах.
Решение:
Br2: молекула брома образована из атомов одного элемента. Электроотрицательность брома равна 2,8 (таблица 18), поэтому Δ электроотрицательности = 2,8 – 2,8 = 0, следовательно, связь в молекуле брома Br2 –ковалентная неполярная, (Br- Br).
HBr: Δ электроотрицательности = 2,8 - 2,1 = 0,7, т.е. <0,7 => ковалентная полярная связь, связующая электронная пара смещена в сторону атома брома (Hδ+→Brδ-). Поэтому атом водорода приобретает эффективный положительный заряд, а брома – эффективный отрицательный.
KBr : Δ электроотрицательности = 2,8 - 0,91 = 1,89, т.е.>1,7 => связь преимущественно ионная, (K-Br).
У атома брома валентными являются электроны четвертого энергетического уровня: …4s24p5,
s p
| ↑↓ | ↑↓ | ↑↓ | ↑ |
В=I
неспаренный электрон находится на р-орбитали, электронная орбиталь имеет форму гантели.
Образование химической связи в молекуле Br2 можно отобразить схемой:

 |  |
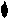
 + →
+ →
Br Br Br — Br
У атома водорода валентными является 1s-электрон, его электронная орбиталь имеет сферическую форму.
Схема образования химической связи в молекуле HBr.
 |  | ||||
 | |||||

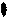
 + →
+ →
H Br H — Br
Контрольные задания
Определите тип химических связей в молекулах, указанных в таблице 3. Изобразите схемы перекрывания валентных орбиталей при образовании ковалентных связей в выделенных молекулах. (При необходимости используйте таблицы 15 – 19).
Таблица 3
| № | Соединения | Поясните, |
| РСl3; HCl | в чем сущность образования ковалентной связи? Какая из следующих связей полярна: а) Р–Cl; б) Н–Сl? | |
| CsF, CaH2 | что называется полярностью химической связи. Ответ поясните, исходя из теории строения атома. | |
| РН3, Н2 | в чем сущность механизма образования ковалентной неполярной связи? | |
| KCl, NH3 | в чем сущность донорно-акцепторного механизма образования ковалентной связи? | |
| F2, H2O | в чем сущность образования ковалентной связи? Какая из следующих связей полярна: а) F–F; б) O–H? | |
| KCl, КI | что называется длиной химической связи? Как изменяется длина связи в указанных молекулах? | |
| СН4, АlCl3 | что такое гибридизация? Определите типы гибридизации в указанных молекулах | |
| Аl(OH)3, С2Н4 | что такое направленность ковалентной связи? Механизм образования π- связи. | |
| NaCl, H2 | что такое направленность ковалентной связи? Механизм образования σ- связи. | |
| HCOH, CCl4 | сколько σ- и π-связей образует атом углерода в выделенной молекуле? Какова его степень окисления? | |
| CH3COOH, CH4 | сколько σ- и π-связей образует атом углерода в выделенной молекуле? Какова его степень окисления? | |
| C2H5OH, СНСl3 | сколько σ- связей образует атом углерода в выделенной молекуле? Каковы его валентность и степень окисления? | |
| NCl3, MgCl2 | что такое SP – гибридизация. Укажите молекулу с этим типом гибридизации. | |
| H2S , H2Se | в какой из указанных молекул значение дипольного момента больше? Ответ поясните. | |
| СН3ОН, Н2О | какую химическую связь называют водородной? В каких случаях она осуществляется? | |
| SiCl4, MgCl2 | что такое SP3 – гибридизация. Укажите молекулу с этим типом гибридизации. | |
| АlCl3 , SiCl4 | что такое SP2 – гибридизация. Укажите молекулу с этим типом гибридизации. | |
| H2O , H2S | в какой молекуле связь более полярна? Укажите направление дипольных моментов в этих молекулах. | |
| KF, К2S | какую химическую связь называют ионной? Покажите механизм ее образования. По каким свойствам ионная связь отличается от ковалентной? | |
| NaAlO2, CH3Cl | сколько σ- и π-связей образует атом алюминия в выделенной молекуле? Какова его степень окисления? |
Тема 3. Энергетика химических процессов
Задания 41-60 (таблица 4)
Пример.
Реакция горения этана выражена термодинамическим уравнением:
C2H6(г) + 3,5 O2(г) = 2 CO2(г) + 3 H2O(ж);
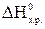 = -1559,87 кДж/моль. Вычислите энтальпию образования этана, если известны стандартные энтальпии образования:
= -1559,87 кДж/моль. Вычислите энтальпию образования этана, если известны стандартные энтальпии образования:
CO2 (г) 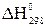 = -393,57 кДж/моль
= -393,57 кДж/моль
H2O(ж) 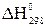 = -285,84 кДж/моль
= -285,84 кДж/моль
Решение:Используя следствие из закона Гесса, можно записать:
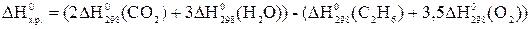 , откуда
, откуда 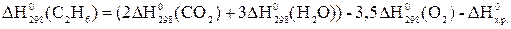
Подставим табличные значения термодинамических величин и зная, что энтальпии образования простых веществ равны нулю, получаем:
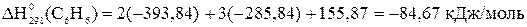
Реакция горения этана экзотермическая т.к. 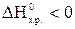
Контрольные задания.
На основании стандартных энтальпий образования и абсолютных стандартных энтропий (таблица 20) соответствующих веществ вычислите изменение энергии Гиббса и температуру равновесного состояния указанной в таблице 4 реакции, а так же возможность протекания данной реакции в прямом направлении при стандартных условиях.
Таблица 4
| № | Уравнение |
| CO2(г) + 4H2(г) = CH4(г) + 2H2O(ж) | |
| Fe2O3(к) + 3H2(г) = 2Fe(к) + 3H2O(г) | |
| PCl5(г) = PCl3(г) + Cl2(г) | |
| CO(г) + 3H2(г) = CH4(г) + H2O(г) | |
| C2H4(г) + 3O2(г) = 2H2O(ж) + 2CO2(г) | |
| 2CH4(г) = C2H2(г) + 3H2(г) | |
| C(к) + O2(г) = CO2 (г) | |
| Аl2O3(к) + H2(г) = Al(к) + H2O(г) | |
| N2(г) + 3H2(г) = 2NH3(г) | |
| 2CO(г) + O2(г) = 2CO2(г) | |
| CO(г) + H2O(ж) = CO2(г) + H2(г) | |
| CO(г) + Cl2(г) = 2COCl2(г) | |
| 2C2H6(г) + 7O2(г) = 6H2O(ж) + 4CO2(г) | |
| CaO(к) + H2O(ж) = 2Ca(OH)2(к) | |
| CaCO3(к) = CaO(к) + CO2(г) | |
| 2H2O2(ж) = 2H2O(ж) + O2(г) | |
| О2(г) +4HCl(г) = 4HCl(г) + 2H2O(ж) | |
| NH4Cl(к) + NaOH(к) = NaCl(к) + NH3(г) + H2O(г) | |
| 2ZnS(к) + 3O2(г) = 2ZnO(к) + 2SO2(г) | |
| 2C2H2(г) + 5O2(г) = 2H2O(ж) + 4CO2(г) |
Тема 4. Химическая кинетика, катализ и химическое равновесие
Задания 61 – 80 (таблица 5)
Пример 1.
Как изменится скорость химической реакции между азотом и водородом N2(г) + 3H2(г) 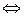 2NH3(г), если, не изменяя температуру, уменьшить давление системы в 2 раза?
2NH3(г), если, не изменяя температуру, уменьшить давление системы в 2 раза?
Решение:По закону действующих масс
V = k[N2][H2]3.
Для уменьшения давления системы в 2 раза, объем ее следует увеличить в 2 раза. При этом во столько же раз уменьшиться концентрация каждого из участвующих в реакции компонентов. Концентрация азота будет равна [N2]/2 и водорода [H2]/2. Скорость химической реакции при этих условиях будет:
V’ = k[N2/2][H2/2]3 = 1/16k[N2][H2]3
и соотношение скоростей
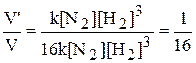
При уменьшении давления в системе в 2 раза скорость химической реакции между азотом и водородом уменьшиться в 16 раз.
Пример 2.
Напишите выражение константы равновесия для гетерогенной системы
SO2(г) + 2H2S(г) 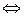 3S(т) + 2H2O(г)
3S(т) + 2H2O(г)
Как следует изменить концентрацию и давление, чтобы сместить равновесие в сторону обратной реакции?
Решение:Концентрация твердого вещества в уравнении закона действующих масс не учитывается, следовательно:
Vпр = k1[SO2][H2S]2
Vобр = k2[H2O]2
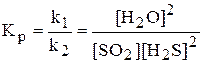
Руководствуясь принципом Ле-Шателье, который гласит: «Если на систему, находящуюся в равновесии, оказать какое-либо воздействие, то в результате протекающих в ней процессов равновесие сместится в направлении, уменьшающем это воздействие», приходим к выводу, что для смещения равновесия в сторону обратной реакции надо увеличить концентрацию водяного пара или уменьшить концентрацию SO2 и H2S.
Контрольные задания
Для всех заданий в таблице 5 дайте обоснованный ответ, а для задач с определением направления смещения равновесия, напишите выражение константы равновесия (Кр).
Таблица 5
| № | Условие задания |
Как изменится скорость прямой химической реакции Н2(г) + Сl2(г) 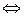 2 HCl (г), если, не изменяя температуру, уменьшить давление системы в 3 раза? 2 HCl (г), если, не изменяя температуру, уменьшить давление системы в 3 раза? | |
Как изменится скорость химической реакции между кислородом и водородом 2Н2(г) + О2(г) 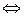 2H2О (г), если, не изменяя температуру, уменьшить концентрацию исходных веществ в 4 раза? 2H2О (г), если, не изменяя температуру, уменьшить концентрацию исходных веществ в 4 раза? | |
Во сколько раз надо увеличить концентрации СО, чтобы скорость прямой химической реакции 2СО(г) 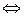 С(т)+СО2(г) увеличилась в 4 раза? С(т)+СО2(г) увеличилась в 4 раза? | |
Во сколько раз надо увеличить концентрации SО2, чтобы скорость прямой химической реакции 2SО2(г) + O2(г) 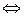 2SО3(г) увеличилась в 2 раза? 2SО3(г) увеличилась в 2 раза? | |
Действием каких факторов можно сместить равновесие в сторону продуктов реакции Н2(г) + 3N2 (г) 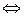 2NН3(г)? ∆Н = -92 кДж/моль 2NН3(г)? ∆Н = -92 кДж/моль | |
Во сколько раз надо увеличить концентрации О2, чтобы скорость прямой химической реакции 2SО2(г) + O2(г) 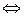 2SО3(г) увеличилась в 3 раза? 2SО3(г) увеличилась в 3 раза? | |
Действием каких факторов можно сместить равновесие химической реакции N2(г) +O2 (г) 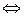 2NO(г) вправо? ∆Н =180 кДж/моль? 2NO(г) вправо? ∆Н =180 кДж/моль? | |
| Как следует изменить концентрацию, температуру и давление в реакции горения углерода, чтобы сместить равновесие в сторону обратной реакции? | |
Во сколько раз изменится скорость прямой реакции А(г) + 2В(г) 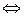 АВ2 (г) при увеличении давления в 2 раза? АВ2 (г) при увеличении давления в 2 раза? | |
Действием каких факторов можно сместить равновесие в реакции N2 (г) + 3Мg(т) 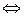 Mg3N2(т) в сторону продуктов реакции? ∆Н < 0 Mg3N2(т) в сторону продуктов реакции? ∆Н < 0 | |
Действием каких факторов можно сместить равновесие в сторону продуктов реакции С2Н4 + 3О2 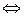 2СО2 + 2Н2О? ∆Н < 0 2СО2 + 2Н2О? ∆Н < 0 | |
| Во сколько раз уменьшится скорость химической реакции при уменьшении температура с 36оС до 28оС, если температурный коэффициент равен 2? | |
Действием каких факторов можно сместить равновесие в химической реакции N2(г) + 6Li(т) 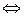 2Li3N(т)+ 39 кДж/моль в сторону продуктов реакции? 2Li3N(т)+ 39 кДж/моль в сторону продуктов реакции? | |
| Во сколько раз увеличится скорость химической реакции при изменении температуры от 35 до 75оС, если температурный коэффициент равен 2? | |
Действием каких факторов можно сместить равновесие химической реакции Fe3O4(т) +4CO(г) 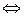 3Fe(т) + 4CO2(г) вправо? ∆Н < 0. 3Fe(т) + 4CO2(г) вправо? ∆Н < 0. | |
Действием каких факторов можно сместить равновесие в сторону прямой химической реакции Fe(т) +2HCl(ж) 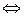 FeCl2(ж) + Н2(г)? ∆Н > 0 FeCl2(ж) + Н2(г)? ∆Н > 0 | |
| Скорость химической реакции увеличилась в 81 раз при увеличении температуры на 30оС. Определите величину температурного коэффициента. | |
| Чему равен температурный коэффициент, если при увеличении температуры на 30оС скорость химической реакции возрастает в 27 раз? | |
| Во сколько раз увеличится скорость химической реакции при повышении температуры на 45оС, если температурный коэффициент равен 2? | |
| Чему равен температурный коэффициент, если при увеличении температуры на 30оС скорость химической реакции возрастает в 21 раз? |
Тема 5. Истинные растворы и способы выражения концентраций
растворов
Задания 81 – 100 (таблица 6)
Контрольные задания
Решите задачи, приведенные в таблице 6. Дайте полное объяснение хода решения, используя таблицу 21.
Таблица 6
| № | Условие задания |
| Определите массовую долю глюкозы (C6H12O6) в растворе, содержащем 280 г воды и 40 г глюкозы. | |
| 1 см3 25% раствора NaCl содержит 0,458 г растворенного вещества. Какова плотность этого раствора? | |
| Сколько граммов 30% раствора NaCl надо добавить к 300 г воды, чтобы получить 10% раствор соли? | |
| Определите массу нитрата натрия необходимую для приготовления 300 см3 0,2 М раствора. | |
| Какой объем 6 М раствора соляной кислоты нужно взять, чтобы получить 25 см3 2,5 М раствора НСl? | |
| Вычислите молярную концентрацию и молярную концентрацию эквивалента 20% раствора хлорида кальция плотностью 1,178 г. | |
| Чему равна молярная концентрация эквивалента 30% раствора NaOH плотностью 1,328 г/см3? К 1 л этого раствора прибавили 5 л воды. Вычислите процентную концентрацию полученного раствора. | |
| К 3 л 10% HNO3 (1,054 г/см3) прибавили 5 л 2% раствора HNO3 (1,009 г/см3). Вычислите массовую долю и его молярную концентрации. | |
| Вычислите молярную и моляльную концентрации 20,8% раствора HNO3 плотностью 1,12 г/см3. Сколько граммов кислоты содержится в 4 л этого раствора? | |
| Вычислите молярную и моляльную концентрации 16% раствора хлорида алюминия плотностью 1,149 г/см3. | |
| Смешали 10 см3 20% раствора HNO3 (1,2 г/см3) и 100 см3 30% раствора HNO3 (1,22 г/см3). Вычислите массовую долю полученного раствора. | |
| Какой объем 50% раствора КОН (1,5 г/см3) нужно взять для приготовления 1 дм3 6% раствора КОН (1,042 г/см3) | |
| Какой объем 0,3 М раствора соляной кислоты необходимо взять для нейтрализации 40 см3 раствора гидроксида натрия, содержащего 0,32 г вещества? | |
| Сколько см3 0,1 М раствора соляной кислоты необходимо взять для нейтрализации 1дм3 25% раствора гидроксида калия (1,2 г/см3)? | |
| Сколько грамм HNO3, содержалось в растворе, если на нейтрализацию этого раствора потребовалось 35 см3 0,1 М раствора NaOH? | |
| Какую массу NaNO3 нужно растворить в 300 г воды, чтобы получить 20% раствор соли? | |
| Смешали 300 г 20% раствора с 500 г 46% раствора хлорида натрия. Определите массовую долю полученного раствора. | |
| Определите массовую долю раствора, полученного смешиванием 247 граствора с массовой долей 62% и 145 г раствора с массовой долей 18%. | |
| Из 700 г 62% раствора серной кислоты выпариванием удалили 200 г воды. Определите массовую долю полученного раствора. | |
| Из 10 кг 20% (по массе) раствора при охлаждении выделилось 400 г растворенного вещества. Чему равна массовая доля этого вещества в оставшемся растворе? |
Тема 6. Физические свойства растворов
Задания 101 – 120 (таблица 7)
Пример.
Вычислите температуры кристаллизации и кипения 2% водного раствора глюкозы (С6Н12О6).
Решение:Согласно 2 закону Рауля понижение температуры кристаллизации и повышение температуры кипения раствора (Δt) по сравнению с температурами кристаллизации и кипения растворителя выражаются уравнением:
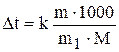 , (1)
, (1)
где k-криоскопическая или эбуллиоскопическая постоянная.
Для воды они соответственно равны 1,86 и 0,52о (таблица 23);
M и m – соответственно масса растворенного вещества и его мольная масса;
m1 – масса растворителя.
Понижение температуры кристаллизации 2% раствора глюкозы С2Н12О6 находим из формулы (1).
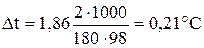 .
.
Вода кристаллизируется при 0оС, следовательно, температура кристаллизации равна 0 – 0,21= – 0,21оС.
Из формулы (1) находим и повышение температуры кипения 2% раствора
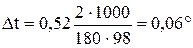
Вода кипит при 100оС, следовательно, температура кипения этого раствора 100 + 0,06 оС = 100,6оС.
Контрольные задания.
Решите задачи, приведенные в таблице 7. Дайте полное объяснение хода решения, используя таблицу 22.
Таблица 7
