Опреснение воды вымораживанием
Тема 1. Введение
1.1 Химическое производство и проблема окружающей среды.
Показатели качества воды:
• Природная вода
• Техническая вода
• Вода, идущая на хозяйственно-питьевые нужды
Техническая вода - это вода, идущая для питания паровых котлов, для охлаждения двигателей внутреннего сгорания, конденсаторов. Качество воды является важной особенностью безаварийной работы котлов.
Вода нормируется по следующим показателям:
1. Общее солесодержание:
– не должно превышать 1 г/л;
2. Сухой остаток:
– количество растворимых веществ в 100 мл профильтрованной воды и последующего высушивания при 110-120° С (мг/л);
3.Содержание коррозионно-активных газов в воде:
– 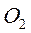 ,
, 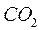 ,
, 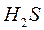 ,
, 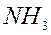 первые 3 - коррозионно-агрессивные: обуславливающие или способствующие коррозии. Удаление газов из воды называется дегазацией;
первые 3 - коррозионно-агрессивные: обуславливающие или способствующие коррозии. Удаление газов из воды называется дегазацией;
4. Активная реакция воды:
– определяет PH среды. Водопроводная вода должна иметь РН≈7. Техническая РH 6,5 - 9,5
5. Мутность и цветность воды:
– обусловлена содержанием взвешенных частиц (песка, глины, илистых веществ органического происхождения). Для осветления воды ее:
а) отстаивают;
б) фильтруют;
Отстаивание воды является естественным процессом, при котором взвешенные в воде грубодисперсные частицы с плотностью, превышающей плотность воды осаждаются под действием силы тяжести. Для удаления из воды коллоида дисперсных частиц (они не осаждаются в осветлителях и не задерживаются в осветлительных фильтрах) необходимо укрупнение этих частиц коагулированием. Для этого воду обрабатывают химическими веществами коагулянтами ( 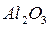 ,
, 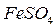 ,
, 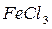 ).
).
Цветность воды зависит еще от того, где расположены озера и реки. Цветность определяется по шкале цветности в сравнении с эталонной водой.
6. Жесткость воды:
– обусловлена содержанием в ней растворимых солей ионов 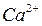 и
и 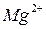 , Различают два вида жесткости: временную (гидрокарбонатную) и постоянную (некарбонатную). Временная жесткость вызывается присутствием в воде гидрокарбонатов кальция
, Различают два вида жесткости: временную (гидрокарбонатную) и постоянную (некарбонатную). Временная жесткость вызывается присутствием в воде гидрокарбонатов кальция 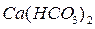 и магния
и магния 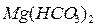 . Временная жесткость может быть легко устранена путем нагревания.
. Временная жесткость может быть легко устранена путем нагревания.
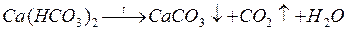
Постоянная жесткость вызывается наличием в воде хлоридов 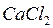 ,
, 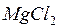 , сульфатов
, сульфатов 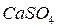 ,
, 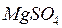 , силикатов
, силикатов 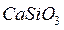 ,
, 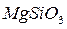 и других некарбонатных солей. Жесткость измеряется в (мг-экв/л)
и других некарбонатных солей. Жесткость измеряется в (мг-экв/л) 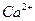 ,
, 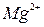 или (
или ( 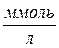 )
)
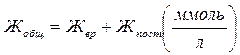 или
или 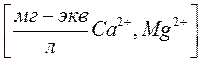
Исходя из единицы жесткости:
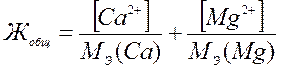 , где [ ] – концентрация ионов.
, где [ ] – концентрация ионов.
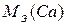 =
= 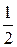
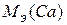 =
= 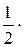 40 = 20 мг/моль
40 = 20 мг/моль
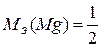
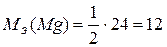 мг/моль
мг/моль
По величине общей жёсткости воду делят на следующие группы:
1. мягкая 0-3 ммоль/л 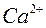 ,
, 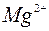 ;
;
2. жёсткая 3-11,8 ммоль/л 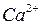 ,
, 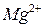 ;
;
3. очень жёсткая более 12 ммоль/л 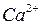 ,
, 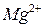 ;
;
В судовых котлах допустимая жёсткость не более 0,0355 ммоль/л.
7. Соленость воды
– соленость воды обуславливается содержанием в ней растворимых хлоридов 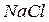 ,
, 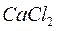 ,
, 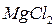 ,
, 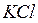 . Определение солености сводится к определению иона
. Определение солености сводится к определению иона 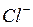 . Определение производится путем титрования
. Определение производится путем титрования 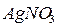 в присутствии индикатора хромата калия.
в присутствии индикатора хромата калия.
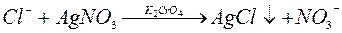
Хромат калия - индикатор, который позволяет установить окончание реакции, т. е. практически полное осаждение из раствора хлор-иона. После того, как 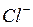 -ион будет полностью осаждён дальнейшее прибавление
-ион будет полностью осаждён дальнейшее прибавление 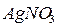 вызовет образование малорастворимой соли хромата серебра.
вызовет образование малорастворимой соли хромата серебра.
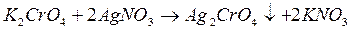
Выражается солёность в мг/л 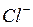 и °Б (градус Брандта)
и °Б (градус Брандта)
1°Б соответствует содержанию хлоридов, эквивалентному 10 мг 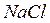 в 1 литре
в 1 литре 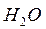 ;
;
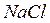 /58,5 - 35,5(мг)
/58,5 - 35,5(мг) 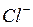 ;
;
10 – X;
Х = 6,06 мг/л 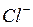 ;
;
1°Б = 6,06 мг/л 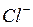 ;
;
Солёность ухудшает качество 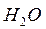 ,
, 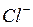 разрушают стенки котлов и паропроводящую систему. Допустимая соленость до 1°Б.
разрушают стенки котлов и паропроводящую систему. Допустимая соленость до 1°Б.
8. Щёлочность
– обуславливается содержанием в воде солей сильных оснований и слабых кислот, при гидролизе которых образуется щелочная среда.
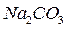 ,
, 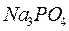 ,
, 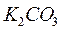 ,
, 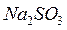 ;
; 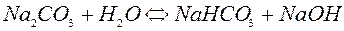
Определяется щёлочность щелочным числом.
Щелочное число = 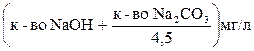 ;
;
4,5 – опытный коэффициент, учитывающий частичный гидролиз соли. Щёлочность воды для питания котлов 150-300 мг/л.
Проверка воды на содержание газов. Дегазация.
Процесс удаления газов из 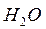 называется - дегазацией. Главную коррозионную опасность для некоторых металлических конструкций представляет растворённый кислород:
называется - дегазацией. Главную коррозионную опасность для некоторых металлических конструкций представляет растворённый кислород:
1). Физические методы:
– При t=102-103° C;
– Пропуская через железный фильтр
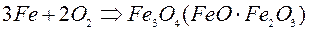
2). Добавляя химикаты:
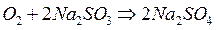
Для более глубокого удаления 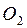

Удаление 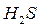 :
:
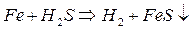 – забивает трубы;
– забивает трубы;
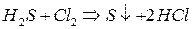
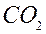 – удаляется продувкой котлов;
– удаляется продувкой котлов;
Удаление 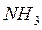 :
:
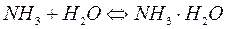 – и нейтрализуют
– и нейтрализуют 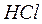
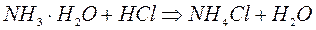
Умягчение воды.
• Физический метод - метод дистилляции (выпаривание) - осуществляется в выпарных аппаратах. Получают высокую степень очистки.
Недостаток метода - большой расход тепловой энергии ≈ 2250 кДж/кг выпариваемой воды. Для снижения этого расхода применяют 3-х корпусные вакуумные установки, на которых пар, полученный в первом выпарном аппарате, является греющим паром для второго и так далее.
Метод дистилляции используется в нашей стране на установках для опреснения морской воды (г. Шевченко) и на станциях для очистки засолёных природных вод.
Магнитная обработка - вода пропускается через систему постоянных магнитов. Механизм воздействия магнитного поля на воду не ясен. Можно полагать, что под влиянием магнитного поля происходит определенное изменение "структуры" водного раствора и достигается эффект умягчения воды. В настоящее время в СССР серийно выпускают устройства для магнитной обработки. На чистую воду (без примесей) магнитная обработка не влияет.
Во многих случаях физические методы экономически более выгодны, чем химические, более чисты экологически. Энергетические затраты не значительны.
• Химические методы.
Цель этих методов - осаждение накипиобразователей путём введения различных реагентов, т. е. умягчения - это удаление из 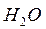 только солей жёсткости.
только солей жёсткости.
1. Известково-содовый:
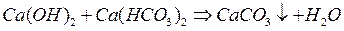
удаляются только соли временной жесткости
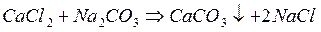
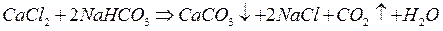
Этим методом устраняется временная (известь) и постоянная жесткость (сода). Однако в воде остается много ионов 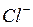 , коррозионно-активных ионов.
, коррозионно-активных ионов.
2. Фосфатный:
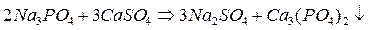
3. Пермутитный:
с помощью природных алюмосиликатов, имеющих в своем составе подвижный катион 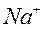 , способный обмениваться на катионы
, способный обмениваться на катионы 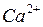 и
и 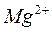 .
.
Формула:
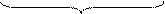
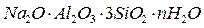 –
– 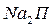
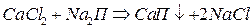
Недостатки химических методов умягчения 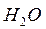 :
:
1. коррозионная агрессивность воды по отношению к оборудованию сохраняется;
2. такая вода не может применяться на парогенераторных установках, т.к. не полностью удаляются 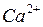 и
и 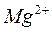 ;
;
Полное удаление всех солей достигается обессоливанием;
Методы опреснения воды
Метод ионного обмена
Основан на прохождении воды через слой специальных веществ - ионообменных смол (иониты).
Иониты - твердые высокомолекулярные соединения, содержащие в своем составе фиксированные и подвижные ионы, способные обмениваться на ионы, находящиеся в водном растворе. Иониты делятся на катиониты, применяемые для извлечения катионов и аниониты - обмен анионов.
Этот метод может быть использован для умягчения воды, обессоливания (деионизации). Также применяется для извлечения токсичных катионов тяжелых и цветных металлов и сточных вод.
Аниониты - это вещества, содержащие гидроксилфенольную группу
( 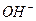 ,
, 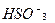 ,
, 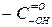 )
)
Катиониты - вещества, содержащие в своем составе активные группы:
первичные аминогруппы, 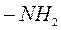 ;
;
вторичные аминогруппы, 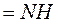 ;
;
третичные аминогруппы, 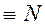 ;
;
Обмен ионами в анионитах:
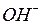 | 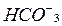 |
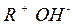 | 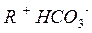 |
R - радикал с большим ионным весом.
Обмен ионами в катионитах:
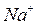 | 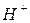 | 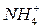 |
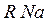 | 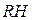 | 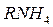 |
В качестве катионита используют искусственно полученные смолы на основе стирола.
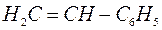 – стирол термостоек (t=120° - 140°), хранится под слоем воды. Но смолы очень дорогие.
– стирол термостоек (t=120° - 140°), хранится под слоем воды. Но смолы очень дорогие.
Реакции обмена катионитов:
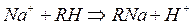
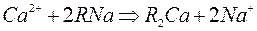
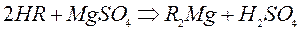
При катионировании происходит обмен всех катионов, находящихся в воде, на катионы водорода или натрия и т.д.
Реакции обмена анионитов:
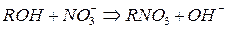
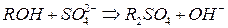
Обессоливание с помощью смол производится чаще по схеме: катионит-анионит.
Пусть вода содержит 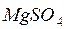 .
.
Обессолить ее:
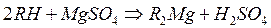
Получается подкисленная вода, которую пропускают через анионит:
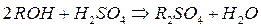
Полнота обессоливания этим методом зависит от скорости фильтрации и объемной емкости ионитов.
Иониты поглощают одновалентные ионы до тех пор, пока в них не замещены ионы 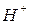 и
и 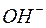 на другие ионы. После этого иониты подвергают регенерации. Регенерация катионита заключается в следующем: через слой отработанного катионита пропускают раствор
на другие ионы. После этого иониты подвергают регенерации. Регенерация катионита заключается в следующем: через слой отработанного катионита пропускают раствор 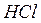 или
или 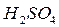 до тех пор, пока не будут замещены все катионы металлов в катионите на ионы водорода.
до тех пор, пока не будут замещены все катионы металлов в катионите на ионы водорода.
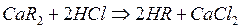
В настоящее время имеются установки, способные перерабатывать более 2 млн. 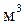 воды за сутки. Вода, прошедшая через такие ионообменники близка к дистиллированной, но обходится в несколько раз дешевле
воды за сутки. Вода, прошедшая через такие ионообменники близка к дистиллированной, но обходится в несколько раз дешевле 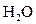 , полученной перегонкой.
, полученной перегонкой.
После регенерации производят отмывку избыточной кислоты чистой обессоленной водой до нейтральной реакции.
Аниониты регенерируются 3-5% раствором NaОН.
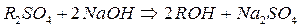
Регенерация щелочью проводится до тех пор, пока анионы кислот
полностью не будут замещены на ионы 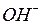 . После этого фильтр
. После этого фильтр
промывается и включается в общую схему водоподготовки.
Экономически по методу ионного обмена целесообразно перерабатывать воду с содержанием 1,5 г/л солей.
Ионирование может выполнять две функции:
а) Только катионирование - умягчение воды;
б) Катионирование и анионирование - обессоливание воды.
Электродиализ
Процесс удаления из растворов поляризованных веществ путем переноса их через мембрану в поле постоянного электрического тока, В такой системе возникает направленное движение ионов растворенных солей, а также ионов 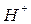 и
и 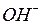 , причем катионы движутся к катоду, анионы - к аноду.
, причем катионы движутся к катоду, анионы - к аноду.
На катоде:
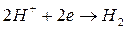
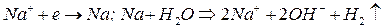
Анодные реакции:
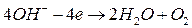
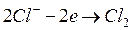
Для предотвращения переноса ионов 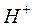 и
и 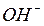 образующихся по реакциям, электродиализатор разделяют на отсеки с помощью специальных мембран, проницаемых только для катионов или только для анионов (рис.1.1).
образующихся по реакциям, электродиализатор разделяют на отсеки с помощью специальных мембран, проницаемых только для катионов или только для анионов (рис.1.1).
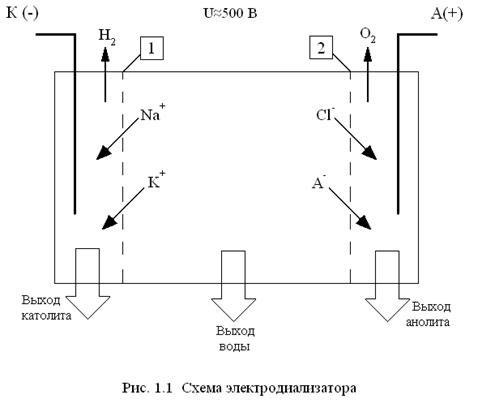 |
1 – катионитовая мембрана;
2 – анионитовая мембрана;
Расход электроэнергии на 1  воды Q=96500
воды Q=96500 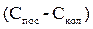
Метод обратного осмоса
Осмос - это самопроизвольная диффузия растворителя из менее концентрированного раствора в более концентрированный раствор через полупроницаемую перегородку. Если чистую воду отделить такой перегородкой от соленой воды, то молекулы воды проникнут в раствор, разбавляя его. Уровень раствора повысится (рис.1.2).
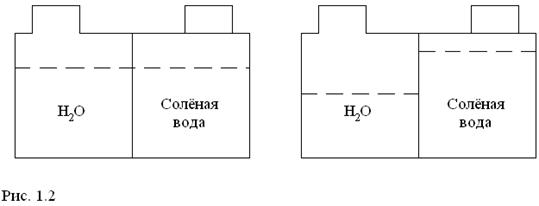
Схема самопроизвольной диффузии
Разница уровней в момент равновесия будет характеризоваться осмотическим давлением раствора. Зависит Росм от концентрации раствора. Если к раствору приложить давление большее, чем Росм, то будет наблюдаться явление обратного осмоса: вода из раствора будет переходить в направлении, обратном естественной диффузии (рис.1.3).
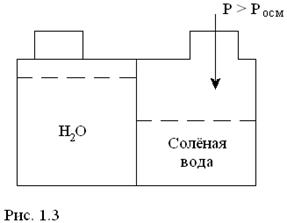
Схема опреснения воды методом обратного осмоса
Вода проходит через отверстия в 3,5 А, а молекулы солей через поры
более 5 А.
В качестве полупроницаемых мембран применяются пористый фарфор, пропитанный ферроцианидом меди (II) 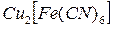
Стоимость получения пресной воды этим методом составляет 1 доллар за 16000 л.
Опреснение воды вымораживанием
Известно, что лед, образовывающийся при замерзании морской воды, почти не содержит солей.
Морская вода представляет собой раствор солей, и при замерзании воды и соли образуют различные кристаллографические структуры.
Если чистая вода замерзает при 0°, то морская вода с солесодержанием 35 г/л при t= - 1,85°. Этим по видимому обусловлен тот факт, что при замерзании морской воды в первую очередь образуются кристаллы пресного льда, а затем замерзает рассол, который в виде тонких оболочек покрывает эти кристаллы. При медленном замерзании получают более крупные кристаллы льда со значительно меньшими кристаллами рассола. Процесс таяния идет в обратной последовательности - сначала из морского льда стекает охлажденный рассол 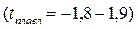 , а затем чистая вода.
, а затем чистая вода.
Опреснение воды вымораживанием состоит из трех основных операций; образования кристаллов льда, отделение их от рассола и плавление льда.
Такие установки разработали в Японии (1969). У нас спроектирована такая установка в Туркмении, производит 30 кг/час.
