Атом з певним зарядом ядра; 4 страница
 Урок № 9 Розрахунки за хімічними формулами
Урок № 9 Розрахунки за хімічними формулами
 1. Розрахуйте кількість речовини (моль) 3,01 *1023
1. Розрахуйте кількість речовини (моль) 3,01 *1023
| А | Б | В | Г |
молекул азоту N2:
А) 0,5 ;
Б) 1;
В) 1,5;
Г) 2.
2. Розрахуйте масу кисню(г) об’ємом 3,36 л (н.у.):
| А | Б | В | Г |
А) 3,7 ;
Б) 4,8 ;
В) 4,5 ;
Г) 5,07.
| А | Б | В | Г |
3. Розрахуйте об’єм (л) за н.у. водню речовини 2 моль:
А) 22,4;
Б) 11,2;
В) 44,8;
Г) 4,0.
| А | Б | В | Г |
4. Розрахуйте кількість молекул в 32 г сульфур (IV) оксиду:
а) 3,01*1023;
б) 6,02 *1023;
в) 12*1023;
г) 1,5 * 1023.
5. Виберіть твердження щодо відносної густини сірководню (Н2S) за воднем:
| А | Б | В | Г |
а) за воднем дорівнює 17;
б) за киснем більше 2;
в) за азотом дорівнює 2,43;
г) за повітрям дорівнює 1,6.
6. Встановіть відповідність між масою та кількістю речовини:
Маса речовини, г: Кількість речовини, моль:
| А | Б | В | Г | |
1. 196 г H2SO4; а) 2,0;
Г NaOH; б) 10,0;
ГNaCl в) 0,5;
4. 20г CaCO3 г)0,2.
7. Встановіть послідовність речовини для кисню згідно з ланцюжком
маса ( г) → кількість речовини (моль)→ об’єм (н.у.) (л)→ кількість молекул :
| А | Б | В | Г | |
а) 0,6 *10 23;
Б) 3,2 ;
В) 2,24 ;
Г) 0,1.

 Урок № 10
Урок № 10
Узагальнюючий урок
1. Заповніть таблицю:
| Назва речовини | Формула Речовини | Об’єм | Молярна маса | Кількість Речовини | Кількість Молекул | Маса |
| калій гідроксид | КОН | - | 0,5 моль | |||
| карбон (IV) оксид | 24*1023молекул | |||||
| сульфур (VI) оксид | 67,2 л | |||||
| хлоридна кислота | НСl | - | 71 г |
2. Яка маса, скільки молекул та яка кількість речовини в 11,2 л карбон (ІІ) оксиду :
| А | Б | В | Г |
А) 2,2 г, 0,3*1023, 0,05 моль;
Б) 44г, 6*1023, 1 моль;
В) 88 г, 12*1023, 2 моль;
Г) 22 г, 3*1023, 0,5 моль.
3. Яка маса і скільки молекул в
0,3 моль NaОН:
| А | Б | В | Г |
А) 8 г і 1,2*1023;
Б) 120 г і 18*1023;
В) 12г і 1,8*1023;
Г) 28 г і 3*1023.
Відповідь підтвердити розрахунками
| А | Б | В | Г | |
4. Встановіть відповідність між формулою газу та його відносною густиною за повітрям (відносна молекулярна маса повітря 29). Відповідь підтвердити розрахунками.
Формула газу Відносна густина за повітрям:
А) СО 1. 2,2;
Б) СО2 2. 0,97;
В) SO2 3. 1,52
Г) NО2 4. 1,59
 Урок № 11 Оксиди, їх назви і склад. Класифікація оксидів.
Урок № 11 Оксиди, їх назви і склад. Класифікація оксидів.
1. Серед запропонованих формул виберіть формули оксидів, кислот, основ, солей та запишіть їх у відповідний стовпчик таблиці –
MnO2, H2SO4, NaOH, Ca(OH)2, CuSO4, N2O5, HNO3, Al2(SO4)3:
| Оксиди | Кислоти | Основи | Солі |
2. Запишіть формули несолєтворних оксидів та дайте їм назви:
__________________________;
__________________________;
__________________________.
| Основні оксиди | Кислотні оксиди |
3. Серед запропонованих формул виберіть формули основних та кислотних оксидів –
BaO, CuO,N2O5, Na2O, Mn2O7, SO3:
4. Складіть формули оксидів:
а) нітроген (V) оксид _______________;
б) алюміній оксид___________________;
в) сульфур (VІ) оксид_______________;
г) станум (ІV) оксид_________________.
5. Встановіть відповідність між назвою та формулою оксиду:
Назва оксиду: Формула оксиду:
| А | ||||||
| Б | ||||||
| В | ||||||
| Г | ||||||
| Д | ||||||
| Е |
а) кальцій оксид; 1. CO;
б) карбон (ІV) оксид; 2. CaO;
в) карбон (ІІ) оксид; 3. CO2;
г) нітроген (І) оксид; 4. N2O;
д) натрій оксид; 5. Na2O.
е) калій оксид. 6. К2О.
Урок № 12 Кислоти, їх назви і склад. Класифікація кислот.
 1. Встановіть відповідність між назвою та формулою кислоти:
1. Встановіть відповідність між назвою та формулою кислоти:
| А | ||||||||
| Б | ||||||||
| В | ||||||||
| Г | ||||||||
| Д | ||||||||
| Е | ||||||||
| Є | ||||||||
| Ж |
Назва кислоти: Формула кислоти:
а) хлоридна; 1. H2S;
б) сульфатна; 2. H2CO3;
в) силікатна; 3. H2SiO3;
г) сульфітна; 4. HCl;
д) карбонатна; 5. H2SO4;
е) нітратна; 6. H2SO3;
є) сульфідна; 7. HNO3;
ж) ортофосфатна. 8. H3PO4.
2. З’єднайте формулу кислоти з її характеристиками, як це показано в прикладі:







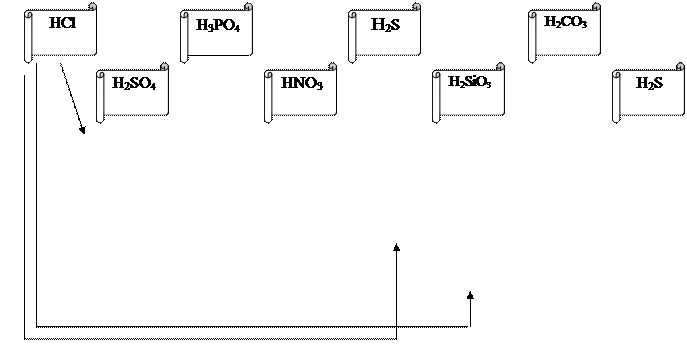 3. Визначити кількість речовини, число молекул , що містяться в 49 г сульфатної кислоти.
3. Визначити кількість речовини, число молекул , що містяться в 49 г сульфатної кислоти.
4. Визначити масу та число молекул , що містяться в 0,5 моль нітратної кислоти.
