Термокаталитические превращения
По характеру взаимодействия катализатора с реагирующими веществами и по типу промежуточных продуктов различают окислительно-восстановительные и кислотно-основные реакции и соответственно катализаторы.
Многие промышленные катализаторы являются бифункциональными, так как окислительно-восстановительный катализатор наносят на кислотный носитель. С другой стороны, многие сульфиды и окислы сами по себе обладают и окислительно-восстановительной, и кислотно-основной активностью.
Механизм действия катализаторов
Окислительно-восстановительного типа
В окислительно-восстановительных реакциях каталитическое воздействие обусловлено, по-видимому, образованием гомеополярных связей адсорбированных молекул реагирующих веществ с активными центрами катализатора. Эти реакции катализируются металлами и полупроводниками. Активность переходных металлов (Fe, Co, Ni, Ru, Rh, W, Re, Os, Ir, Pt и др.) в окислительно-восстановительных реакциях объясняется незавершенностью их d‑оболочек. Неспаренный электрон незавершенной d-орбитали действует как «свободная валентность», в значительной мере подобно свободному радикалу. Если адсорбированная молекула имеет незанятые орбитали, то возникает π-связь с такими активными центрами. Молекула, являющаяся донором пары электронов, может образовать координационную связь с незаполненной орбиталью катализатора.
В случае полупроводников свободные валентности (свободные электроны и электронные дырки) появляются вследствие неполной координированности атомов кристаллической решетки. Обычно это связано с различными дефектами кристалла полупроводника. Например, узел кристалла, в котором отсутствует катион, ведет себя как отрицательный заряд, отталкивая электроны в ближайших узлах. В результате эти электроны могут быть вытеснены из валентной зоны в зону проводимости.
Появление электронов в зоне проводимости в полупроводниках может быть вызвано также присутствием в кристалле различных примесей. На поверхности кристалла такие электроны будут играть роль свободной валентности.
Таким образом, каталитическая активность прямо связывается с числом свободных валентностей на поверхности катализатора.
Кислотный катализ
Катализ кислотами широко применяется в нефтеперерабатывающей промышленности. Каталитическое действие кислот обусловлено образованием при их взаимодействии с углеводородами катионов, называемых карбоний-ионами или карбкатионами. Обычно карбкатионы образуются при передаче протона от кислоты к молекуле ненасыщенного углеводорода:
НХ + CH3CH=CHR ® CH3CH2CH+R + X-
Кислоты Льюиса являются энергичными акцепторами электронной пары и также могут инициировать реакцию с участием карбоний-иона:
ALX3 + RH ® R+ + HAIX-3
Образование карбкатионов в присутствии кислых галогенидов облегчается, если в системе имеется некоторое количество галогеналкилов:
AlX3 + RX ® R+ + A1X4-
Галогеналкилы в этом случае играют роль промоторов.
Карбкатионы — чрезвычайно реакционноспособные соединения. Константы скорости ионных реакций на несколько порядков выше аналогичных радикальных реакций. Об относительной устойчивости карбкатионов можно судить по теплоте их образования, в кДж/моль:
| СН3+ | СН3СН2СН2СН2+ | ||
| СН3СН2+ | СН3СH2 С+НСН3+ | ||
| CH3CH2CH2+ | (СН3)3С+ | ||
| CH3 C+HCH3+ | (CH3)3CCH2+ | 8.2 |
Как следует из этих данных, стабильность карбкатионов возрастает в последовательности: первичный < вторичный < третичный.
Основными реакциями карбкатионов, как и радикалов, являются мономолекулярный распад по β-правилу и бимолекулярные реакции замещения и присоединения. Существенное отличие карбкатионов от радикалов — их способность к изомеризации.
 15.3. Реакции карбкатионов
15.3. Реакции карбкатионов
Изомеризация. Изомеризация карбкатионов может происходить в результате переноса как гидрид-иона, так и метиланиона:
+ + +
CH2 CH CH2 CH2 CH3« CH3 CH CH CH2 CH3 « CH3 CH2 CH CH2 CH3
 •• ••
•• ••

 Н Н
Н Н
+ + +
 CH3CHCH2:CH3 « CH3CHCH2 « CH3CCH3+ 76 кДж/моль
CH3CHCH2:CH3 « CH3CHCH2 « CH3CCH3+ 76 кДж/моль
 | |
| |
 CH3 CH3
CH3 CH3
Подобное перемещение происходит быстро в направлении от первичного иона карбония к вторичному и далее к наиболее устойчивому — третичному.
Распад по β-правилу. Расщепление карбкатионов обычно происходит по наиболее слабой связи β-С—С. Реакция эндотермична:
+
CH2 CH2 CH2 CH2 CH2 CH2 CH2 CH3 ®
+
® CH2=CH2 + CH2 CH2 CH2 CH2 CH2 CH3 — 92 кДж/моль
Склонность к распаду снижается при переходе от первичного иона к вторичному и от вторичного к третичному. Если для распада первичного октилкатиона требуется 92 кДж/моль, то для вторичного октилкатиона надо затратить 176 кДж/моль.
Склонность к распаду возрастает при отщеплении вторичного иона и — еще в большей степени — третичного:
+
CH3 CH2 CH CH2 C(CH3)2 CH2 CH3 ®
+
®CH3CH2CH=CH2 + C(CH3)2CH2CH3- 21 кДж/моль
Сопоставление энергетики распада и изомеризации карбкатионов показывает, что изомеризация должна предшествовать в большинстве случаев распаду. Преимущественное образование третичных карбкатионов и их устойчивость должны приводить к накоплению изоструктур при распаде неразветвленных алкильных карбкатионов с большим числом углеродных атомов.
Присоединение карбкатионов к алкенам и аренам. Эта реакция обратна реакции распада карбкатионов:
+ CH3 +
|
(CH3)3C + CH2=CCH3 ® (CH3)3CCH2C(CH3)2
+
(CH3)3C + C6H6 ® 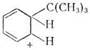
Поэтому характер изменения теплового эффекта противоположен реакции распада.
Потеря протона смежным углеродным атомом и передача протона молекуле алкена. Например:
+
СН3СН2СНСН3 ® СН3СН=СНСН3 + Н+
+
СН2СН(СН3)СН3 + СН3СН=СНСН3 ®
+
® СН2=С(СН3)СН3+СН3СНСН2СН3 + 42 кДж/моль
Наиболее энергетически выгодна такая реакция, когда протон отщепляется от первичного карбкатиона, а в результате образуется третичный карбкатион.
Отрыв гидрид-иона от молекулы углеводорода. Например:
+
СН3СНСН2СН3 + СН3СН(СН3)СН3 ®
+
® СН3СН2СН2СН3 + СН3С(СН3)СН3 + 67 кДж/моль
Активность карбкатиона в реакции отрыва гидрид-иона от молекулы углеводорода также снижается в ряду:
R+перв > R+втор > R+трет
Карбкатионные реакции всегда протекают или в жидкой фазе, или на поверхности твердого катализатора. Сольватация в растворе и адсорбция при реакции на твердой поверхности значительно изменяют тепловые эффекты реакции ионов. В результате соотношения между различными реакциями ионов в реальных процессах могут существенно отличаться от расчетных.
Каталитический крекинг
Реакции углеводородов при каталитическом крекинге протекают по цепному карбкатионному механизму. Наряду с крекингом углеводороды в условиях процесса вступают в реакции алкилирования, изомеризации, полимеризации, гидрирования и деалкилирования.
Превращения алканов
Часть молекул алканов подвергается вначале термическому крекингу. Образующиеся олефины присоединяют протоны, находящиеся на катализаторе, и превращаются в карбкатионы:
+
RCH=CH2 + Н+А- ® RCHCH3 + A-
Образовавшийся ион карбония отрывает гидрид-ион от молекулы алкана:
+
RCCH3 + СН3СН2СН2СН2СН2СН2СН3 ®
+
® RCH2CH3 + СН3СН2СН2СН2СН2СН2СН2
Далее реакция развивается по цепному пути. Карбкатион может разложиться (по β-правилу):
+ +
СН3СН2СН2СН2СН2СН2СН2 ® СН3СН2СН2СН2СН2 + (CH2=CH2)
Однако высокая скорость изомеризации ионов приводит к тому, что этилена — продукта распада первичного карбкатиона — образуется очень мало.
Изомеризация происходит как путем перемещения гидрид-иона, так и при перемещении метиланиона. В первом случае образующиеся вторичные ионы сохраняют прямую углеводородную цепь. Тепло, выделяющееся при изомеризации, затрачивается на расщепление. Превращение протекает по схеме:
+

 СН3СН2СН2СН2СН2СН2СН2
СН3СН2СН2СН2СН2СН2СН2
+ +
СН3СН2СН2СН2СН2СНСН3 ® СН3СН2СН2СН2 + (СН2=СНСН3)
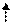 + +
+ +
СН3СН2СН2СН2СНСН2СН3 ® СН3СН2СН2 + (СН2=СНСН2СН3)
Изомеризация карбкатиона с перемещением метиланиона дает продукты с разветвлением углеводородного скелета:
+ +
СН3СН2СН2СН2СНСН2СН3 « СН3СН2СН2СН2СН(СН3)СН2
+ +
 СН3СН2СН2 + (СН2=С(СН3)2) СН3СН2СН2СН2С(СН3)СН3
СН3СН2СН2 + (СН2=С(СН3)2) СН3СН2СН2СН2С(СН3)СН3
Чередование экзотермической изомеризации и эндотермического β-распада продолжается до образования карбкатионов, содержащих 3–5 атомов углерода. Тепловой эффект изомеризации этих ионов уже не компенсирует затраты тепла на расщепление. Поэтому карбкатионы С3—С5 после изомеризации отрывают гидрид-ион от молекулы исходного углеводорода:
+ +
СН3СН2СН2 ® СН3СНСН3
+
CH3CHCH3 + CH3CH2CH2CH2CH2CH2CH3 ®
+
® (СН3СН2СН3) + CH3CH2CH2CH2CH2CH2CH2
Затем весь цикл реакций повторяется. Обрыв цепи происходит при встрече карбкатиона с анионом катализатора:
+
СН3СН2СН2 + А- ® СН3СН2СН2А
Первая стадия — отрыв гидрид-иона от алкана — протекает быстрее в том случае, если гидрид-ион отрывается от третичного углеродного атома. Поэтому скорость крекинга разветвленных алканов выше, чем нормальных. Вместе с тем и распад ионов наиболее легко идет с отщеплением третичных карбкатионов, в результате чего в продуктах распада нормальных алканов с числом атомов углерода четыре и более преобладают изоструктуры.
Скорость каталитического крекинга алканов на один-два порядка выше скорости их термического крекинга.
Превращение циклоалканов
Скорость каталитического крекинга циклоалканов близка к скорости крекинга алканов с равным числом атомов углерода и увеличивается при наличии третичного атома углерода.
Стадия инициирования — возникновения карбкатионов — для насыщенных углеводородов циклического и ациклического строения протекает одинаково. За счет высокой температуры возникает небольшое количество алкенов, которые, присоединяя протон от катализатора, превращаются в карбкатионы.
Образовавшиеся ионы карбония отрывают гидрид-ион от молекулы циклоалкана. Отщепление гидрид-иона от третичного углеродного атома протекает легче, чем от вторичного, поэтому глубина крекинга возрастает с увеличением числа заместителей в кольце:
Строение молекулы
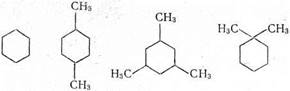
Глубина крекинга, % 47 75,6 78,6 51,8
Неоструктуры (1,1-диметилциклогексан) отщепляют гидрид-ион от вторичного углерода, поэтому степень превращения близка к незамещенному циклогексану.
Распад циклогексильного иона может происходить двумя путями: 1) с разрывом кольца; 2) без разрыва кольца.
1) 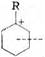 | R  + + | |
| ® CH2=СCH2CH2CH2CH2 | ||
При разрыве С—С-связи образуется алкенильный ион, который легко изомеризуется в ион аллильного типа:
+ +
H2C=C(R)CH2CH2CH2CH2 ® H2C=CRCHCH2CH2CH3
Последний может расщепиться по β-правилу, оторвать гидрид-ион от исходного углеводорода или передать протон молекуле алкена или катализатору.
При крекинге по этому пути из циклогексана образуются алкены и диены.
2) Циклогексильный ион может передать протон алкену или катализатору и превратиться в циклоалкен:
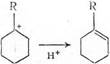
Этот путь энергетически выгоднее, чем распад по С—С-связи (1).
Циклоалкены крекируются быстрее, чем циклоалканы, со значительным выходом аренов.
Выход аренов достигает 25% и более от продуктов превращения циклогексанов, а газы крекинга циклоалканов содержат повышенное по сравнению с газами крекинга алканов количество водорода.
Наблюдается также изомеризация циклогексанов в циклопентаны и обратно:
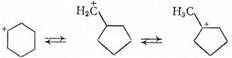
Циклопентаны в условиях каталитического крекинга более устойчивы, чем циклогексаны. При наличии длинных боковых цепей в молекуле циклоалкана возможны изомеризация боковой цепи и деалкилирование молекулы.
Бициклические циклоалканы ароматизируются в большей степени, чем моноциклические.
Превращение алкенов
Скорость каталитического крекинга алкенов на два-три порядка выше скорости крекинга соответствующих алканов, что объясняется легкостью образования из алкенов карбкатионов:
+
Н2С=СНСН2СН3 + Н+ ® Н3ССНСН2СН3 + 724 кДж/моль
При присоединении протона к молекуле алкена образуется такой же ион, как и при отщеплении гидрид-иона от алкана, что определяет общность их реакций при каталитическом крекинге.
Кроме образования низших алканов и алкенов каталитический крекинг алкенов приводит к образованию циклоалканов и аренов. Механизм этих процессов может быть представлен схемой:
+ +
CH2=CHCH2 + CH2=C(CH3)CH3 ® CH2=CHCH2CH2C(CH3)CH3 ® 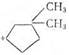
Далее может произойти изомеризация в шестичленный цикл и превращение в арен.
Превращение аренов
Незамещенные арены в условиях каталитического крекинга устойчивы. Метилзамещенные арены реагируют со скоростью, близкой к алканам. Алкилпроизводные аренов, содержащие два и более атомов углерода в цепи, крекируются примерно с такой же скоростью, что и алкены. Основной реакцией алкилпроизводных аренов является деалкилирование. Это объясняется большим сродством ароматического кольца к протону, чем к алкильному иону:
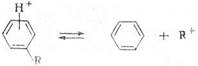
Скорость реакции возрастает с увеличением длины цепи алкильного заместителя.
В случае метилзамещенных аренов отщепление карбкатиона энергетически затруднено, поэтому в основном протекают реакции диспропорционирования (а) и изомеризации по положению заместителей (б):
а) 2С6Н5СН3 « С6Н6 + C6H4(CH3)2
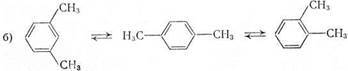
Полициклические арены прочно сорбируются на катализаторе и подвергаются постепенной деструкции и перераспределению водорода с образованием кокса.
