Варіанти хроматографії за фазовим станом
§ Газова хроматографія (використовується наприклад для визначення якості харчового спирту)
§ Рідинна хроматографія (використовується для аналізу та виділення органічних сполук)
§ Хроматографія над критичними рідинами/газами (рідкісний вид, проміжний між першими двома. Найчастіше використовують як елюєнт вуглкислий газ під високим тиском та підвищених температурах)
Варіанти хроматографії за способом проведення
§ Препаративна - використовується для розділення речовин залежно від їхньої швидкості руху. В більшості випадків застосовують рідинну хроматографію.
§ Аналітична - має на меті лиш оцінити склад суміші. Маси зразків - мікрограми.
Найросповсюдженіші техніки
Тонкошарова хроматографія
Аналітична Тонкошарова хроматографія широко застосовується в органічній хімії для поточного аналізу сумішей (сумарний час експерименту 2-10хв). Нерухомою фазою служить силікагель нанесений на пластинку (найчастіше товсту алюмінієву фольгу). Як рухому фазу застосовують органічні розчинник. Набір гептан<етилацетат<метанолдозволяє елюювати більшість сполук. Часто також застосовують етер та хлороформ.
Тонкошарова хроматографія можлива й в препарати
Колонкова хроматографія
Один з основних спосіб очистки органічних речовин в сучасній синтетичній практиці. Силікагелем набивають скляну колонку завтовшки 5-50мм. Зверху наносять малу кількість концентрованого р-ну суміші, а потім починають елюювання аналізуючи час від часу розчин, що виходить через малий отвір знизу колонки.
HPLC (ВЕРХ)
HPLC (ВЕРХ, ВисокоЕфективна Рідинна Хроматографія) використовує прикладання зовнішнього тиску для прискорення проходження рідини через колонку. Це дозволяє застосовувати наповнювач з часточками меншого розміру й прискорює розділення. Препаративні хроматографи для розділення органічних речовин працюють при тиску порядку 100-600 бар з металевими колонками діаметром 0.5-4.6 мм (найчастіше використовують диаметром 2.1 та 4.0 - 4.6 мм) та довжиною 15-300 мм. Як нерухому фазу застосовують ліпофільно-модифікований силікагель (оберненофазна хроматографія), тоді як рухомою фазою слугують суміші води та органічного розчинника (найчастіше ацетонітрилу). ВЕРХ застосовують як для аналізу, так і для розділення сумішей. Типовий час експерименту 2-30хв.
Афінна хроматографія
Для розділення біологічних зразків часто застосовують модифікування нерухомої фази речовиною, що вибірково зв'язується з сполукою, що цікавить експериментатора. Так, наприклад очистка антитіл може проводитись на колонках з сефарози модифікованої протеїном.
2.розрахунки pH i pOH
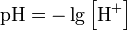
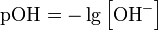
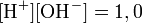 *
* 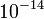
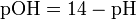
Наприклад
1. Дано [H+] = С(HNO3)=0.01моль/дм3
С(HNO3)=0.01моль/дм3 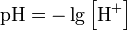 = 2
= 2
Знайти:
pH-?
- Дано с(OH)=C(KOH)= 0.05 моль/дм3
c(KOH)=0.05 моль/дм3 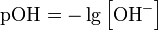 =1.3
=1.3
pH-? pOH-? pH= 14-pOH=14-1.3=12.7
Білєт 17
Йонообмінна хроматографія
Хроматографія – метод розділення та аналізу суміші речовин. Вперше хроматографування здійснювалось за допомогою паперу, на якому краплина суміші, розділившись на складові частини (компоненти), утворила пляму (хроматограму) з різнозабарвленими зонами на різній відстані від її центра, звідки й пішла назва методу.
Йонообмінна хроматографія
Йонообмінна хроматографія ґрунтується на оборотному обміні йонами між взірцем (рідинна рухома фаза), який підлягає аналізу, і сорбентом, який називають йонообмінником (тверда нерухома фаза), або йонітом. Йоніти, які вступають у обмін з катіонами (позитивно зарядженими йонами), називають катіонітами, а при взаємодії з аніонами (негативно зарядженими йонами) – аніонітами.
Здатність до йонного обміну проявляють деякі мінерали і низка синтетичних матеріалів. Найпоширеніше застосування отримали синтетичні органічні йонообмінники на основі штучних смол.
Зазвичай синтетичний йоніт є полімером, який містить різні функціональні групи. Ці групи визначають характерні властивості йонообмінних смол. Полімер складається із каркасу – тривимірної просторової структури, утвореної матрицею з нерозчинної хімічно інертної органічної речовини R. Матриця з’єднана з йоногенними групами, здатними до обміну з йонами розчину. Наприклад, у йоніті на основі полістиролу 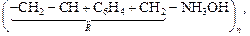 де органічна частина – CH2 – CH + C6H4 + CH2є матрицею, а
де органічна частина – CH2 – CH + C6H4 + CH2є матрицею, а 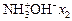 – йоногенною групою.
– йоногенною групою.
Одна частина йоногенної групи (у цьому прикладі 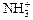 ) жорстко закріплена у каркасі. Ці йони називають фіксованими: вони створюють заряд каркаса (у наведеному прикладі
) жорстко закріплена у каркасі. Ці йони називають фіксованими: вони створюють заряд каркаса (у наведеному прикладі 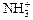 – фіксований йон, каркас позитивно заряджений, отже,
– фіксований йон, каркас позитивно заряджений, отже, 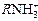 – аніоніт). Заряд каркаса компенсується іншою частиною йоногенної групи – протийонами (у наведеному прикладі – OH -), які є рухомими. Протийони беруть участь у йонному обміні, переходячи у розчин, а на їхнє місце приходить еквівалентна кількість йонів із розчину, які мають заряд того ж знака, що і протийони; отже, йоніт залишається електронейтральним.
– аніоніт). Заряд каркаса компенсується іншою частиною йоногенної групи – протийонами (у наведеному прикладі – OH -), які є рухомими. Протийони беруть участь у йонному обміні, переходячи у розчин, а на їхнє місце приходить еквівалентна кількість йонів із розчину, які мають заряд того ж знака, що і протийони; отже, йоніт залишається електронейтральним.
Схема йонного обміну для наведеного прикладу має вигляд:
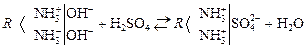 .
.
Аналогічним є рівняння йонного обміну для катіоніта:
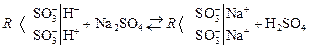 .
.
Зазначимо, що існують біполярні йонообмінні смоли-амфоліти, які мають властивості як аніонітів, так і катіонітів.
Якість йонообмінників характеризують їхньою сорбційною (обмінною) ємністю і хімічною стійкістю.
Обмінна ємність – це кількість йонів із розчину, яку поглинає одиниця маси або об’єму йоніта (число грам-екв. протийонів на 1 г сухої смоли).
Хімічну стійкість визначають відношенням йоніта до робочого середовища при хроматографічному аналізі. Її мірою є ступінь зменшення маси і ємності йоніта.
Для йонообмінників визначені адсорбційні ряди (ряди селективності) йонів, у яких кожен наступний член ряду має дещо більшу здатність утримуватись йонітом (зазвичай цій здатності відповідає більший заряд і менший радіус йона).
Йонообмінний цикл налічує дві стадії.
Перша стадія – сорбція – поглинання йонів нерухомою фазою (йонітом). Друга – десорбція – добуття йонів із йонообмінника за допомогою рухомої фази – елюенту.
Практично це виглядає так:
Ä підбирають відповідний йоніт, здійснюють його обробку і розташовують у колонці;
Ä пропускають через колонку розчин, який підлягає аналізу;
Ä пропускають через колонку елюент;
Ä здійснюють аналіз елюенту.
Підбираючи склад і кислотність елюенту, можна вилучати із колонки одні йони, залишаючи адсорбованими інші (селективне елюювання).
Основні напрями застосування йонообмінної хроматографії: розділення близьких за властивостями елементів; вилучення заважаючих йонів; концентрування цінних мікроелементів із природних і промислових вод; кількісне визначення сумарного вмісту солей у розчинах; демінералізація води; отримання солей, кислот і основ.
