Поведение загрязняющих веществ в природных водах
Судьба загрязняющих веществ в природных водах складывается по – разному. Тяжелые металлы, попав в водоем, распределяются по различным формам, после чего постепенно выносятся с течением, захватываются донными отложениями или поглощаются водными организмами (в первую очередь, связываясь с SH –группами), с которыми и оседают на дно, причем разные формы тяжелых металлов поглощаются в разной степени.
Нефтепродукты практически не смешиваются с водой и растекаются по ее поверхности тонкой пленкой, которая уносится течениями и со временем адсорбируется на взвешенных частицах и оседает на дно. Растворенные нефтепродукты также адсорбируются на взвешенных частицах, либо окисляются растворенным в воде кислородом, причем разветвленные углеводороды окисляются быстрее неразветвленных. Также нефтепродукты могут усваиваться водными микроорганизмами, однако здесь ситуация обратная: разветвленные усваиваются медленнее.
Поверхностно – активные вещества адсорбируются на взвешенных частицах и оседают на дно. Также они могут разлагаться некоторыми микроорганизмами. Некоторые ПАВ образуют нерастворимые соли с кальцием и магнием, однако поскольку такие ПАВ плохо мылятся в жесткой воде, их стараются заменять веществами, не образующими нерастворимых солей. Поведение ПАВ, не образующих нерастворимых солей, в основном описывается кинетическими моделями с использованием эффективной линейной скорости потока из толщи воды на дно.
Удобрения, попав в водоем, обычно поглощаются живыми организмами, резко увеличивая биомассу, но, в конечном итоге, все равно оседают на дно (хотя частично могут быть извлечены из донных отложений обратно).
Большинство органических веществ, в том числе ядохимикаты, либо гидролизуются, либо окисляются растворенным кислородом, либо (несколько реже) связываются с гумусовыми кислотами или ионами Fe3+. И окислению и гидролизу могут способствовать некоторые микроорганизмы. Окислению подвергаются вещества, содержащие серу в низких степенях окисления, двойные связи, ароматические кольца с донорными заместителями. Также окисляются атомы углерода, связанные с кислородом, и атомы углерода у поляризованных связей:
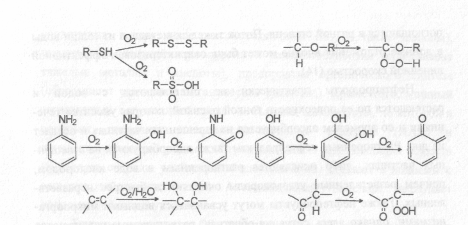
Галогенсодержащие соединения, а также ароматические соединения с мета –ориентирующими заместителями (например, NO2 –группой) и галогенами окисляются гораздо медленнее, чем незамещенные аналоги. Кислородсодержащие группы в молекуле или o, n – ориентирующие заместители (кроме галогенов) в ароматическом кольце, наоборот, ускоряют окисление. В общем, относительная устойчивость соединений к окислению в воде примерно такая же, как и в атмосфере.
Гидролизу подвергаются, в первую очередь, соединения, содержащие полярные связи углерод – галоген, существенно медленнее — сложноэфирные связи, еще медленнее — связи C –N.
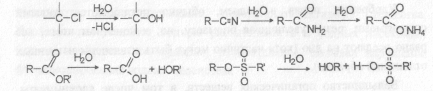
Увеличение полярности связи приводит к ускорению гидролиза. Кратные связи, а также связи с ароматическим ядром практически не гидролизуются. Также плохо гидролизуются соединения, в которых у одного атома углерода находится несколько атомов галогенов. Если в результате гидролиза образуются кислоты, то повышение рН, как правило, способствует этому процессу, если образуются основания – усилению гидролиза способствует уменьшение рН. В сильнокислых средах ускоряется процесс гидролиза связей С – О, но замедляется гидролиз связей углерод – галоген.
Как окисление, так и гидролиз органических соединений описываются кинетическими моделями и могут быть охарактеризованы периодом полупревращения этих соединений. Гидролиз, катализируемый кислотами и основаниями описывается более сложными моделями, поскольку его скорость очень сильно зависит от рН (Рис.).
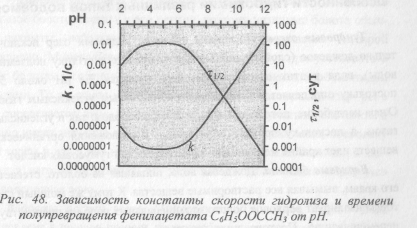
Такую зависимость обычно выражают уравнением
k = kn + kа *10-pH + kb £„ *1014 –рН,
где k — общая константа скорости гидролиза, kn — константа скорости гидролиза в нейтральной среде, ka – константа скорости гидролиза, катализируемого кислотой, kb, — константа скорости гидролиза, катализируемого основанием.
Продукты окисления и гидролиза, как правило, менее опасны для организмов, чем исходные вещества. Кроме того, они могут далее окислиться до Н2О и СО2 или усвоиться микроорганизмами. В гидросфере второй путь более вероятен. Химически устойчивые органические вещества в итоге оказываются в донных отложениях за счет адсорбции на взвесях или поглощения микроорганизмами.
Во всех водоемах эффективные линейные скорости потока растворенных веществ на дно обычно намного меньше 10 см/сут, поэтому этот путь очищения водоемов достаточно медленный, но зато весьма надежный. Органические вещества, попавшие в донные отложения, обычно разрушаются обитающими в них микроорганизмами, тяжелые металлы превращаются в нерастворимые сульфиды.
