Опыт 3: Углекислый газ, угольная кислота и ее соли
а) Универсальным индикатором измерили рН дистиллированной воды. рН = 6.Это обусловлено тем, что в ней растворен углекислый газ.
б) Из аппарата Киппа очищенным и осушенным углекислым газом (очистить можно пропусканием углекислого газа через дистиллированную воду, а осушить – пропусканием через концентрированную серную кислоту) наполнили три большие банки (чтобы убедиться, что банки полностью наполнены углекислым газом, надо горящую лучинку внести в банку: если пламя гаснет в верхней части банки, значит она полная). На слабое пламя горелки вылили содержимое одной из них. Пламя горелки затухает. Во вторую банку щипцами внесли горящий магний. Он продолжал гореть, и при этом сильно коптил. В третью внесли ложечку с горящим красным фосфором. Горение прекратилось. Таким образом, углекислый газ поддерживает горение магния, а фосфора – нет.
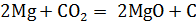
 2
2 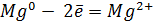
 1
1 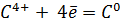
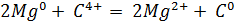
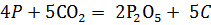

 4
4 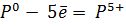
5 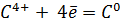
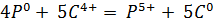
в) В 0,1 н раствор щелочи добавили каплю раствора фенолфталеина и пропустили ток чистого углекислого газа из аппарата Киппа до исчезновения окраски. Затем раствор прокипятили. Окраска снова появилась.
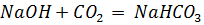
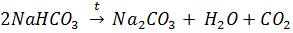
г) Теоретически оценили рН раствора питьевой соды. Соответствующие константы диссоциации для угольной кислоты:
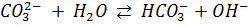 ; Ka1=4,5*10-7
; Ka1=4,5*10-7
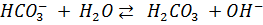 ; Ka2=5*10-11
; Ka2=5*10-11
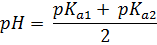
Для децинормального (0,1M)раствора питьевой соды в воде получаем:
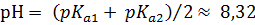
д) Растворы хлоридов магния и алюминия обработали раствором соды. При взаимодействии с раствором хлорида магния выпадает белый осадок, при взаимодействии с хлоридом алюминия – студенистый белый осадок.
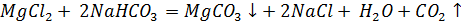
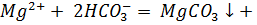
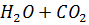
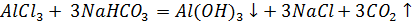
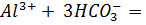
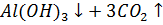
е) Для очистки карбоната от гидрокарбоната, сульфита и сульфата в водном растворе необходимо:
1. Прокипятить раствор. При этом: 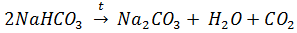
2. Произвести окисление перекисью водорода:
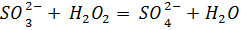
3. Титрованием установить точную концентрацию сульфата в растворе, рассчитать количество 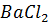 , необходимое для его связывания, и прибавить к раствору, тщательно перемешивая.
, необходимое для его связывания, и прибавить к раствору, тщательно перемешивая.
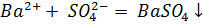
4. Отфильтровать полученный раствор.
Вывод. Предложили рациональную схему очистки карбоната от примесей гидрокарбоната, сульфита и сульфата.
