Межатомное взаимодействие
Между двумя атомами действует сила притяжения. Природе является кулоновской, следовательно, она убывает обратно пропорционально квадрату расстояния между атомами. Помимо силы притяжения, между атомами действует и сила взаимного отталкивания, которая обратно пропорциональна расстоянию в степени n, где n больше 2. Складывая силы притяжения и отталкивания, получаем результирующую силу взаимодействия двух атомов (рис 1 а). При расстоянии между атомами, равном rО силы притяжения и отталкивания взаимно компенсируют друг друга, результирующая сила взаимодействия равна нулю, и это расстояние является наиболее устойчивым.
Оценим энергию потенциального взаимодействия двух атомов как работу, с обратным знаком, по перемещению иона из бесконечности в данную точку.
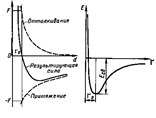 Рис.1. Зависимость сил взаимодействия между атомами (а) и энергии потенциального взаимодействия (б) от расстояния между атомами. Рис.1. Зависимость сил взаимодействия между атомами (а) и энергии потенциального взаимодействия (б) от расстояния между атомами. |
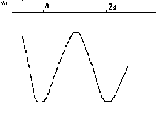 Рис. 2. Зависимость энергии потенциального взаимодействия (Wp) от расстояния между атомами (x) для случая взаимодействия множества атомов. Рис. 2. Зависимость энергии потенциального взаимодействия (Wp) от расстояния между атомами (x) для случая взаимодействия множества атомов. |
Из рисунка 1 б видно, что при минимальной энергии потенциального взаимодействия расстояние между соседними ионами равно rО. Увеличение энергии системы двух атомов (например, за счет роста тепловой энергии) ведет к появлению возможности взаимного смещения атомов относительно друг друга, причем с ростом энергии системы амплитуда колебаний возрастает. Другой интересной особенностью влияния температуры на свойства материалов является термическое расширение. Как видно из рисунка 1 б, кривая потенциального взаимодействия (или потенциальная кривая) асимметрична, поэтому при росте температуры среднее расстояние между атомами увеличивается, и линейные размеры тел увеличиваются. Изменение линейных размеров тела при нагреве описывается коэффициентом теплового расширения: aТ = (1/L)(dL/dT). Как видно из рис. 2б), коэффициент теплового расширения снижается при увеличении глубины потенциальной ямы.
В том случае, когда взаимодействует множество атомов, смещение любого из них приводит к росту энергии системы, Поэтому потенциальную кривую можно представить в виде периодической функции (рис. 2).
Для переброса атома из одного равновесного положения в другое требуется повышение энергии. Поэтому в том случае, когда энергия системы минимальна или незначительно отличается от минимальной, атомы не могут перемещаться из одного положения в другое, и мы имеем дело с твердым телом. При значительном повышении энергии системы атомы активно колеблются, обмениваются энергией - и в результате могут переходить из одного положения в другое. В этом случае мы имеем дело с жидким телом. Дальнейший рост энергии системы приводит к выходу атомов из потенциальной ямы, они перестают взаимодействовать друг с другом, могут занимать различные положения – и мы имеем дело с газом.
Увеличение глубины потенциальной ямы ведет к росту температуры плавления и температуры испарения вещества. Вместе с тем, увеличение глубины потенциальной ямы ведет к уменьшению коэффициента теплового расширения: aТ = (1/L)(dL/dT). Таким образом, вещества с большей температурой плавления, как правило, имеют меньший коэффициент термического расширения.
При воздействии на тело силовых полей (электрического, механического, магнитного) частицы тела смещаются из равновесных положений. При этом могут реализовываться три случая.
1. Чем "круче" стенки потенциальной ямы, тем труднее осуществляется упругий бесгистерезисный процесс, в частности, растет модуль упругости материала.
2. упругогистерезисными (типичный пример - "неупругость" пружин) и характеризуются замкнутыми кривыми, называемыми циклами гистерезиса.
3. то при снятии внешнего воздействия частицы в исходные положения не возвращаются, появляется остаточный эффект
Подводя итог сказанному выше, следует отметить, что увеличение глубины потенциальной ямы ведет к росту напряжения течения при пластической деформации, увеличению модуля упругости, повышению температур плавления и испарения, к снижению коэффициента теплового расширения. Таким образом, зная одни свойства материала, можно прогнозировать другие свойства.
Типы химических связей.
 Рис. 3. Схема образования ковалентной связи Рис. 3. Схема образования ковалентной связи |
Ковалентная связь. Ковалентная связь образуется между атомами одного или нескольких химических элементов с близкими ионизационными потенциалами. В чистом виде ковалентная связь реализуется при взаимодействии элементов с наполовину заполненными электронными оболочками. Из квантовой химии следует, что система из положительно заряженного ядра и отрицательно заряженных электронных оболочек имеет минимальную энергию в том случае, когда электронные оболочки заполнены полностью. Поэтому атомы с наполовину заполненными электронными оболочками обмениваются электронами. При этом образуются пары электронов с противоположно направленными спиновыми магнитными моментами, причем эти пары принадлежат обоим соседним атомам.
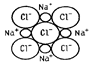 Рис. 3. Схема образования ионной связи Рис. 3. Схема образования ионной связи
Рис. 5. Схема образования металлической связи. |
Появление между положительно заряженными ионами пары отрицательно заряженных электронов приводит к тому, что оба иона притягиваются к обобществленным электронам и, тем самым, притягиваются друг к другу. Каждый атом взаимодействует с ограниченным числом соседей, причем число соседей равно числу валентных электронов атома. Следовательно, ковалентная связь насыщенна. Кроме того, атом взаимодействует только с теми соседями, с которыми он обменялся электронами, то есть ковалентная связь направленна.
В результате, с ростом порядкового номера элемента падает температура плавления, растет коэффициент теплового расширения, уменьшается модуль упругости.
Ионная связь. Ионная связь образуется при взаимодействии атомов с малым количеством валентных электронов и атомов с большим количеством электронов на валентных оболочках. При этом наружные электроны атомов с низкими потенциалами ионизации переходят на валентные оболочки атомов с высокими ионизационными потенциалами. В результате образуются положительно и отрицательно заряженные ионы, взаимно притягивающиеся электростатическими силами. Ионная связь ненасыщенна, поскольку каждый из отрицательно заряженных ионов притягивает к себе положительно заряженные, а каждый из положительно заряженных ионов притягивает к себе все отрицательно заряженные. Однако ионная связь направлена, поскольку ион притягивает к себе разноименно заряженные ионы и отталкивает одноименно заряженные.
Уменьшение размера иона и увеличение его заряда ведет к росту энергии связи, а следовательно, к росту температуру плавления материала, уменьшению коэффициента теплового расширения и к увеличению модуля упругости.
Металлическая связь образуется между атомами одного или нескольких химических элементов, у которых валентные электронные оболочки застроены меньше чем на половину. Поскольку энергия иона минимальна при полностью заполненной внешней оболочке, атомы отдают внешние валентные электроны и превращаются в положительно заряженные ионы, между которыми находятся свободные электроны (электронный газ).
Каждый из положительно заряженных ионов притягивается к свободным электронам, и, тем самым, ионы притягиваются друг к другу. Металлическая связь ненаправленна и ненасыщенна, и число ближайших соседей у иона определяется в основном геометрическим и энергетическими факторами. Следовательно, кристаллические решетки металлов упакованы плотно. Под действием электрического поля не связанные с ионами электроны перемещаются, то есть металлы обладают высокой электропроводностью.
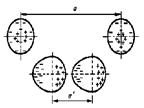 Рис. 6 Схема образования диполей при сближении нейтральных атомов Рис. 6 Схема образования диполей при сближении нейтральных атомов |
Поляризационная связь, или связь Ван-дер-Ваальса. Образуется при сближении молекул или атомов инертных газов.
У одиночного атома электронная оболочка симметрична. При сближении двух атомов их электронные оболочки электрически взаимодействуют и деформируются (см. рис. 6). В итоге атомы превращаются в диполи, которые взаимно притягиваются. Чем больше порядковый номер атома, тем больше у него электронных оболочек, а следовательно, связь валентных электронов с ядром ослабевает, и деформировать ее становится легче. Следовательно, возрастает дипольный момент атома и увеличивается энергия связи между атомами.
При сближении электрически нейтральных молекул. Причем чем выше молекулярный вес, тем больший дипольный момент молекул и выше энергия связи

