Способы выражения концентрации раствора.
31. Сколько граммов Na2SO3 потребуется для приготовления 5 л 8% -ного (по массе) раствора ( 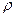 =1.075 г/мл)?
=1.075 г/мл)?
Ответ 430 г.
32. Из 400 г 50%-ного (по массе) раствора Н2SO4 удалили (выпариванием) 100 г воды. Чему равна массовая доля Н2SO4 в оставшемся растворе?
Ответ 66,7%
33. Найти массовую долю азотной кислоты в растворе , в 1 л которого содержится 224 г НNО3 раствора ( 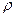 =1.12 г/мл)?
=1.12 г/мл)?
Ответ 20%
34. В какой массе воды нужно растворить 2S2 CuSO4 5H2O, чтобы получить 8%-ный (по массе) раствор CuSO4.
Ответ 174,7 г.
35. Сколько граммов Na2SO4 10 H2O надо растворить в 800 г. воды, чтобы получить 10% ный раствор (по массе) раствор Na2SO4?
Ответ 235,3 г.
36. Чему равно осмотическое давление 0,5 М раствора глюкозы С6Н12О6 при 25 °С.
Ответ 1,24 МПа.
37. Сколько молей неэлектролита должен содержать 1 л раствора, чтобы его осмотическое давление при 25 °С было равно 2,47 кПа?
Ответ 0,001 моля.
38. На сколько градусов повысится температура кипения воды, если в 100 г воды растворить 9 г глюкозы С6Н12О6?
Ответ 0,26 °С.
39. При какой температуре будет кипеть 50% -ный (по массе) раствор сахарозы С12Н22О11?
Ответ 101°С.
40. В радиатор автомобиля налили 9 л воды и прибавили 2 л спирта ( 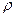 =0,8 г/мл). При какой наинизшей температуре можно после этого оставить автомобиль на открытом воздухе, не опасаясь , что вода в радиаторе замерзнет?
=0,8 г/мл). При какой наинизшей температуре можно после этого оставить автомобиль на открытом воздухе, не опасаясь , что вода в радиаторе замерзнет?
Ответ - 8°С.
41. Константа диссоциации масляной кислоты С3Н7С00Н 1,5 10–5. Вычислить степень ее диссоциации в 0,05 М растворе.
Ответ 0,055.
42. Найти степень диссоциации хлорноватистой кислоты НОСl в 0,2 н растворе.
Ответ 5 10-4.
43. Степень диссоциации муравьиной кислоты НСООН в 0,2 н растворе равна 0,03. Определить константу диссоциации кислоты и значение рК.
Ответ К = 1,8 10-4
РК = 3,75.
44. При какой концентрации раствора степень диссоциации азотистой кислоты НNО2 будет равна 0,2?
Ответ 0,01 моль/л.
45. Сколько воды нужно прибавить к 300 мл 0,2 М раствора уксусной кислоты, чтобы степень диссоциации кислоты удвоилась?
Ответ 900 мл.
46. Определить рН раствора в 1л которого содержится 0,1 г N4ОН. Диссоциацию щелочи считать полной.
Ответ 11,4.
47. Во сколько раз концентрация ионов водорода в крови (рН=7,36) больше, чем спинномозговой жидкости (рН = 7,53)?
Ответ 1,5 раз.
48. Определить [Н+] и [ОН-] в растворе, рН которого равен 6,2.
Ответ [Н+] = 6,3 10-7 моль/л
[ОН-] = 1,6 10-8 моль/л.
49. Вычислить рН следующих растворов слабых электролитов:
· 0.02 М NН4ОН;
· 0,1 М НСN;
· 0,05 М НСООН;
· 0,01 М СН3СООН.
Ответ
· 10,78;
· 5,05;
· 2,52;
· 2,38.
50. Вычислить рН растворов, в которых концентрация ионов ОН- (в моль/л) равна:
· 4,6 10-4;
· 5 10-6;
· 9,3 10-9.
Ответ
· 10,66;
· 8,70;
· 5,97.
Окислительно-восстановительными называются реакции, сопровождающиеся изменением степени окисления атомов, входящих в состав реагирующих веществ. Под степенью окисления (n) понимают тот условный заряд атома, который вычисляется исходя из предложения, что молекула состоит только из ионов. Иными словами: степень окисления – это тот условный заряд, который приобрел бы атом элемента, если предположить, что он принял или отдал то или иное число электронов.
Окисление-восстановление – это единый взаимосвязанный процесс. Окисление приводит к повышению степени окисления восстановителя, а восстановление – к ее понижению у окислителя (т.е. окислитель принимает электроны, а восстановитель отдает).
Атом того или иного элемента в своей высшей степени окисления не может ее повысить (отдать электроны) и проявляет только окислительные свойства, а в своей низшей степени окисления не может ее понизить (принять электроны) и проявляет только восстановительные свойства. Атом же элемента, имеющий промежуточную степень окисления, может проявлять как окислительные, так и восстановительные свойства.
Например, степень окисленности Mn в различных соединениях может изменяться от +7 до +2. Поэтому перманганат калия (К Mn О4), степень окисленности которого составляет +7 проявляет только окислительные свойства. Соединение NH3 (N3-) проявляет только восстановительные свойства.
При окислительно-восстановительных реакциях валентность атомов может не меняться. Например, в окислительно-восстановительной реакции Н20+Cl20 = 2Н+Cl- валентность атомов водорода и хлора до и после реакции равна 1. Изменилась их степень окисления. Валентность определяет число связей, образованных данным атомом, и поэтому знака не имеет. Степень же окисления имеет знак плюс или минус.
Вещество, в состав которого входит окисляющийся элемент, называется восстановителем; вещество содержащее восстанавливающийся элемент, называется окислителем. Так, в реакции NiO + CO = Ni + CO2 никель снижает степень окисленности от +2 до 0 и служит окислителем, а углерод повышает степень окисленности от +2 до +4 и является восстановителем.
Пример № 1
Составьте уравнения окислительно - восстановительно реакции, идущей по схеме:
+7 +3 +2 +5
 KMnO4 + H3PO4 + H2SO4 MnSO4 + H3PO4 + K2SO4 +H2O
KMnO4 + H3PO4 + H2SO4 MnSO4 + H3PO4 + K2SO4 +H2O
Решение
Если в условии задачи даны как исходные вещества, так и продукты их взаимодействия, то написание уравнения реакции сводится, как правило, к нахождению и расстановке коэффициентов. Коэффициенты определяют методом электронного баланса с помощью электронных уравнений. Вычисляют, как изменяют свою степень окисления восстановитель и окислитель, и отражают это в электронных уравнениях:
 восстановитель 5 Р3+ - 2е- = Р5+ окисление
восстановитель 5 Р3+ - 2е- = Р5+ окисление
окислитель 2 Mn7+ + 5e- = Mn2+ восстановление
Общее число электронов, отданных числу электронов, которое присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов десять. Разделив это число на 5, получаем коэффициент 2 для окислителя и продукта его восстановления, а при делении 10 на 2 получаем коэффициент 5 для восстановителя и продукта его окисления. Коэффициенты перед веществами, атомы которых не меняют свою степень окисления находят подбором. Уравнение реакции будет иметь вид:
 2KMnO4 + 5H3PO4 + 3H2SO4 2MnSO4 + 5H3PO4 + K2SO4 +3H2O
2KMnO4 + 5H3PO4 + 3H2SO4 2MnSO4 + 5H3PO4 + K2SO4 +3H2O
51. Какие из следующих реакций относятся к окислительно-восстановительным?
· Н2 + Вr2 = 2НВr
· NH4Cl = NH3 +HCl
· NH4NO3 = N2O + 2H2O
· 2K2CrO4 = K2Cr2O7 + K2SO4 +H2O
· H3BO3 + 4HF = HBF4 + 3H2O
· Fe + S = FeS
52. Для следующих реакций указать, какие вещества и за счет каких именно элементов играют роль окислителей и какие- восстановителей:
· SO2 + Br2 + 2H2O = 2HBr + H2SO4
· Mg + H2SO4 = MgSO4 + H2
· Cu + 2H2SO4 = CuSO4 + SO2 + 2H2O
· 3J2 + 6KOH = KJO3 +5KJ + 3H2O
53. Указать, какие из реакций относятся к окислительно-восстановительным?
· Сr(SO4)3 + 6RbOH = 2 Cr(OH)3 + 3Rb2SO4
· 2Rb+2H2O = 2RbOH + H2
· CuJ2 = 2CuJ + J2
· NH4Cl + NaOH = NaCl + NH3 + H2O
· 2K4 [Fe(CN6)] + Br2 = 2K3 [Fe(CN6)] + 2KBr
54. До каких продуктов может быть окислена вода:
· до О2 и Н+
· до ОН- и Н2
· до 2ОН-
55. В каких из указанных превращений кислород выполняет функции восстановителя:
·  Ag2O Ag + O2
Ag2O Ag + O2
·  F2 + H20 HF + O2
F2 + H20 HF + O2
·  NH3 + O2 N2 + H2O
NH3 + O2 N2 + H2O
· 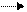 AgNO3 + KOH + H2 O2 Ag + KNO3 + O2
AgNO3 + KOH + H2 O2 Ag + KNO3 + O2
56. Составьте электронные уравнения, Расставьте коэффициенты в уравнениях реакций. Для каждой реакции укажите, какое вещество является окислителем, какое - восстановителем, какое вещество окисляется. Какое восстанавливается.
· 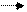 P + HJO3 + H2O H3PO4 + HJ
P + HJO3 + H2O H3PO4 + HJ
· 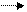 H2S + Cl2 + H2O H2SO4 +HCl
H2S + Cl2 + H2O H2SO4 +HCl
57. Составьте электронные уравнения, Расставьте коэффициенты в уравнениях реакций. Для каждой реакции укажите, какое вещество является окислителем, какое - восстановителем, какое вещество окисляется. Какое восстанавливается.
·  P + HNO3 + H2O H3PO4 + NO
P + HNO3 + H2O H3PO4 + NO
· 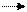 KMnO4 + Na2SO3 +KOH K2MnO4 + Na2SO4 + H2O
KMnO4 + Na2SO3 +KOH K2MnO4 + Na2SO4 + H2O
58. Составьте электронные уравнения, Расставьте коэффициенты в уравнениях реакций. Для каждой реакции укажите, какое вещество является окислителем, какое - восстановителем, какое вещество окисляется. Какое восстанавливается.
·  H2S + Cl2 + H2O H3 SO4 + HCl
H2S + Cl2 + H2O H3 SO4 + HCl
·  K2Cr2O7 + H2SO4 +H2S S+ K2SO4 + Cr2(SO4 )3+ H2O
K2Cr2O7 + H2SO4 +H2S S+ K2SO4 + Cr2(SO4 )3+ H2O
59. Составьте электронные уравнения, Расставьте коэффициенты в уравнениях реакций. Для каждой реакции укажите, какое вещество является окислителем, какое - восстановителем, какое вещество окисляется. Какое восстанавливается.
·  KClO3 + Na2SO3 Na2 SO4 + KCl
KClO3 + Na2SO3 Na2 SO4 + KCl
·  KMnO4 + HBr Br2+ KBr + MnBr2 + H2O
KMnO4 + HBr Br2+ KBr + MnBr2 + H2O
60. Составьте электронные уравнения, Расставьте коэффициенты в уравнениях реакций. Для каждой реакции укажите, какое вещество является окислителем, какое - восстановителем, какое вещество окисляется. Какое восстанавливается.
·  P + HClO3 + H2O H3PO4 + HCl
P + HClO3 + H2O H3PO4 + HCl
·  H3AsO3 + KMnO4 + H2SO4 H3AsO4 + MnSO4 + K2SO4 + H2O
H3AsO3 + KMnO4 + H2SO4 H3AsO4 + MnSO4 + K2SO4 + H2O
