Электрическая проводимость растворов
Электрическая проводимость растворов определяется скоростью движения ионов, а также их числом в единице объема и, следовательно, зависит от концентрации, природы растворенного вещества и растворителя, температуры и давления.
Удельная электрическая проводимость сильных электролитов с ростом концентрации линейно возрастает, проходит через максимум, и затем уменьшается (рис. 5.6). Наибольшим значением κ в водных растворах обладают минеральные кислоты, затем гидроксиды и соли. Аналогичный характер имеет зависимость κ— С и в случае неводных растворителей, но абсолютные значения κ меньше (рис. 5.7).
Концентрация электролита, отвечающая максимуму электрической проводимости, специфична для данного электролита и растворителя. С повышением температуры удельная электрическая проводимость возрастает (рис.. 5.8). Однако при достаточно высо ких температурах удельная электрическая проводимость с ростом температуры, как это установлено еще Аррениусом, уменьшается.
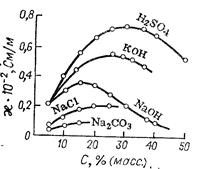

Рис. 5.6. Зависимость удельной электрической проводимости c водных растворов некоторых соединений от концентрации С.
Рис. 5.7. Зависимость удельной электрической проводимости κ неводных растворов некоторых солей от концентрации С.
LiС1 растворен в диметилацетамиде, LiBr и А1С1з —в пропиленкарбонате;
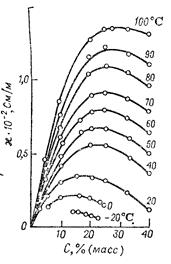
Pиc. 5.8. Зависимость удельной электрической проводимости гидроксида натрия от концентрации при разных температурах.
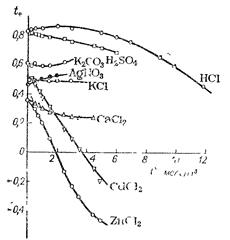
Рис. 5.9. Зависимость чисел переноса катионов некоторых электролитов от концентрации.
Эквивалентная электрическая проводимость максимальна в бесконечно разбавленных растворах, с ростом концентрации — уменьшается, а с повышением температуры — возрастает.
Кольрауш показал, что в ряде случаев в разбавленных растворах эквивалентная электрическая проводимость линейно уменьшается в соответствии с уравнением:
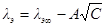
По Гхошу иногда получается лучшее совпадение с экспериментом, если изменение эквивалентной электрической проводимости представить уравнением
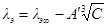
Эквивалентную электрическую проводимость при бесконечном разведении (нулевой концентрации) можно найти экстраполяцией
на С = 0 прямолинейных участков λ– 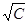 кривых, отвечающих уравнениям Кольрауша или Гхоша.
кривых, отвечающих уравнениям Кольрауша или Гхоша.
Большие значения проводимости сильных кислот и оснований определяются высокой скоростью движения иона гидроксония и гидроксид-иона. Ниже приведены подвижности некоторых ионов в водных растворах при бесконечном разведении и 25 °С:
Ион l∞∙104, Ион l∞∙104, Ион l∞∙104,
См∙м2/экв См∙м2/экв См∙м2/экв
Ag+ 61,9 Na+ 50,1 ⅓ Fe(CN)63– 99,1
⅓ Al3+ 63,0 ½ Ni2+ 54,0 ¼ Fe(CN)64– 111,0
½ Ca2+ 59,5 ½ Pb2+ 70,0 I– 76,8
½ Cd2+ 54,0 ½ Zn2+ 54,0 MnO4– 61,3
½ Co2+ 49,0 (CH3)4N+ 44,9 NO3– 71,4
⅓ Cr3+ 67,0 (C2H5)4N+ 32,6 OH– 197,6
½ Cu2+ 55,0 (C3H7)4N+ 23,4 ½ SO42– 80,0
½ Fe2+ 53,5 (C4H9)4N+ 19,4 ½ WO42– 69,4
⅓ Fe3+ 68,0 (C5H11)4N+ 17,4 HCOO– 54,6
Н3О+ 349,8 Br– 78,1 CH3COO– 40,9
½ Hg2+ 63,6 Cl– 76,3 CH2ClCOO– 39,8
K+ 73,5 ½ CrO42– 83,0 C6H5COO– 32,3
Li+ 386 F– 55,4
NH4+ 73,5
Поскольку числа переноса ионов определяются скоростями движения всех сортов ионов в электролите, то, естественно, что в кислотах и щелочах числа переноса ионов гидроксония и гидр-оксида при бесконечном разведении будут существенно больше половины, в то время как для растворов солей отклонение чисел переноса от величины 0,5 не очень значительно. С увеличением концентрации числа переноса катиона и аниона в водных растворах некоторых электролитов остаются постоянными, а в других — более или менее резко изменяются (рис. 5.9). Отрицательные значения чисел переноса ионов Cd2+ и Zn2+ в растворах CdCl2 и ZnCl2 не имеют физического смысла и показывают лишь, что примененный метод измерения регистрирует суммарный эффект, связанный с переносом катиона в составе отрицательно заряженного комплексного аниона.
