Строение дыхательной цепи (ДЦ), комплексы, ингибиторы. Механизм работы. Пункты сопряжения, величина ОВП компонентов ДЦ. Коэффициент Р/О, его значение
Дыхательная цепь.
Поэтапное «контролируемое сгорание» достигается путём промежуточного включения дыхательных ферментов, обладающих различным редокс-потенциалом. Редокс-потенциал (окислительно-восстановительный потенциал) определяет направление переноса протонов и электронов ферментами дыхательной цепи (рис.1).
Редокс-потенциал выражается значением электродвижущей силы (в вольтах), которая возникает в растворе между окислителем и восстановителем, присутствующих в концентрации 1,0 моль/л при 25˚ С (при рН=7,0 оба находятся в равновесии с электродом, который может обратимо принимать электроны от восстановителя). При рН=7,0 редокс-потенциал системы Н2 /2Н++2ē равен – 0,42 v. Знак – означает, что данная редокс-пара легко отдаёт электроны, т.е. играет роль восстановителя, знак + указывает на способность редокс-пары принимать электроны, т.е. играть роль окислителя. Например, редокс-потенциал пары НАДН∙Н+/ НАД+ равен – 0,32 v, что говорит о высокой её способности отдавать электроны, а окислительно-восстановительная пара ½О2 /Н2О имеет наибольшую положительную величину +0,81 v, т.е. кислород обладает наивысшей способностью принимать электроны.
В процессе окисления АцКоА в ЦТК, восстановленные формы НАДН2 и ФАДН2 поступают в ДЦ, где энергия электронов и протонов трансформируется в энергию макроэргических связей АТФ.
ДЦ - совокупность дегидрогеназ, которые транспортируют электороны и протоны с субстрата на кислород.
Принципы функционирования ДЦ основаны на 1-ом и 2-ом законах термодинамики.
Движущей силой ДЦ является разность ОВП. Суммарная разность всей ДЦ составляет 1,1 В. Пункты фосфорилирования должны иметь перепад ОВП = 0,25 - 0,3 В.
1. Пара НАД-Н имеет ОВП = 0,32 В.
2. Пара Q-b - / - /- - 0 В.
3. O2 - имеет +0,82 В.
ДЦ локализуется во внутренней мембране митохондрий и имеет 2 пути введения электронов и протонов или 2 входа; ДЦ образует 4 комплекса.
1 вход: НАД-зависимый (поступают электроны и протоны со всех НАД-зависимых реакций).
2 вход: ФАД-зависимый
НАД ---->ФП
Q --->b--->c1--->c--->aa3---->1/2O2
Янтарная кислота ---->ФП
Дыхательная цепь – форма реализации биологического окисления.
Тканевое дыхание – это последовательность окислительно-восстанови-тельных реакций, протекающих во внутренней митохондриальной мембране с участием ферментов дыхательной цепи. Дыхательная цепь имеет чёткую структурную организацию, её компоненты формируют дыхательные комплексы, порядок расположения которых зависит от величины их редокс-потенциала (рис.5.1). Количество дыхательных цепей в отдельно взятой митохондрии из клеток разных тканей неодинаково: в печени – 5000, в сердце – около 20 000, следовательно, миокардиоциты отличаются более интенсивным дыханием, чем гепатоциты.
|
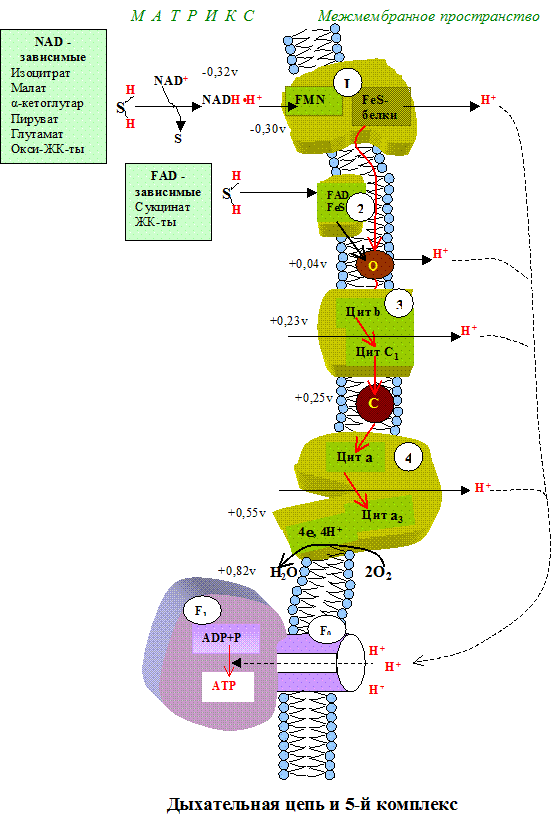
Прежде чем остановиться на характеристике каждого из компонентов дыхательной цепи, познакомимся с субстратами тканевого дыхания.
Субстраты тканевого дыхания подразделяются на 2 группы:
1. НАД-зависимые – субстраты цикла Кребса изоцитрат, α-кетоглутарат и малат. Это также пируват, гидроксибутират и β–гидрокси-ацил~КоА, глутамат и некоторые другие аминокислоты. Водород от НАД-зависимых субстратов c помощью НАД-зависимых дегидрогеназ передаётся на I-й комплекс дыхательной цепи.
2.ФАД-зависимые – сукцинат, глицерол-3-фосфат, ацил~КоА и некоторые другие. Водород от ФАД-зависимых субстратов передаётся на II-й комплекс дыхательной цепи.
При дегидрировании субстратов НАД-зависимыми дегидрогеназами образуется восстановленная форма НАД (НАДH∙H+).
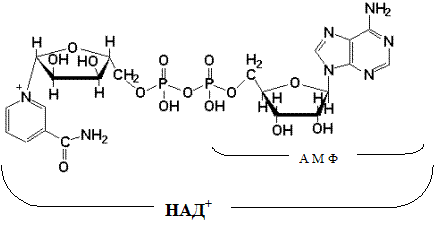
Указана окисленная форма кофермента НАД+. Этот кофермент является динуклеотидом (никотинамид-аденин-динуклеотид): в состав одного нуклеотида входит витамин РР (никотинамид), другой представляет собой АМФ. Способность кофермента играть роль промежуточного переносчика водородов связана с наличием в его структуре витамина РР. В электронно-протонной форме процесс обратимого гидрирования-дегидрирования может быть представлен уравнением (R- остальная часть кофермента):

НАДH∙H+ может образовываться не только в митохондриях, но и в цитозоле клетки при протекании определённых процессов метаболизма. Однако цитоплазматический кофермент не может проникать в митохондрии. Водород восстановленного кофермента должен быть сначала перенесен на субстраты, которые могут проникать в митохондрии. Такими «Н2-переносящими субстратами» являются:
Оксалацетат → малат
Ацетоацетат → β-гидроксибутират
Дигидроксиацетон фосфат → глицерол-3-фосфат
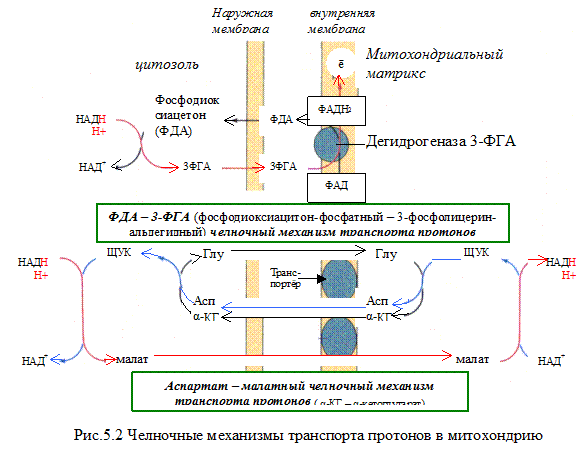
НАДH∙H+ затем окисляется 1-м комплексом дыхательной цепи. Рассмотрим работу этого комплекса.
I комплекс цепи тканевого дыхания – НАДH∙H+-убихинон-оксидодуктаза.
Первый комплекс является самым большим в дыхательной цепи (представлен 23-30 субъединицами). Он катализирует перенос водорода от НАДH∙H+ на убихинон (рис. 5.1 и рис. 5.3). В его состав входят кофермент ФМН (флавинмононуклеотид) и железосерные белки, содержащие негеминовое железо. Функция этих белков заключается в разделении потока протонов и электронов: электроны переносятся от ФМН∙Н2 к внутренней поверхности внутренней мембраны митохндрий (обращенной к матриксу), а протоны – к внешней поверхности внутренней мембраны и затем высвобождаются в митохондриальный метрикс.
При транспорте протонов и электронов редокс-потенциал первого комплекса снижается на 0,38 v, что вполне достаточно для синтеза АТФ. Однако в самом комплексе АТФ не образуется, а высвобождающаяся в результате работы комплекса энергия аккумулируется (см. ниже образование электро-химического потенциала) и частично рассеивается в виде тепла.
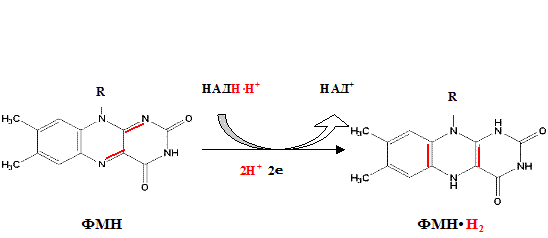
По своему строению ФМН – мононуклеотид, в котором азотистое основание представлено изоаллоксазиновым ядром рибофлавина, а пентозой является рибитол (иными словами, ФМН – это фосфорилированная форма витамина В2).
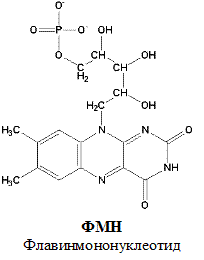
Функция ФМН заключается в акцепции 2 атомов водорода от НАДH∙H+ и передачи их железосерным белкам. Водород (2 электрона и 2 протона) присоединяется к атомам азота изоаллоксазинового кольца, при этом происходит внутримолекулярная перегруппировка двойных связей с образованием промежуточного семихинона – соединения свободнорадикальной природы (на схеме представлено суммарное уравнение реакции, где R – остальная часть молекулы)
II комплекс цепи тканевого дыхания –сукцинат-убихинон-оксидоредуктаза.
Этот комплекс имеет меньшую молекулярную массу и также содержит железосерные белки. Сукцинат-убихинон-оксидоредуктаза катализирует перенос водорода от сукцината на убихинон. В состав комплекса входит кофермент ФАД (флавин-аденин-динуклеотид) и фермент сукцинатдегидрогеназа, который является одновременно ферментом цикла Кребса. Ацил~SКоА, 3-фосфо-глицерат и диоксиацетон фосфат также являются ФАД-зависимыми субстратами тканевого дыхания и с помощью этого кофермента контактируют со вторым комплексом.

Рис. 5.3 Первый комплекс дыхательной цепи
Энергия включения водорода субстратов во II комплекс цепи тканевого дыхания рассеивается в основном в виде тепла, так как на этом участке цепи редокс-потенциал снижается незначительно и этой энергии для синтеза АТФ мало.
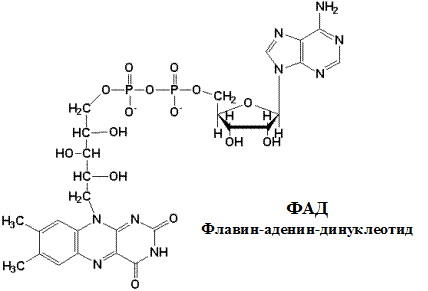
Процесс восстановления ФАД протекает аналогично таковому ФМН.
Кофермент Q или убихинон - гидрофобное соединение, является компонентом клеточных мембран, содержится в большой концентрации, относится к группе витаминов. относится к группе витаминов.
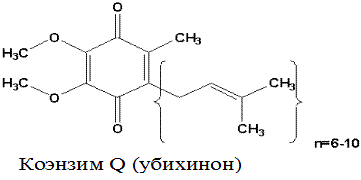
Убихинон (коэнзим Q). Убихинон – небольшая липофильная молекула, по химическому строению представляющая собой бензохинон с длинной боковой цепью (число изопреноидных единиц колеблется от 6 у бактерий до 10 у млекопитающих).
В дыхательной цепи коэнзим Q является своеобразным депо (пулом) водорода, который он получает от различных флавопротеинов. Липофильный характер молекулы убихинона обуславливает его способность свободно перемещаться в липидной фазе митохондриальной мембраны, перехватывая протоны и электроны не только от I и II комплексов дыхательной цепи, но и захватывая из митохондриального матрикса протоны. При этом убихинон восстанавливается с образованием промежуточного свободнорадикального продукта – семихинона .
Восстановленная форма убихинона – убихинол – передаёт протоны и электроны на III комплекс дыхательной цепи.
 |
Цитохромоксидаза имеет высокую степень сродства к кислороду и может работать при его низких концентрациях.
аа3 - состоит из 6 субъединиц каждая из которых содержит гем и атом меди. 2 субъединицы составляют цитохром а, а остальные 4 относятся к цитохрому а3.
Между НАД и ФП, b-c, a-a3 имеет место max перепад ОВП. Эти пункты являются местом синтеза АТФ (местом фосфорилирования АДФ).
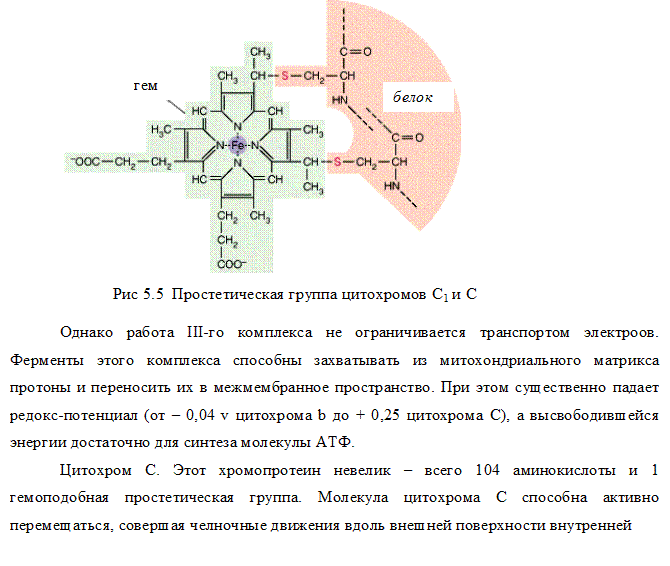
III комплекс цепи тканевого дыхания –убихинол-цитохром С-оксидоредуктаза. В состав III комплекса входят цитохромы b и с1, относящиеся к группе сложных белков хромопротеинов. Простетическая группа этих белков окрашена (chroma – краска) и близка по химическому строению к гему гемоглобина. Однако в противоположность гемоглобину и оксигемоглобину, в которых железо должно быть только в 2-х валентной форме, железо в цитохромах при работе дыхательной цепи переходит от двух- к трёхвалентному состоянию (и обратно).
Как видно из названия, III комплекс переносит электроны от убихинола на цитохром С. Вначале электроны поступают на окисленную форму цитохрома b (Fe3+), который при этом восстанавливается (Fe2+), затем восстановленный цитохром b передаёт электроны окисленной форме цитохрома с, который также восстанавливается и, в свою очередь, передаёт электроны цитохрому С.
|
IV комплекс дыхательной цепи – цитохром С-оксидаза. Комплекс назван оксидазой из-за способности непосредственно взаимодействовать с кислородом. У млекопитающих этот крупный (~ 200 kD) трансмембранный белок состоит из 6-13 субъединиц, из которых некоторые кодируются митохондриальной ДНК. В состав IV комплекса входят 2 хромопротена – цитохром а и цитохром а3. В отличие от других цитохромов, цитохромы а и а3каждый содержат не только атом железа, но и атом меди. Медь в составе этих цитохромов при транспорте электронов также попеременно переходит в окисленное (Cu2+) и восстановленное (Cu+) состояние.
Цитохром с-оксидаза катализирует одноэлектронное окисление 4-х восстановленных молекул цитохрома си при этом одновременно осуществляет полное (4-х электронное) восстановление молекулы кислорода:
 4 цитохрома с(Fe2+) + 4 H+ + O2 4 цитохрома с(Fe3+) + H2O
4 цитохрома с(Fe2+) + 4 H+ + O2 4 цитохрома с(Fe3+) + H2O
Протоны для образования молекул воды поступают из матрикса. Следует заметить, что эта реакция весьма сложна и протекает через промежуточные стадии образования свободных радикалов кислорода.
Окислительно-восстановительный потенциал IV комплекса является самым большим (+0,57 v), его энергии вполне достаточно для синтеза 3-х молекул АТФ, однако большая часть этой энергии используется на «перекачивание» протонов из матрикса митохондрий в межмембранное пространство. В связи с активным транспортом протонов цитохром с-оксидаза получила название «протонного насоса».
Таким образом, тканевое дыхание представляет собой процесс транспорта электронов и протонов от НАД- или ФАД-зависимых субстратов на кислород, а также протонов, поставляемых матриксом митохондрий. При транспорте падает редокс-потенциал, что сопровождается высвобождением заключённой в субстратах тканевого дыхания энергии. Полное восстановление молекулярного кислорода воздуха в дыхательной цепи сопровождается образованием воды.
