Акустические свойства льда
ВВЕДЕНИЕ
Материаловедение – прикладная наука, изучающая связи между составом, строением, свойствами материалов и композитов в различных условиях.
В дисциплине «Материаловедение» рассматривается шесть материалов: вода, лед, металлы и сплавы, бетон, древесина и почвогрунты.
Целью дисциплины является ознакомление студентов гидрологов с теми материалами и их свойствами, с которыми они столкнуться в своей профессиональной деятельности.
Задачи дисциплины заключаются в развитии у студентов навыков позволяющих осуществлять рациональный выбор материалов для конкретного применения. Например, от материалов, применяемых при гидротехническом строительстве, зависят технология построения конструкций, качество и стоимость сооружения. Поэтому свойства материалов нужно знать, уметь их определять, а также готовить материалы к работе и правильному их использованию.
В дисциплине информация о материалах вода и лед является дополнительной к содержимому учебника «Гидрофизика». В результате изучения этих материалов студенты должны получить представление о выявлении, взаимодействии, использовании их свойств, в том числе и «необычных», не освещенных в «Гидрофизике».
Материалы бетоны, металлы и сплавы, древесина и своеобразие их свойств рассмотрены применительно к задачам гидрологии. После изучения металлов и сплавов студенты должны знать особенности строения и зависимость свойств от строения, способы определения и улучшения характеристик металлов и сплавов, маркировку и методы защиты их. Раздел о бетонах знакомит студентов со свойствами бетонов, связью между ними и заполнителями, используемыми для изготовления бетонных смесей, и со специальным гидротехническим бетоном. Раздел, в котором рассматривается древесина, преследует цель дать студентам информацию об особенностях строения разных пород деревьев, о физических и механических свойствах их древесины, об изделиях из древесины и способах ее консервации. Знания, полученные о выше перечисленных материалах, необходимы при строительстве и эксплуатации гидротехнических и гидрометрических сооружений, мостовых переходов, трубопроводов и других водохозяйственных объектов.
Почвогрунты рассматриваются как материал в отличие от изложенного в курсе лекций по «Гидрогеологии», в котором они представлены как факторы, влияющие на динамику водных процессов в поверхностном слое Земли. Рассматриваются отдельно почва и грунты: составляющие, свойства, взаимодействие и влияние различных природных условий на них.
Материаловедение подразумевает также и исследование свойств материалов по данным, полученным на экспериментальных установках. В дисциплине применен метод моделирования механических воздействий для получения информации о свойствах материалов в программном пакете MatLab.
История материаловедения
Наука о материалах имеет глубокую историю развития. Условно можно выделить три основных этапа в ее истории, не равных по своей продолжительности.
Первый этап охватывает наиболее длительный период. Исходным моментов для становления науки о материалах явилось получение керамики путем сознательного изменения структуры глины при ее нагревании и обжиге. С течением времени человечество познало самородные, а затем и рудные металлы, крепость и жесткость которых были известны уже с 8-го тыс. до н. э. Холоднокованая самородная медь была вытеснена медью, выплавленной из руд, которые встречались в природе чаще и в больших количествах. В дальнейшем к меди стали добавлять другие металлы. Вскоре человечество вступило из бронзового века в железный, поскольку железные руды оказались доступнее медных. В 1-м тысячелетии до н. э. научились железо соединять с углеродом. Первыми и наиболее правдоподобными суждениями о сущности качества материалов и о слагающих частицах вещества были суждения древнегреческих философов Демокрита (около 460 или 470 до н. э.) и Эпикура (341–270 до н. э.). Их учения об атомизме возникли под влиянием наблюдений за состоянием и свойствами природных камней, керамики, бронзы и стали. Примерно к тому же времени относится и философия древнегреческого ученого Аристотеля, который установил 18 качеств у материалов: плавкость–неплавкость, вязкость–хрупкость, горючесть–негорючесть и т. п. К первому периоду относится и средневековье с характерной для него алхимией. К этому периоду относится и учение Декарта (1596–1650) о том, что природа представляет собой непрерывную совокупность материальных частиц, что движение материального мира вечно и сводится к перемещению мельчайших частиц атомов. Перемещение атомов или, как их тогда называли, корпускул, составляло основу корпускулярной теории строения вещества, что было значительным достижением в области познания составов, внутренних взаимодействий и свойств веществ. В первых книгах по материаловедению Бирингуччо (1480–1539) и Агриколы (1494–1555) суммировались эмпирические сведения о сущности операций, выполняемых в литейном и кузнечном производствах, о плавлении руд и характере металлургического производства. Большой вклад в развитие науки о материалах был внесен гениальными русскими учеными М. В. Ломоносовым и Д. И. Менделеевым. М. В. Ломоносов (1711–1765) заложил основы передовой русской философии и науки, особенно в области химии, физики, геологии. Он явился основоположником курса физической химии и химической атомистики, обосновывающей атомно-молекулярное строение вещества. Д. И. Менделеев (1834–1907) открыл важнейшую закономерность природы – периодический закон и создал таблицу, в соответствии с которым свойства элементов находятся в периодической зависимости от величины их атомной массы. Для первого этапа становления и развития материаловедения, который начался с глубокой древности и продолжался до начала второй половины XIX в., характерно сравнительно ограниченное количество разновидностей материалов и опытных данных по их качественным характеристикам. Однако были установлены некоторые общие зависимости свойств веществ, особенно механических, от их состава. Менее изученной оставалась зависимость свойств от структуры, хотя еще в 1665 г. английский ученый Роберт Гук выявил у металлов типичную кристаллическую структуру, т. е. за 200 лет до открытия микроструктуры стали под микроскопом английским ученым Генри Сорби.
Второй этап развития материаловедения условно начался со второй половины XIX в. и закончился в первой половине XX в. Он отличается сравнительно быстрым ростом производства новых материалов. Например, кроме применявшихся на первом этапе камня немолотого или грубо околотого, меди, бронзы, железа и стали, керамики, стекла, отдельных вяжущих, например гипса, извести, появились новые цементы, и начался массовый выпуск портландцемента, открытого Е. Челиевым в начале XIX в. Кроме того, быстро развивалось производство цементных бетонов различного назначения; сформировалась специальная наука о бетонах – бетоноведение. В конце XIX в. формируется технология изготовления железобетона. Этот высокопрочный материал был предложен французскими учеными Ламбо и Ковалье, садовником Монье (1850–1870). Уровень познания поднялся так, что в цементной, полимерной, стекольной и некоторых других отраслях разрыв во времени между окончанием научной разработки и внедрением ее в производство становился весьма малым, т. е. наука превращалась в непосредственную производительную силу.
Третий этапохватывает период со второй половины XX в. до настоящего времени. Этот этап материаловедения характеризовался не только развитием практики, но и теории, систематизацией теоретических знаний о материалах в их сложной совокупности и взаимосвязи. Были установлены общие закономерности в свойствах искусственных и природных материалов оптимальной структуры, общие научные принципы в технологиях различных материалов, общие методы оптимизации их структуры, обобщение критериев (качественные и количественные) прогрессивных технологий и др. Первые обобщения в науке о материалах выразились в разработке Д. С. Белянкина (1876-1953). Новым импульсом развития материаловедческой науки на третьем этапе стала физико-химическая механика - пограничная наука между физической химией и механикой, разработанная П. А. Ребиндером при участии большой группы ученых. В этой области науки показаны основы управления технологическими процессами получения различных материалов с заданными свойствами, высокой надежностью и долговечностью. С начала второй половины XX в. возникла и получила последующее развитие теория искусственных материалов И. А. Рыбьева, над которой работают и в настоящее время.
Основные понятия
Плотность тела, удельный объем, удельный вес, теплоемкость, теплопроводность – это основные свойства материалов.
Плотность тела (кг/м3) - физическая характеристика тела (вещества) численно равная массе единицы объема тела (отношение массы тела к его объему). Плотность вещества растет с увеличением давления и, как правило, убывает с ростом температуры. При переходе вещества из жидкого состояния в газообразное и из твердого в жидкое плотность вещества скачкообразно уменьшается (исключение представляют вода и чугун, плотность которых при плавлении увеличивается).
Удельный объем (м3/кг) - физическая величина, равная отношению объема, занимаемого веществом, к его массе; величина обратная плотности.
Удельный вес (Н/м3) - физическая величина, равная отношению веса тела к его объему.
Теплоемкость - отношение количества теплоты, сообщаемого телу при бесконечно малом изменении его состояния в каком-либо процессе, к соответствующему изменению температуры этого тела. Отношение теплоемкости к массе тела называется удельной (Дж/кг × К). Теплоемкость зависит от химического состава и состояния тела, а также от процесса сообщения телу теплоты.
Теплопроводность - один из видов теплообмена, при котором перенос энергии в форме теплоты в неравномерно нагретой среде имеет атомно-молекулярный характер. В газах перенос энергии при теплопроводности осуществляется хаотически движущимися молекулами, в металлах - в основном электронами проводимости, в диэлектриках - за счет связанных колебаний частиц, образующих кристаллическую решетку.
ВОДА
Человечество с древних времен пользуется разными методами измерения, прогнозирования стока и способами управления им.
Например, первые попытки регулировать сток были предприняты в Древнем Египте. В 1855 г. в 30 км к югу от Каира обнаружены на временном водотоке (вади) остатки плотины бутовой кладки, длиной 100 м по гребню, высотой 11 м, которую некоторые исследователи считают древнейшей в мире – она была построена около 5000 лет назад. Плотину прорвало в первый же год существования (не было водослива). Греческие историки Геродот и Диодор Сицилийский сообщают, что в Египте в период Среднего Царства (2160–1788 г. до н. э.), когда Нил разливался, воды его задерживали в искусственных озерах для регулирования стока в целях орошения. Одним из таких озер являлось искусственное Меридово озеро, называемое сейчас Биркет-Карун.
Примерно в ту же эпоху (около 2300 лет до н. э.), после сильнейшего в истории Китая наводнения китайский император Яо поручил строителю Ю «укротить» реки Хуанхэ, Хуайхэ и Янцзы, затоплявшие огромные пространства во время частых катастрофических паводков, и осушить заболоченные ими земли. Ю, изучив режим рек и рельеф затопляемых территорий, создал целую систему гидротехнических сооружений – дамб, плотин, осушительных каналов, помогавших рекам находить путь к морю. Мероприятия, осуществленные Ю, увенчались успехом. После смерти императора гидролог-гидротехник Ю по воле народа был возведен на императорский трон и получил титул «Великого» и «Укротителя рек». Позднее Ю стал божественным покровителем всех гидрологов и гидротехников. В начале прошлого столетия во всех приречных храмах Китая все еще возносили молитвы в честь великого императора-гидротехника. Это единственный в истории случай обожествления гидролога.
Помимо того, что с водой связаны многие блага человеческой жизни, самой жизнью человек также обязан воде.
В настоящее время известно, что жизнь на Земле зародилась именно в водной среде. Это произошло около 4 миллиардов лет тому назад. 400 миллионов лет назад жизнь вышла из моря. 65 миллионов лет назад появились первые млекопитающие. Но вода и сейчас продолжает составлять значительную часть в живых организмах, причем как в морских животных, так и в млекопитающих, обитающих на суше (включая человека). Например, у десятидневного человеческого эмбриона содержание воды достигает 95%, у новорожденного – приблизительно 72%, а у взрослого человека – в среднем 60%.
В 1953 г, американский физик С. Миллер синтезировал ряд аминокислот, пропуская электрический разряд через смесь газов (молекулярного водорода Н2, метана СН4, аммиака NН3 и паров воды), предположительно составлявших первичную атмосферу Земли. И таким образом экспериментально доказал возможность возникновения сложных органических соединений в условиях, близких к условиям, господствовавшим на Земле в период появления на ней жизни.
Попав в какой-то водоем, эти соединения были защищены от жесткой солнечной радиации слоем воды. Далее следовал процесс постепенного усложнения углеродистых соединений.
Еще осталось много неясного в гипотезах возникновения жизни, но в принципе вопрос о первичном абиогенном образовании водного раствора органических веществ на еще безжизненной Земле можно считать решенным.
Строение же человека таково, что его плотность оказывается близкой к плотности воды. У многих людей она чуть меньше, особенно когда желудок пустой, а вода соленая. В таких случаях человек способен свободно находиться на поверхности воды, не боясь утонуть. На Земле есть и такое море, в котором вообще невозможно утонуть. Это соленое озеро, называемое Мертвым морем. Оно настолько соленое, что в нем отсутствует всякая жизнь (за исключением некоторых видов бактерий). Если вода большинства морей и океанов содержит 2–3% соли, то в Мертвом море ее содержится более 27%. Из-за большого содержания соли плотность воды здесь оказывается больше плотности человеческого тела, и потому человек в Мертвом море может спокойно лежать на его поверхности и читать книгу. Если же в эту воду войдет лошадь, то, как пишет Марк Твен, она оказывается в столь неустойчивом состоянии, что «не может ни плавать, ни стоять в Мертвом море, – она тотчас же ложится на бок».
Помимо Мертвого моря, огромной соленостью обладают также воды залива Кара-Богаз-Гол и озера Эльтон в Волгоградской области.
Можно экспериментально в домашних условиях определить среднюю плотность своего тела. Для этого сначала надо измерить свою массу. Затем определить объем тела. При определении своего объема погрузитесь полностью в ванну с водой. Одновременно с этим ваш друг с помощью кусочка липкой ленты (скотча) должен отметить уровень поднявшейся воды в ванне. Затем, выйдя из ванны, возьмите литровую банку и добавьте в ванну столько воды, чтобы ее поверхность поднялась до отмеченного лентой уровня. Подсчитав, сколько банок воды пришлось вылить в ванну, вы найдете свой объем, а зная объем и массу, – плотность.
Определив свою плотность, можно сравнить ее с плотностью воды. Будете ли вы тонуть в морской воде? Плотность морской воды составляет обычно 1010–1050 кг/м3. Плотность воды в заливе Кара-Богаз-Гол равна 1180 кг/м3.
В заключение повествования о воде как источнике жизни хочется привести слова Леонардо да Винчи (1452–1519), сказанные в эпоху, когда человечество стояло у истоков изучения воды, но точно и емко вобравшие все то, в чем на опыте убедились последующие поколения: «Воде была дана волшебная власть стать соком жизни на Земле».
Количество воды на Земле
Мировой океан вмещает 1 млрд. 338 млн. км3 воды, общее же количество воды на Земле, по последним данным, 1386 млн. км3.
Из общего количества воды на Земле только 35 млн. км3, или 2,5%, приходится на долю пресных, все остальное (97,5%) – соленые воды Мирового океана, минерализованные подземные воды и воды соленых озер. Пресной называют воду, 1 л которой содержит не более 1 г растворенных веществ (солей), т. е. воду с соленостью не более 0,1%. Соленость океанической воды равна 3,5% или в 1 л ее содержится 35 г солей. Без предварительной обработки, уменьшающей их жесткость, все осолоненные воды не пригодны не только для питья, но даже пока для технических нужд.
Количество пресной воды в 35 млн. км3 – это более 8 млн. м3 на каждого жителя Земли. Но подавляющая часть пресной воды на Земле находится в таком состоянии, которое делает ее труднодоступной для человека. Почти 70% пресных вод заключено в ледниковых покровах «полярных стран» и в горных ледниках, 30% – в водоносных слоях под землей, а в руслах всех рек содержатся одновременно лишь 0,006% пресных вод, или немногим более 1/1 000 000 части общих запасов воды (табл. 1).
Таблица 1.
Распределение пресной воды на земном шаре по водным объектам
| Водный объект | Количество воды, тыс. км3 |
| Ледники, подземные льды, постоянный снежный покров (в пересчете на воду) | 24364,0 |
| Подземные воды | 10 530,0 |
| Влага в почве | 16,5 |
| Пресные озера | 91,0 |
| Болота | 11,5 |
| Вода в руслах рек | 2,1 |
| Вода в атмосфере | 12,9 |
| Биологические воды (в живых организмах) | 1,1 |
Любопытно, что древние греки, не имевшие представления о круговороте воды, отводили в своих мифах очень важную роль Океану, прародителю всех богов. Жена Океана Тетис родила ему три тысячи дочерей – океанид, морских нимф, и три тысячи сыновей – речных божеств. Таким образом, по мифологии Океан стал родоначальником всех морей, рек и других водоемов на Земле.
Свойства воды
Из сказок известно, что существует живая вода – это вода, дающая молодость, здоровье, жизнь и мертвая вода – погружающая человека в сон, подобный смерти.
Подобие живой и мертвой воды существует в природе: живая, животворная – это талая вода, образовавшаяся от растаявшего снега или льда; мертвая, не утоляющая жажду и губящая все живое, – это тяжелая вода.
Более ста лет после того, как Лавуазье, Пристли, Гемфри Дэви установили, что вода состоит из двух объемов водорода и одного объема кислорода, физикам и химикам не удавалось узнать ничего нового о воде. Но вот в 1932 г. американцы Г. Юри и Э. Осборн обнаружили, что даже в самой чистой воде, которую только можно получить в лабораторных условиях, содержится незначительное количество какого-то вещества, выражающегося, по-видимому, той же химической формулой Н2О, но обладающего молекулярным весом 20 вместо веса 18, присущего обычной воде. Юри назвал это вещество тяжелой водой. Больший вес тяжелой воды объясняется тем, что ее молекулы состоят из атомов водорода с удвоенным атомным весом по сравнению с атомами обычного водорода.
Двойной вес этих атомов в свою очередь обусловливается тем, что их ядра содержат, кроме единственного протона, составляющего ядро обычного водорода, еще один нейтрон. Тяжелый изотоп водорода получил название дейтерия (D или Н2), а обычный водород стали называть протием. Тяжелая вода, окись дейтерия, выражается формулой D2O.
Вскоре был открыт третий, сверхтяжелый изотоп водорода с одним протоном и двумя нейтронами в ядре, который был назван тритием (обозначается Т или Н3).[1] В соединении с кислородом тритий образует сверхтяжелую воду Т2О с молекулярным весом 22.
Кроме того, были найдены три изотопа кислорода с атомными весами 16 (обыкновенный кислород), 17 и 18. Все вновь открытые изотопы водорода и кислорода в общей сложности составляют лишь ничтожную часть воды, поэтому в природных водах содержится в среднем около 0,016% тяжелой воды, т. е. на один атом дейтерия приходится 6600 атомов протия. Таким образом, почти вся вода в природе является тем, чем ее давно считали, а именно – соединением самых обычных изотопов водорода (протия) и кислорода, т. е. H2O.
Тяжелая вода внешне похожа на обычную воду, но по многим физическим свойствам она отличается от нее. Точка кипения тяжелой воды 101,4°С, точка замерзания +3,8°С. Тяжелая вода на 11 % тяжелее обычной. Самую большую плотность тяжелая вода имеет при 11°С. Ее удельный вес при 25 °С равен 1,1. Она хуже (на 5–15%) растворяет различные соли. В тяжелой воде скорость протекания некоторых химических реакций иная, чем в обычной воде, например, разложение электрическим током на водород и кислород происходит в пять раз медленнее. Обычная вода испаряется легче, поэтому неиспарившийся остаток ее обогащается тяжелой водой.
И в физиологическом отношении тяжелая вода воздействует на живое вещество иначе: в отличие от Н2О, обладающей живительной силой, тяжелая вода совершенно инертна. Семена растений, если их поливать тяжелой водой, не прорастают; головастики, микробы, черви, рыбы в такой воде не могут существовать; если животных поить одной тяжелой водой, они погибают от жажды.
Тяжелая вода – это мертвая вода. Символично, что один из составляющих ее элементов, а именно дейтерий, используется как ядерное горючее для водородной бомбы. Кроме того, тяжелая вода применяется в реакторах атомных электростанций для замедления нейтронов, которое необходимо для поддержания цепной реакции деления урана.
Было высказано предположение, что тяжелая вода, вернее, тяжелый водород, должна постепенно накапливаться в нашем организме и действительно становиться своего рода тормозом для жизненных функций, замедляющим обмен веществ. А ведь жизнь – это обмен веществ.
Логический вывод из этих рассуждений – «Не пейте тяжелой, мертвой воды. Пейте живую воду, освобожденную от дейтерия!»
Но избавиться от него пока практически невозможно. Впрочем, вскоре было обнаружено, что «живая вода» – талая вода. Ее чудесные целебные свойства связывают не с отсутствием в ней дейтерия (его столько же, сколько и в любой другой воде), а с тем, что в течение некоторого времени после образования талая вода частично сохраняет еще структуру льда, более «рыхлую», чем структура жидкой воды, в которой молекулы «упакованы» плотнее.
Ледяные структуры, легко проникая в ткани человека и животных, оказывают омолаживающее и оздоравливающее действие на организм. В литературе имеются указания, что талая вода увеличивает прирост веса молодняка, яйценоскость кур, молочность коров. Прокипяченная талая вода теряет свои чудесные свойства.
Может быть, березовый сок, собираемый ранней весной, который считается в народной медицине тоже полезным для здоровья, оттого и полезен, что представляет собой талую воду, прошедшую через живые клетки и обогатившуюся витаминами.
Другой вид живой воды, так называемая серебряная вода, был известен в глубокой древности. Это вода, бывшая в течение некоторого времени в соприкосновении с серебром или содержащая электролитический раствор серебра.
Еще 2500 лет назад персидский царь Кир в походах в Индию и Малую Азию пользовался питьевой водой, хранившейся в серебряных сосудах, чтобы предохранить ее от порчи. В 1893 г. швейцарский ботаник К. Негели впервые сообщил в печати об открытом им свойстве серебра при контакте с водой убивать находящиеся в ней микроорганизмы.
В нашей стране и за рубежом были выполнены исследования бактерицидных и лечебных свойств серебряной воды, разработаны эффективные способы ее получения и применения, создана соответствующая аппаратура. Приборами для получения серебряной воды оборудовано более 40 крупных морских судов. Космонавт В. Быковский пользовался в полете серебряной водой.
Имеется еще один вид воды, отличающийся по физическим свойствам от обычной воды, – это омагниченная вода. Такую воду получают с помощью магнитов, вмонтированных в трубопровод, по которому течет вода. Вода, проходя через невидимые силовые линии магнитного поля, изменяет некоторые свои физико-химические свойства, скорость химических реакций в ней увеличивается, ускоряется кристаллизация растворенных веществ, увеличивается слипание твердых частиц примесей и выпадение их в осадок с образованием крупных хлопьев (коагуляция). Омагничивание успешно применяется на водопроводных станциях при большой мутности забираемой воды, оно позволяет также быстро осаждать загрязненные промышленные стоки. Наиболее эффективной областью применения воды магнитной обработки оказалась борьба с накипью паровых котлов: использование омагниченной воды в котлах практически прекращает оседание на их стенках накипеобразующих солей.
Причины изменений свойств воды под воздействием магнитного поля пока не вполне ясны.
Важным свойством жидкости (воды) как материала является вязкость. Вязкость – свойство жидкости, обусловливающее появление касательных напряжений между слоями движущейся жидкости при их относительном перемещении. Количественной мерой вязкости являются величины динамической m (Н×с/м2) и кинематической u (стокс (Ст), 1 Ст = 10–4 м2/с) вязкостей. Они связаны соотношением
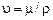 ,
,
где r – плотность жидкости.
Динамический коэффициент вязкости воды в сильной степени зависит от температуры и мало зависит от давления. При расчете динамического коэффициента вязкости применяют эмпирическую формулу Пуазейля:
m = 0,000183/(1 + 0,0337t + 0,000221t2),
где t – температура воды.
Динамический коэффициент вязкости соленой воды незначительно отличается от коэффициента вязкости пресной воды. Например, при t = 20°C и S = 25°/00 он равен 1,052 ×10–3 Па×с, а для пресной воды – 1,003 ×10–3 Па×с, т. е. больше примерно на 5%.
С ростом температуры жидкости значения m и u уменьшаются (для газов возрастают), а с увеличением давления – несколько увеличиваются. Значения m для воды, ртути, керосина и бензина приведены в табл. 2.
Таблица 2.
Значения динамической вязкости для некоторых жидкостей (m×103, Н×с/м2)
| Температура, °С | Дистиллированная вода | Ртуть | Керосин | Бензин |
| 1,7525 | 1,687 | 2,15 | 0,735 | |
| 1,2992 | – | 1,73 | 0,643 | |
| 1,0015 | 1,556 | 1,49 | 0,529 | |
| 0,7970 | – | – | – | |
| 0,6513 | 1,457 | 1,08 | 0,411 | |
| 0,5440 | – | – | – | |
| 0,4630 | 1,372 | 0,832 | 0,328 | |
| 0,4005 | – | – | – | |
| 0,3510 | 1,301 | 0,664 | 0,269 | |
| 0,3113 | – | – | – | |
| 0,2790 | 1,241 | 0,545 | 0,225 | |
| 0,1338 | 1,039 | 0,262 | 0,111 |
Отметим, что жидкость, не обладающая вязкостью, поверхностным натяжением и не изменяющая объема при изменении температуры и давления, называется идеальной. К идеальной жидкости близок по свойствам жидкий гелий.
Рассмотрим зависимость кинематической вязкости и удельной потери hп энергии (потери напора) при перемещении единицы массы вязкой жидкости. Вспомним уравнение Бернулли для больших потоков вязкой жидкости с неравномерным полем скоростей по нормальным и медленно изменяющимся вдоль потока сечениям:
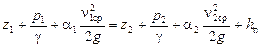 ,
,
где 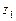 и
и 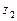 – расстояние от плоскости сравнения до центров тяжести нормальных сечений I и II; p1 и p2 – давления в этих сечениях на уровне центров тяжести; n1ср и n2ср – средние скорости в сечениях I и II; a1 и a2 – безразмерные коэффициенты кинетической энергии (коэффициенты Кориолиса); g – ускорение свободного падения; g – удельный объем жидкости.
– расстояние от плоскости сравнения до центров тяжести нормальных сечений I и II; p1 и p2 – давления в этих сечениях на уровне центров тяжести; n1ср и n2ср – средние скорости в сечениях I и II; a1 и a2 – безразмерные коэффициенты кинетической энергии (коэффициенты Кориолиса); g – ускорение свободного падения; g – удельный объем жидкости.
Из уравнения Бернулли выводится зависимость кинематической вязкости и потери напора в трубах при ламинарном режиме потока.
 Кроме труб ламинарный режим может существовать при протекании жидкости в щелях малого сечения, в капиллярах, в смазочном слое гидродинамических подшипников.
Кроме труб ламинарный режим может существовать при протекании жидкости в щелях малого сечения, в капиллярах, в смазочном слое гидродинамических подшипников.
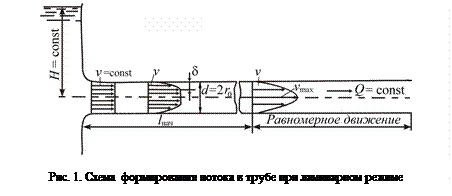
При ламинарном режиме поток на входе в трубу круглого сечения диаметром d (рис. 1) формируется так, что там создается равномерное поле скоростей по всему нормальному сечению потока (за исключением бесконечно тонкого слоя у стенок трубы, где имеет место прилипание жидкого слоя, т. е. его скорость v = 0). В последующих сечениях центральный участок с равномерным полем скоростей (ядро потока) уменьшается и вытягивается из-за тормозящего действия слоя, прилипшего к стенкам трубы. При этом возрастает толщина слоя d, на который распространяется торможение, обусловленное стенками трубы. Этот слой называют пограничным. На расстоянии lнач от входа в трубу значение d доходит до d = d/2, т. е. ядро сечения полностью ликвидируется; с этого момента начинается равномерное движение жидкости в трубе.
При ламинарном режиме длина начального участка
lнач » 0,029 Re d,
где Re – число Рейнольдса.
Поле скоростей v в любом сечении за начальным участком имеет параболическую форму с максимальной скоростью по оси трубы
vmax = 2vср.
На радиусе r трубы
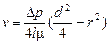 ,
,
где Dр – перепад давления на участке горизонтальной трубы длиной l; m – динамическая вязкость жидкости.
С учетом выше приведенного уравнения для равномерного движения потока в трубе круглого сечения при ламинарном режиме коэффициент кинетической энергии a = 2. В этом же случае потери напора на гидравлическое трение hп = hl на участке трубы диаметром d и длиной l, входящие в уравнение Бернулли, определяют по формуле
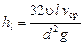 ,
,
u – кинематическая вязкость жидкости; g – ускорение свободного падения.
Заменяя vcp на Q/(p*d2/4), получим явную зависимость hl от кинематической вязкости при ламинарном режиме:
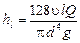 .
.
Для того чтобы графически реализовать эту зависимость в пакете MatLab необходимо знать следующие пункты.
Основным видом данных, которые используются в пакете MatLab (сокр. от англ. Matrix Laboratory – дословно «Матричная лаборатория»), являются матрицы. Даже общепринятые скалярные переменные рассматриваются как матрицы размерности 1´1.
2. Числовые данные, с которыми оперирует MatLab, в памяти компьютера представлены в формате double. Это означает, что каждое вещественное число занимает 8 байт в оперативной памяти и принимает по модулю значения из диапазона [10-308, 10+308]. Количество значащих десятичных цифр при этом достигает 16–17. Изменить формат данных можно вподпункте Свойства (Preference) пункта Файл (File) окна управления.
3. Необходимо обратить внимание на то, что следует: 1) при задании массива значениями заключать их в квадратные скобки; 2) элементы в строке массива разделять пробелами или запятыми; 3) при указании списка индексов использовать круглые скобки и разделительные запятые (указание индекса символом двоеточия соответствует заданию всех значений по соответствующему индексу).
4. При работе с массивами можно пользоваться списками i:k иi:j:k. В первом варианте понимается, что «от i до k с шагом 1» и во втором – то же с шагом j.
5. Приходится различать поэлементные операциис массивами и операции над матрицами по правилам линейной алгебры (для массивов перед знаком операции ставят точку).
6. Для того чтобы построить график функции y = f(x), необходимо сформировать два вектора одинаковой размерности – вектор значений аргументов (х) и вектор соответствующих значений функции (у), и обратиться к процедуре plot.
Пример: построение графика функции y = sin (x) * e–x
>> x = 0:0.1:6.28
% изменение аргумента x от 0 до 6,28 с шагом 0,1
>> y = sin(x).*exp(-x)
>> plot (x, y, ‘:g’)
Дополнительный параметр в процедуре plot – символ, ассоциированный с одним из 8 предусмотренных цветов: у – желтый (от yellow); g – зеленый (от green); m – малиновый (от magenta); b – синий (от blue); с – циановый (от cyan); w – белый (от white); r – красный (от red); k – черный (от black).
Вид графика можно изменить, задав стиль линии и форму маркера, которым метятся табличные точки. Стиль линии предусматривает выбор одной из четырех возможностей – сплошная линия (по умолчанию, управляющий символ – тире), пунктирная линия (управляющий символ – двоеточие), штрих-пунктирная линия (управляющие символы – тире и точка), штриховая линия (управляющие символы – два тире). Управляющие символы, определяющие стиль линии, задаются в строке третьего параметра вместе с цветом. Порядок следования символов – любой.
Дополнительные украшения графика заключаются в возможности снабдить его заголовком (процедура title), подписать оси (процедуры xlabel, ylabel), нанести координатную сетку (процедура grid on) и разместить легенду (процедура legend).
Для совмещение двух графиков в одном окне MatLab предлагает процедуру plotyy, которая производит двойную оцифровку осей. Для первой функции цифруются ось х внизу, ось у слева, а для второй функции ось х размечается вверху, ось у – справа. Цвет оцифровки при этом совпадает с цветом кривых.
Может оказаться, что в одном графическом окне необходимо отобразить большее число графиков. Тогда можно прибегнуть к функции subplot, которая позволяет разделить область рисования на несколько прямоугольных областей равного размера, расположенных подобно элементам матрицы:
>> subplot (row, col, cur);
Первые два аргумента задают количество рядов (row) и колонок (col). Третий параметр (cur) объявляет порядковый номер подобласти, в котором очередная функция plot будет строить свой график.
ЛЕД
Лед представляет собой прочный, дешевый и весьма распространенный в природе материал.
Предки современных эскимосов, населявшие арктическое побережье Северной Америки еще во второй половине первого тысячелетия нашей эры научились строить хижины из льда. Для постройки хижины изготавливалось около 60 снежных кирпичей размером 60´60´20 см3, при кладке кирпичи скреплялись водой. При горении жировых светильников температура в хижине поддерживалась около +2°C.
В Якутии до сих пор иногда создают «ледяные хижины». Для этого деревянные жилые строения щедро обливают на морозе водой. Образующаяся после замерзания воды довольно толстая корка льда способствует лучшему сохранению тепла в помещениях.
Самый большой ледяной дворец был построен в 1740 году по приказу русской императрицы Анны Иоановны, которая ради забавы решила отпраздновать женитьбу шута на одной из придворных приживалок. Для этой цели в Петербурге на Неве был выстроен ледяной дом с площадью основания около 80 м2 и высотой до 6 м. Стены и пол дома были выложены ледяными плитами и скреплены водой. Дом получился добротным и красивым, соответствующим церемонии, для которой был предназначен. Весной он растаял.
Как строительный материал лед использовался еще руководителями крестьянских восстаний Болотниковым и Пугачевым в военных целях. Для этого они обливали на морозе стога сена водой. Через некоторое время вода замерзала и превращала каждый стог в солидную преграду.
Немалую роль в истории нашей страны сыграли ледяные переправы. Еще во время войны со шведами по льду Финского и Ботнического заливов переправлялись русские войска. В гражданскую войну ледяная переправа действовала на Азовском море (между Керчью и Таманским полуостровом). Во время Великой Отечественной войны по льду Ладожского озера к осажденному Ленинграду проходила автомобильная дорога протяженностью в 27 км известная в истории как «Дорога жизни». Чтобы ледяной покров под влиянием проходившего по нему потока автомашин не пришел в резонансные колебания и не разрушился, принимались специальные меры. Для этого груз автомашин подбирался таким образом, чтобы частота свободных колебаний ледяного покрова отличалась от частоты, с которой воздействовали на ледяной покров подходившие автомашины.
Многообразно применение льда в хозяйстве. Например, зимой на севере Сибири с помощью льда укрепляют полотно зимних автотранспортных магистралей («зимников»). В этих условиях приходится считаться со скольжением по льду.
Строители Заполярья иногда используют в качестве строительного материала ледобетон. Так называют лед с включенной в него галькой. Ледобетон настолько прочен, что при работе с ним нередко ломаются даже стальные зубья экскаваторов. Другим вариантом ледобетона является лед с добавлением к нему древесной пульпы («ледопласт»). Материал этот выдерживает давление до 50 кг/см2 и может быть использован в качестве заменителя цемента при постройке плотин на реках Заполярья.
Армирование льда волокнистым материалом повышает предел его текучести и увеличивает прочность. При использовании хлопковых и древесных волокон прочность увеличивается в 2–3 раза, стекловолокно дает увеличение прочности до 8 раз. Древесные опилки и размельченный торф, смоченные водой и нанесенные на поверхность льда, хорошо предохраняют от таяния складские помещения из льда и ледяные причалы. Промораживание водонасыщенных плывунных грунтов укрепляет стенки котлованов на стройках и избавляет от необходимости производить откачку воды, что приводит к удешевлению строительства.
Свойства льда
Ледники являются большими хранилищами влаги, в них сосредоточено до 2,1% мировых запасов воды. Если бы все ледники растаяли, то уровень воды на Земле поднялся бы на 64 м, и около 1/8 поверхности суши было бы затоплено водой. В эпоху оледенения Европы, Канады и Сибири толщина ледяного покрова в горных местностях достигала 2 км. В настоящее время вследствие потепления климата Земли постепенно отступают границы ледников. Это обуславливает медленное повышение уровня воды в океанах.
При замерзании чистая вода расширяется почти на 10%, а у морского льда изменение объема происходит на меньшую величину. Поскольку вода при замерзании расширяется, увеличение внешнего давления понижает температуру ее замерзания; температура плавления льда, наоборот, повышается с давлением. В лабораторных условиях при давлении более 40 тыс. атмосфер можно получить лед, который будет плавиться при температуре 175°C. Теплоемкость и теплота плавления льда уменьшаются с температурой, теплопроводность же почти не зависит от температуры. Когда толщина льда на поверхности водоема достигает 15 см, он становится надежным теплоизолятором между водой и воздухом.
Морская вода замерзает при температуре – 1,91°C. При дальнейшем понижении температуры до – 8,2°C начинается осаждение сернокислого натрия, и только при температуре – 23°C из раствора выпадает хлористый натрий. Так как часть рассола при кристаллизации уходит изо льда, соленость его меньше солености морской воды. Многолетний морской лед настолько опресняется, что из него можно получать питьевую воду. Температура максимальной плотности морской воды ниже температуры замерзания. Это является причиной довольно интенсивной конвекции, охватывающей значительную толщу морской воды и затрудняющей замерзание. Теплоемкость морской воды стоит на третьем месте после теплоемкости водорода и жидкого аммиака.
Иногда вода замерзает при положительной температуре. Такое явление наблюдается в трубопроводах и почвенных капиллярах. В трубопроводах вода может замерзнуть при температуре +20°C. Объясняется это присутствием в воде метана. Поскольку молекулы метана занимают примерно в 2 раза больший объем, чем молекулы воды, они «расталкивают» молекулы воды, увеличивают расстояние между ними, что приводит к понижению внутреннего давления и повышению температуры замерзания. В почвенной влаге аналогичную роль выполняют молекулы белка. За счет влияния белковых молекул температура замерзания воды в почвенных капиллярах может возрасти до +4,4°C.
В воздухе содержится водяной пар, поэтому в нем образуются кристаллы льда – снежинки, которые, как правило, бывают в виде шести- и двенадцатилучевых звездочек, шестиугольных пластинок, шестигранных призм. При понижении температуры воздуха уменьшаются размеры образующихся кристаллов и возрастает разнообразие их форм.
На окнах тоже образуются кристаллы льда, совокупности которых носят название ледяных узоров, представляющих собой редкое по красоте зрелище. Среди многих видов морозных узоров чаще других встречаются дендриты (древовидные образования) и трихиты (волокнистые формы).
Характер кристаллизации воды на стекле во многом зависит от условий охлаждения. При охлаждении от 0 до –6°C и небольшой исходной упругости водяного пара на поверхности оконного стекла отлагается однородный слой непрозрачного, рыхлого льда. Для начального образования тонкого слоя такого льда в качестве затравок кристаллизации известную роль могут играть дефекты структуры поверхности, царапины. Однако в ходе дальнейшего развития процесса эти влияния полностью перекрываются общей картиной осаждения льда по всей охлаждающейся поверхности.
Если охлаждение поверхности оконного стекла начинается при положительной температуре и более высокой относительной влажности, то на охлаждающейся поверхности сначала отлагается пленка воды, которая уже при отрицательных температурах закристаллизовывается в виде дендритов. Чаще дендритная кристаллизация начинается с нижней части оконного стекла, где вследствие действия силы тяжести накапливается большее количество воды. Размеры дендритных кристаллов зависят от имеющегося для их образования материала. В нижней части окна, где пленка воды толще, дендриты обычно имеют большие размеры, по мере перехода к верхней части окна размеры дендритов уменьшаются. В случае равномерной увлажненности стекла размеры дендритов примерно одинаковы. Дальнейшее охлаждение способствует отложению между дендритами, а затем и на дендритах тонких слоев пушистого льда. Быстрые и значительные по величине переохлаждения дают мелкомасштабную дендритную кристаллизацию. При недостатке влаги на стекле нарушается сплошной характер кристаллизации: дендриты растут островками, их формы менее резко выражены, а размеры уменьшены в сравнении с нормальными условиями.
Трихиты образуются у острых краев царапин на поверхности охлаждающегося твердого тела. При этом вначале кристаллы образуют узкие параллельные полоски инея, вырождающиеся при дальнейшем охлаждении в достаточно плотные ледяные волокна, исходящие от основного стебля. В большинстве случаев как основное волокно, так и прилегающие к нему тонкие полоски инея слегка изогнуты.
В метеорологии инеем называется отложение льда из влажного воздуха на достаточно охлажденную горизонтальную поверхность. Отложение рыхлого льда на стеклах окон имеет черты сходства с инеем, несмотря на вертикальное расположение охлаждающей поверхности.
Известно, что крепкая серная кислота хорошо поглощает воду. Если между рамами окна поставить стаканчик с такой кислотой, основное количество водяного пара из пространства между стеклами поглотится ею, и отложения льда на окне при не очень сильных морозах происходить не будет. Тщательная теплоизоляция внешнего оконного стекла в местах его соприкосновения с рамой не допускает сильного охлаждения прилежащего изнутри к стеклу слоя воздуха, что также не благоприятствует осаждению льда на внутренней стороне стекла. С помощью этих мер затрудняется образование морозных узоров на окнах и обеспечивается необходимая прозрачность оконных стекол в зимнее время.
Акустические свойства льда
В утренние часы в горах происходит подтаивание находящегося между камнями льда. Это приводит к уменьшению сцепления камней друг с другом, к возникновению шумных камнепадов, лавин и осыпей. В вечерние часы камнепады происходят из-за перемещений камней при замерзании воды. Так как камнепады приносят людям немало вреда, разработаны приборы, предупреждающие о возможном обрушении пород – они фиксируют звуки, возникающие в горной породе при растрескивании, предшествующем камнепаду.
Растрескивание ледяного покрова на крупных внутриматериковых водоемах и в северных морях сопровождается звуками, напоминающими сухие ружейные выстрелы. Чем толще лед, тем шире и глубже трещины и сильнее звуки растрескивания. В полярных странах они настолько часты, что привыкшие к ним животные не боятся и настоящих выстрелов. Интенсивность растрескивания льда зависит от глубины и скорости выхолаживания, от степени неоднородности структуры льда и покрывающего его снежного покрова. Особенно благоприятно для образования трещин отсутствие снежного покрова на льду. Чаще всего растрескивание наблюдается при первых больших морозах в начале зимы и при резких потеплениях в ее середине.
Внимательные наблюдатели природы давно уже обратили внимание на изменение с понижением температуры воздуха скрипа снега при ходьбе: при низких температурах скрип всегда более звонок. Некоторые метеорологи первой четверти прошлого века предлагали даже оценивать температуру по воспринимаемым на слух изменениям в характере скрипа снега.
Акустические измерения показали, что в спектре скрипа снега имеются два пологих и не резко выраженных максимума – в диапазоне 250–400 Гц и 1–1,6 кГц. В большинстве случаев низкочастотный максимум на несколько децибел превышает высокочастотный. При температуре воздуха выше –6° высокочастотный максимум сглаживается и нередко полностью ликвидируется. С понижением температуры от –8° до –20° сила звука скрипа снега увеличивается на 1 дБ.
При ломке ледяных сосулек диаметром 1,5–4 см были отмечены два максимума акустической энергии – в диапазоне 125–200 Гц и 1,25–2 кГц. Максимумы эти достаточно резко выражены и четко отделены друг от друга. Такая же картина распределения акустической энергии по спектру наблюдается и при взламывании речного льда толщиной 0,5 м с помощью ледокола. Таким образом, высокочастотные максимумы акустической энергии для скрипа снега, ломки сосулек и речного льда приходятся на один и тот же диапазон частот, низкочастотные же смещены по спектру. Это указывает на различие в жесткости структуры снега и льда.
Известно, что мягкие материалы при ударе или изломе дают глухой звук, в котором высокие частоты ослаблены или совсем не представлены. Понижение температуры окружающей среды ведет к увеличению твердости материалов, к усилению взаимодействия между частицами вещества. Поэтому при ударе или изломе тел, находящихся в условиях пониженной температуры, спектр возникающих акустических колебаний распространяется в область высоких частот.
Благодаря наличию множества воздушных промежутков между кристаллами льда, снежный покров имеет невысокую плотность, и его с полным основанием можно отнести к категории мягких материалов. При понижении температуры кристаллы становятся более упругими, а снежный покров в целом – более хрупким. Это и обеспечивает расширение акустического спектра скрипа снега в область высоких частот. Поскольку скрип снега является результатом массового слома кристаллов льда, можно полагать, что перераспределение энергии скрипа с температурой указывает на изменения в характере взаимодействия элементов структуры снежного покрова.
В тихую морозную погоду при температуре воздуха ниже –49°С в холодных странах (особенно в Якутии) наблюдатели нередко отмечают шуршащий звук, напоминающий звук пересыпаемого зерна. На первых порах этот звук приписывали полярному сиянию, которое часто наблюдалось при этом явлении. Однако впоследствии было установлено, что причина явления – в столкновении кристаллов льда, которые образуются в большом количестве при дыхании человека в морозном воздухе. У якутов это явление известно под именем «шёпота звезд».
