Раздел 2 . Химическая термодинамика и кинетика
Энергетика химических процессов
БЛОК А
Выбор
2.1.1. Термодинамическая система - это группа тел, …
в- находящихся в окружающей среде.
в- которые отделены от окружающей среды поверхностью.
в+ которые находятся во взаимодействии и мысленно или фактически обособлены от окружающей среды.
в- которые находятся во взаимодействии, обособлены от окружающей среды и совершают работу против внешних сил.
Выбор
2.1.2. Реакции, протекающие с выделением теплоты, называются…
в- эпизодическими
в- эндотермическими
в+ экзотермическими
в- эзотерическими
Выбор
2.1.3. Термодинамическими функциями являются
в+ H – энтальпия.
в- V – объем.
в+ S- энтропия.
в+ U – внутренняя энергия.
в- p – давление.
Выбор
2.1.4. 1-й закон термодинамики выражается уравнением
в- DHОБР = -DHРАЗЛ.
в+ Q = DU + АВНЕШ.
в- DG = DH - TDS.
в- H = U – pV.
Выбор
2.1.5. Самопроизвольное протекание процесса в неизолированной изобарно-изотермической системе сопровождается
в- возрастанием энтропии.
в- увеличением энергии Гиббса.
в+ уменьшением энергии Гиббса.
в- неизменностью энергии Гиббса.
в- совершением работы против внешних сил.
Выбор
2.1.6. Экзотермической является реакция
в- BaCO3(Т) = BaO(Т) + CO2(Г); DH = 258,7 кДж.
в- CaCO3(Т) = CaO(Т) + CO2(Г); DH > 0.
в+ Ca(Т) + O2(Г) = CaO(Т); DH = -645,6 кДж.
в- MgCO3(Т) = MgO(Т) + CO2(Г); DH = 101,6 кДж.
Выбор
2.1.7. Тепловой эффект реакции зависит от …
в- конечного и начального состояний системы и зависит от пути процесса.
в+ конечного и начального состояний системы и не зависит от пути проведения процесса.
в- конечного и начального состояний системы и условий проведения процесса.
в- условий проведения процесса и не зависит от начального и конечного состояний системы.
Выбор
2.1.8. Энтропия при протекании реакции 4NH3(Г) + 3O2(Г) = 2N2(Г) + 6H2O(Г)
в+ увеличивается.
в- уменьшается.
в- не изменяется.
в- зависит от условий проведения реакции.
2.1.9. Тепловой эффект реакции …. соответствует теплоте образования уксусной кислоты CH3COOH
в- CH4 + CO2 = CH3COOH.
в+ 2C + 2H2 + O2 = CH3COOH.
в- C + O2 + CH4 = CH3COOH.
в- 2CH3COH + O2 = 2CH3COOH.
в- CH3COONa + HCl = CH3COOH + NaCl.
2.1.10. Энтальпия образования HCl равна (H2(Г) + Cl2(Г) = 2HCl(Г) выделяется 92,31 кДж)
в- 92,31 кДж/моль.
в- -92,31 кДж/моль.
в- 46,155 кДж/моль.
в+ -46,155 кДж/моль.
2.1.11. Изменение энергии Гиббса при протекании химической реакции вычисляется по уравнению:
| в- | 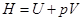 |
| в- | 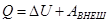 |
| в- | 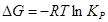 |
| в+ | 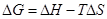 |
2.1.12. Установите соответствие между цифрами на графике и характеристикой состояния
|
|
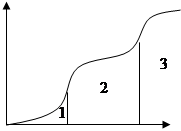
С1 1
О1 твёрдое
С2 2
О2 жидкое
С3 3
О3 газообразное
О4 ионное
2.1.13. Самопроизвольно в прямом направлении протекает реакция:
- CH4(Г) + CO2(Г) D 2CO(Г) + 2H2(Г); DG = 170,63 кДж.
- Fe2O3(Т) + 3H2(Г) D 2Fe(Т) + 3H2(Г), DG = 55,28 кДж.
+ 4NH3(Г) + 5O2(Г) D 4NO(Г) + 6H2(Г), DG = -959,81 кДж.
- H2(Г) + CO2(Г) D CO(Г) + H2(Ж), DG > 0.
2.1.14. Энтропия является функцией состояния и ее изменение равно
в- сумме энтропий исходных веществ и конечных продуктов.
в- разности между суммой энтропий начальных веществ и суммой энтропий продуктов реакции.
в+ разности между суммой энтропий конечных веществ и суммой энтропий начальных веществ.
в- определяется способом проведения процесса.
2.1.15. При получении 2 моль этанола, согласно термохимическому уравнению
C2H4(Г) + H2O (Ж) D C2H5OH(Ж), DH0 = –44 кДж, выделяется ___ кДж теплоты.
в+ 88
в- 66
в- 44
в- 22
2.2. Скорость реакции и методы её регулирования
БЛОК А
2.2.1. Средняя скорость гомогенной реакции выражается формулой:
в- 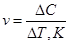
в+ 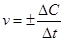
в- 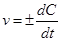
в- 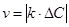
2.2.2. Измельчение твердого вещества скорость химической реакции:
в- уменьшает.
в+ увеличивает.
в- не изменяет.
в- замедляет.
2.2.3. Энергия активации обозначена цифрой на энергетической диаграмме
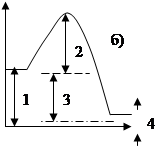
в- 1.
в+ 2.
в-3.
в- 4.
2.2.4. Соответствие между уравнениями реакций и формулами скорости
С1 A + B = D
О1 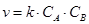
С2 2A + B = D
О2 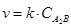
С3 2A + 2B = 2D
О3 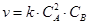
С4 A2B = 2А + В
О4 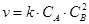
О5 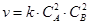
2.2.5. Математическая зависимость скорости реакции от температуры описывается уравнением:
в- 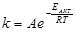
в- 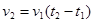
в- 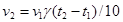
в+ 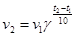
2.2.6. Катализатор скорость химической реакции:
в- не изменяет.
в+ увеличивает.
в- уменьшает.
в- замедляет.
в- периодически влияет.
2.2.7. Катализатор изменяет скорость реакции, потому что…
в- удаляет продукты реакции.
в+ взаимодействует с реагирующими веществами, изменяя энергию активации.
в- изменяет температурный коэффициент реакции.
в- смещает положение равновесия в сторону прямой реакции.
2.2.8. Выражение для скорости 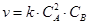 соответствует реакции
соответствует реакции
в- A + B = C.
в+ 2A + B = C.
в- A + 2B = C.
в- 2A + 2B = 2C.
в- A2B = C + D.
2.2.9. Изменение концентрации реагирующих веществ в единицу времени называется ..
в+ скоростью химической реакции.
в- константой равновесия химической реакции.
в- константой скорости химической реакции.
в- изменением плотности химической реакции
2.2.10. Температурный коэффициент показывает:
в+ во сколько раз изменится скорость реакции при повышении температуры на 100.
в- во сколько раз изменяется концентрация при повышении температуры на 100.
в- во сколько раз увеличивается время протекании реакции при повышении температуры на 100.
в- на сколько градусов изменяется температура при протекании реакции.
2.2.11. Соответствие между понятиями и их математическими выражениями:
С1 Закон действующих масс
О1 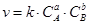
С2 Правило Вант-Гоффа
О2 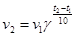
С3 Уравнение Аррениуса
О3 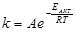
С4 Скорость химической реакции
О4 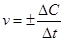
О5 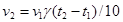
2.2.12. Математическое выражение закона действующих масс
в- 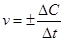
в- 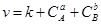
в+ 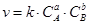
в- 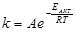
2.2.13. Скорость химической реакции зависит от:
в+ температуры.
в- цвета вещества.
в+ катализатора.
в- формы реактора.
в+ природы вещества.
2.2.14. Величина 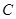 в выражении
в выражении 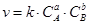 обозначает
обозначает
в- температуру.
в- давление.
в+ концентрацию вещества.
в- скорость реакции.
2.2.15. Закон действующих масс строго соблюдается для ___ реакций
в- гетерогенных
в- последовательных
в- параллельных
в+ гомогенных
