Окислительно-восстановительная реакция между водородом и фтором

Разделяется на две полуреакции:
1) Окисление:

2) Восстановление:

Окисление, восстановление
В окислительно-восстановительных реакциях электроны от одних атомов, молекул или ионов переходят к другим. Процесс отдачи электронов — окисление. При окислении степень окисления повышается:





Процесс присоединения электронов — восстановление. При восстановлении степень окисления понижается:





Атомы или ионы, которые в данной реакции присоединяют электроны являются окислителями, а которые отдают электроны — восстановителями.
Окисли́тель — вещество, в состав которого входят атомы, присоединяющие во время химической реакции электроны, иными словами, окислитель — это акцептор электронов.
В зависимости от поставленной задачи (окисление в жидкой или в газообразной фазе, окисление на поверхности) в качестве окислителя могут быть использованы самые разные вещества.
ВОССТАНОВИТЕЛЬ - вещество, которое вызывает реакции ВОССТАНОВЛЕНИЯ. Восстановлении кислорода для образования воды (2Н2+О2>2Н2О) водород является восстановителем
Окислительно-восстановительные реакции можно разделить на три группы в зависимости от того, где находятся атомы элемента окислителя и восстановителя.
Реакции межатомного и межмолекулярного окисления-восстановления представляют собой реакции, в которых окислитель и восстановитель являются разными веществами. Сюда относятся, например, простейшие реакции соединения и замещения:
| O20 | + | 2Mg0 | = | 2Mg+2O –2 | 2KJ – | + | Cl20 | = | 2KCl + J2. | |
| окисл. | восст. | восст. | окисл. |
Реакции диспропорционирования (самоокисления-самовосстановления) представляют собой реакции, в которых восстановителями являются атомы элементов с промежуточной степенью окисления у одного и того же вещества. В данном случае они реагируют друг с другом как восстановитель и окислитель и способны отдавать и принимать электроны, переходя один в низшую, другой в высшую степени окисления.
Например:
| Сl20 | + H2O = HCl –1 + HCl+1O. |
| окисл., восст. |
Реакции внутримолекулярного окисления-восстановления, в которых степень окисления разных атомов изменяется внутри одной и той же молекулы. Чаще всего это происходит из-за термического разложения вещества. Например:
| 2Hg+2O –2 = 2Hg0 + O20 | N –3H4N+5O3 = N2+1O + 2H2O. |
32
Возникновение скачка потенциала. Механизм возникновения скачка потенциала на границе металл - расплавленный электролит мы здесь не рассматриваем.
Механизм возникновения скачка потенциала на границе металл - расплавленный электролит не рассматривается.
Механизм возникновения скачка потенциала на границе раздела металл - раствор до настоящего времени является еще недостаточно вы-ясненным.
Второй принцип правильно отражает механизм возникновения равновесного скачка потенциала на границе металл - раствор, хотя обмен ионами не исчерпывает всех возможных причин, ответственных за образование скачка потенциала на этой границе. Если между электродом и раствором существует равновесие, то величина электродного потенциала будет мерой изменения свободной энергии F ( или термодинамического потенциала G), которая отвечает электродной реакции. При заданной электродной реакции электродный потенциал должен быть определенной и постоянной величиной.
Второй принцип правильно отражает механизм возникновения равновесного скачка потенциала на границе металл - раствор, хотя обмен ионами не исчерпывает всех возможных причин, ответственных за образование скачка потенциала на этой границе. Если между электродом и раствором существует равновесие, то величина электродного потенциала будет мерой изменения свободной энергии зр ( или термодинамического потенциала G), соответствующей электродной реакции. При заданной электродной реакции электродный потенциал должен быть определенной и постоянной величиной.
Существует несколько теорий, объясняющих механизм возникновения скачка потенциала на границе раствор - металл.
Излагается теория двойного слоя на границе металл-раствор и механизм возникновения скачка потенциала на этой границе. Обсуждается поведение металлических электродов в условиях протекания внешнего тока на основе общей теории кинетики электродных процессов. Детально рассматриваются кинетические закономерности процессов катодного выделения водорода, электрохимического восстановления кислорода и ионизации металлов. Выведены выражения, определяющие коррозионное поведение металлов в условиях их саморастворения для случая идеально однородной поверхности и при ее дифференциации на анодную и катодную зоны.
Электронно-статистическая модель двойного электрического слоя, использующая теорию неоднородного электронного газа металла, дает возможность с единых позиций описать механизм возникновения скачка потенциала, а также такие характеристики ДЭС, как емкость и поверхностное натяжение в достаточно хорошем согласии с экспериментом. Показано, что предпочтение из поляризационного и электронного вкладов в энергию ДЭС должно быть отдано второму. Однако решение вопроса о вкладе поляризационных мод не доведено до логического завершения и осуществлено лишь на качественном уровне. Необходим анализ взаимодействий на микроскопическом количественном уровне.
В предыдущих разделах был выяснен физический смысл электродного потенциала, показана его связь со скачками потенциала на границах раздела фаз, рассмотрены условия возникновения скачка потенциала на границе электрод - электролит - основной составной части электродного потенциала - и разобрана зависимость его величины от состава раствора. При обсуждении механизма возникновения скачка потенциалана границе электрод - электролит было отмечено, что главной причиной появления этого скачка является обмен ионами между металлом электрода и раствором.
В предыдущих разделах был выяснен физический смысл электродного потенциала, показана его связь со скачками потенциала на границах раздела фаз, рассмотрены условия возникновения скачка потенциала на границе электрод - электролит ( основной составной части электродного потенциала) и разобрана зависимость его величины от состава раствора. При обсуждении механизма возникновения скачка потенциалана границе электрод - электролит было отмечено, что главной причиной его появления является обмен ионами между металлом электрода и раствором.
С другой стороны они свидетельствуют о том, что разность потенциалов ТНЗ двух металлов практически не зависит от температуры. Таким образом, механизм возникновения скачка потенциала металл-среда формируется скорее всего электронными подсистемами обеих соприкасающихся фаз. Стоящая слева в формуле (2.6) контактная разность потенциалов формируется электронами металлов в отсутствии раствора S и, следовательно, не зависит от его природы. Чтобы объяснить этот факт, нужно указать механизм подстройки под к р п молекул растворителя ( или расплава), причем такой, который бы не зависел от природы этих молекул.
В электрохимии стандартный электродный потенциал, обозначаемый Eo, E0, или EO, является мерой индивидуального потенциала обратимого электрода (в равновесии) встандартном состоянии, которое осуществляется в растворах при эффективной концентрации в 1 моль/кг и в газах при давлении в 1 атмосферу или 100 кПа (килопаскалей). Объёмы чаще всего взяты при 25 °C. Основой для электрохимической ячейки, такой как гальваническая ячейка всегда является окислительно-восстановительная реакция, которая может быть разбита на две полуреакции: окисление на аноде (потеря электрона) и восстановление на катоде (приобретение электрона). Электричество вырабатывается вследствие различияэлектростатического потенциала двух электродов. Эта разность потенциалов создаётся в результате различий индивидуальных потенциалов двух металлов электродов по отношению к электролиту.
Окислительно-восстановительный потенциал (редокс-потенциал от англ. redox — reduction-oxidation reaction, Eh или Eh) — мера способности химического вещества присоединять электроны (восстанавливаться[1]). Окислительно-восстановительный потенциал выражают в милливольтах (мВ). Примером окислительно-восстановительного электрода: Pt/Fe3+,Fe2+ Окислительно-восстановительный потенциал определяют как электрический потенциал, устанавливающийся при погружении платины или золота (инертный электрод) вокислительно-восстановительную среду, то есть в раствор, содержащий как восстановленное соединение (Ared), так и окисленное соединение (Aox). Если полуреакцию восстановления представить уравнением:
Aox + n·e− → Ared,
то количественная зависимость окислительно-восстановительного потенциала от концентрации (точнее активностей) реагирующих веществ выражается уравнением Нернста.
Окислительно-восстановительный потенциал определяют электрохимическими методами с использованием стеклянного электрода с red-ox функцией[2] и выражают в милливольтах (мВ) относительно стандартного водородного электрода в стандартных условиях.
Уравнение Нернста — уравнение, связывающее окислительно-восстановительный потенциал системы с активностями веществ, входящих в электрохимическое уравнение, истандартными электродными потенциалами окислительно-восстановительных пар.
 ,
,
Где:
 — электродный потенциал,
— электродный потенциал,  — стандартный электродный потенциал, измеряется в вольтах;
— стандартный электродный потенциал, измеряется в вольтах;
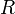 — универсальная газовая постоянная, равная 8.31 Дж/(моль·K);
— универсальная газовая постоянная, равная 8.31 Дж/(моль·K);
 — абсолютная температура;
— абсолютная температура;
 — постоянная Фарадея, равная 96485,35 Кл·моль−1;
— постоянная Фарадея, равная 96485,35 Кл·моль−1;
 — число моль электронов, участвующих в процессе;
— число моль электронов, участвующих в процессе;
 и
и  — активности соответственно окисленной и восстановленной форм вещества, участвующего в полуреакции.
— активности соответственно окисленной и восстановленной форм вещества, участвующего в полуреакции.
Если в формулу Нернста подставить числовые значения констант  и
и  и перейти от натуральных логарифмов к десятичным, то при
и перейти от натуральных логарифмов к десятичным, то при  получим
получим

Гальвани́ческий элеме́нт — химический источник электрического тока, основанный на взаимодействии двух металлов и (или) их оксидов в электролите, приводящем к возникновению в замкнутой цепи электрического тока. Назван в честь Луиджи Гальвани.
Гальванические первичные элементы - это устройства для прямого преобразования химической энергии, заключенных в них реагентов (окислителя и восстановителя), в электрическую. Реагенты, входящие в состав источника, расходуются в процессе его работы, и действие прекращается после расхода реагентов. Примером гальванического элемента является элемент Даниэля –Якоби.
Широкое распространение получили марганцево-цинковые элементы, не содержащие раствора электролита (сухие элементы,батарейки). Так, в солевых элементах Лекланше цинковый электрод служит анодом, электрод из смеси диоксида марганца с графитом служит катодом, графит служит токоотводом. Электролитом является паста из раствора хлорида аммония с добавкой муки или крахмала в качестве загустителя.
Щелочные марганцево-цинковые элементы, в которых в качестве электролита используется паста на основе гидроксида калия, обладают целом рядом преимуществ, в частности существенно большей ёмкостью, лучшей работой при низких температурах и при больших токах нагрузки.
 Солевые и щелочные элементы широко применяются для питания радиоаппаратуры и различных электронных устройств.
Солевые и щелочные элементы широко применяются для питания радиоаппаратуры и различных электронных устройств.
Вторичные источники тока (аккумуляторы) - это устройства, в которых электрическая энергия внешнего источника тока превращается в химическую энергию и накапливается, а химическая – снова превращается в электрическую. Одним из наиболее распространенных аккумуляторов является свинцовый (или кислотный). Электролитом является 25-30 % раствор серной кислоты. Электродами кислотного аккумулятора являются свинцовые решетки, заполненные оксидом свинца, который при взаимодействии с электролитом превращается в PbSO4.
Также существуют щелочные аккумуляторы. Наибольшее применение получили никель-кадмиевые и никель-металлгидридные аккумуляторы, в которых электролитом служит KOH.
В различных электронных устройствах (мобильные телефоны, планшеты, ноутбуки), в основном, применяются литий-ионные илитий-полимерные аккумуляторы, характеризующиеся высокой ёмкостью и отсутствием эффекта памяти.
Электрохимические генераторы (топливные элементы) - это элементы, в которых происходит превращение химической энергии в электрическую. Окислитель и восстановитель хранятся вне элемента, в процессе работы непрерывно и раздельно подаются к электродам. В процессе работы топливного элемента электродые не расходуются. Восстановителем является водород (H2), метанол (CH3OH), метан (CH4) в жидком или газообразном состоянии. Окислителем обычно является кислород воздуха или чистый. В кислородно-водородном топливном элементе со щелочным электролитом происходит превращение химической энергии в электрическую. Энергоустановки применяются на космических кораблях, они обеспечивают энергией космический корабль и космонавтов.
Электро́лиз — физико-химический процесс, состоящий в выделении на электродах составных частей растворённых веществ или других веществ, являющихся результатом вторичных реакций на электродах, который возникает при прохождении электрического тока через раствор либо расплав электролита.
Упорядоченное движение ионов в проводящих жидкостях происходит в электрическом поле, которое создается электродами — проводниками, соединёнными с полюсами источника электрической энергии. Анодом при электролизе называется положительный электрод, катодом — отрицательный[1]. Положительные ионы — катионы — (ионы металлов, водородные ионы, ионы аммония и др.) — движутся к катоду, отрицательные ионы — анионы — (ионы кислотных остатков и гидроксильной группы) — движутся к аноду.
Явление электролиза широко применяется в современной промышленности. В частности, электролиз является одним из способов промышленного получения алюминия, водорода, а также гидроксида натрия, хлора, хлорорганических соединений[источник не указан 1318 дней], диоксида марганца[2], пероксида водорода. Большое количество металлов извлекаются из руд и подвергаются переработке с помощью электролиза (электроэкстракция, электрорафинирование). Также, электролиз является основным процессом, благодаря которому функционирует химический источник тока.
Электролиз находит применение в очистке сточных вод (процессы электрокоагуляции, электроэкстракции, электрофлотации).
Первый закон Фарадея
В 1832 году Фарадей установил, что масса m вещества, выделившегося на электроде, прямо пропорциональна электрическому заряду q, прошедшему через электролит:

если через электролит пропускается в течение времени t постоянный ток с силой тока I. Коэффициент пропорциональности 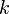 называется электрохимическим эквивалентом вещества. Он численно равен массе вещества, выделившегося при прохождении через электролит единичного электрического заряда, и зависит от химической природы вещества.
называется электрохимическим эквивалентом вещества. Он численно равен массе вещества, выделившегося при прохождении через электролит единичного электрического заряда, и зависит от химической природы вещества.
 (1)
(1)
 (2)
(2)
 (3)
(3)
 (4)
(4)
 , где z — валентность атома (иона) вещества, e — заряд электрона (5)
, где z — валентность атома (иона) вещества, e — заряд электрона (5)
Подставляя (2)-(5) в (1), получим


где  — постоянная Фарадея.
— постоянная Фарадея.


Второй закон Фарадея.Электрохимические эквиваленты различных веществ относятся, как их химические эквиваленты.
Химическим эквивалентом иона называется отношение молярной массы A иона к его валентности z. Поэтому электрохимический эквивалент

где  — постоянная Фарадея.
— постоянная Фарадея.
Второй закон Фарадея записывается в следующем виде:

где  — молярная масса данного вещества, образовавшегося (однако не обязательно выделившегося — оно могло и вступить в какую-либо реакцию сразу после образования) в результате электролиза, г/моль;
— молярная масса данного вещества, образовавшегося (однако не обязательно выделившегося — оно могло и вступить в какую-либо реакцию сразу после образования) в результате электролиза, г/моль;  — сила тока, пропущенного через вещество или смесь веществ (раствор, расплав), А;
— сила тока, пропущенного через вещество или смесь веществ (раствор, расплав), А;  — время, в течение которого проводился электролиз, с;
— время, в течение которого проводился электролиз, с;  — постоянная Фарадея, Кл·моль−1;
— постоянная Фарадея, Кл·моль−1;  — число участвующих в процессе электронов, которое при достаточно больших значениях силы тока равно абсолютной величине заряда иона (и его противоиона), принявшего непосредственное участие в электролизе (окисленного или восстановленного). Однако это не всегда так; например, при электролизе раствора соли меди(II) может образовываться не только свободная медь, но и ионы меди(I) (при небольшой силе тока).
— число участвующих в процессе электронов, которое при достаточно больших значениях силы тока равно абсолютной величине заряда иона (и его противоиона), принявшего непосредственное участие в электролизе (окисленного или восстановленного). Однако это не всегда так; например, при электролизе раствора соли меди(II) может образовываться не только свободная медь, но и ионы меди(I) (при небольшой силе тока).
На катоде в первую очередь восстанавливаются (принимают электроны) катионы с наиболее высокими (максимальными) значениями электродного потенциала (сильные окислители).
1. Если электродный потенциал катиона j°Me/Men+ < -1,6 В, то на катоде восстанавливаются ионы H+ молекулы H2O с выделением H2 и накоплением в растворе OH-:

2. При значении стандартного электродного потенциала катиона  на катоде восстанавливаются только ионы металла, а разряд ионов H+ не происходит:
на катоде восстанавливаются только ионы металла, а разряд ионов H+ не происходит:

3. Если -1,6 В <j°Me/Men+ < 0 В, то на катоде протекают два процесса: восстановление ионов Н+ и ионов металла. Это обусловлено тем, что, во-первых, потенциал водородного электрода зависит от рН раствора:
jH2/2H+ = -0,059· pH,
во-вторых, выделение водорода на катоде происходит с более высоким перенапряжением по сравнению с перенапряжением разряда многих металлов.
Таким образом, при некоторой плотности тока потенциал выделения водорода становится отрицательнее, чем потенциал выделения металла (рис.8.15).
Рис. 8.15. Поляризационные кривые катодного выделения водорода и металла.  Высокое водородное перенапряжение - явление положительное, благодаря этому, из водных растворов удается выделять на катоде марганец, цинк, хром, железо, кадмий, кобальт, никель и другие металлы. Все вышесказанное можно представить следующей схемой: Ряд разряжаемости на катоде (для распространенных катионов) Высокое водородное перенапряжение - явление положительное, благодаря этому, из водных растворов удается выделять на катоде марганец, цинк, хром, железо, кадмий, кобальт, никель и другие металлы. Все вышесказанное можно представить следующей схемой: Ряд разряжаемости на катоде (для распространенных катионов) | ||
| K+, Na+, Mg2+, Al3+ Трудно разряжаемые | H+, Zn2+, Fe2+, Ni2+, Sn2+, Pb2+ ® | Cu2+, Ag+ Легко разряжаемые |
| Продукты электролиза в водном растворе | ||
| Только H2 | Металл и H2 | Только металл |
На аноде, в первую очередь, окисляются (отдают электроны) анионы с минимальным значением электродного потенциала (сильные восстановители).
1) К таким анионам относятся I-, Br-, S2-, OH-, Cl-. Потенциал кислородного электрода в широкой области рН меньше потенциалов галоидных ионов (за исключением иона I-).
jOH-/O2 = 1,23 – 0,059· рН
Однако при наличии в растворе ионов галогенов вследствие высокой поляризации реакции выделения O2 в первую очередь на аноде выделяется йод, затем - бром. При наличии ионов Cl- в растворе при малых плотностях тока идет выделение O2, при высоких плотностях тока - выделение хлора (рис. 8.16).

Рис. 8.16. Поляризационные кривые анодного выделения O2 и Cl2.
2) Кислородсодержащие анионы (NO3-, PO43-) не способны окисляться. Фторид- и сульфат- ионы (F-, SO42-), характеризующиеся слишком высокими для восстановителей значениями электродных потенциалов (j ° > 2 В), в водных растворах не окисляются. Вместо них на нерастворимом аноде окисляются ионы OH- и H2O с выделением кислорода и накоплением в растворе ионов H+.

3) Возможно окисление атомов металла (растворение анода).
Первичные реакции

Вторичные реакции

Выходом по току в гальванотехнике называют выраженное в процентах отношение количества фактически пропущенного через электролит заряда (Qf) к теоретически необходимому (Qt) для осуществления фактически наблюдаемого массопереноса (mf).

Иногда выход по току рассчитывается как отношение массы при фактическом массопереносе mf к теоретическому массопереносу mt, рассчитанному по закону Фарадея:

Для случая осаждения массы на электроде выход по току оказывается всегда выше 1. Для случая растворения материала электрода выход по току оказывается всегда ниже 1.
Выход по току связан с электрохимическим эквивалентом.
Электрохимическим эквивалентом в гальванотехнике называют количество вещества, выделившееся или растворившееся на электроде, отнесённое к величине заряда, пропущенного через электролит:
 ,
,
где
mf - масса фактически осаждённого или растворённого материала электрода;
Qf - фактически пропущенный заряд, определяемый как интеграл пропускаемого через электролит тока по времени.
Прохождение тока вызывает изменение потенциала электрода. Это явление, а также величина изменения потенциала, называются поляризацией:
ΔЕ = Еi - Ep , (8.9)
где ΔЕ – поляризация; Еi – неравновесный потенциал электрода, т.е. потенциал при прохождении электрического тока; Ep– равновесный потенциал.
Изменение потенциала электрода также называют перенапряжением.
Поляризация имеет место как на катоде, так и на аноде, поэтому различают катодную (ΔЕк) и анодную(ΔЕа) поляризацию. Катодная поляризация всегда отрицательна, а анодная всегда положительна.
Поляризация определяется из экспериментально получаемой зависимости потенциала электрода от плотности тока, т.е. отношения тока I к площади электрода S (i=I/S).
График зависимости потенциала от плотности тока носит название поляризационной кривой.
Величина поляризации зависит от плотности тока.
На поляризацию влияет также материал электрода, состояние его поверхности и целый ряд других факторов
Возникновение поляризации: Любой электродный процесс включает в себя не менее трех стадий:
1) подвод реагирующих веществ к электроду;
2) процесс электрохимического превращения на поверхности электрода, который может сопровождаться дополнительными химическими реакциями;
1) отвод продуктов реакции от электрода.
Эти процессы протекают последовательно и имеют, обычно, различные скорости. Скорость наиболее медленной (лимитирующей) стадии определяет общую скорость процесса. Ускорение лимитирующей стадии достигается повышением потенциала электрода, т.е. поляризацией. В зависимости от того, какая стадия является лимитирующей, различают концентрационную и электрохимическую поляризацию.
Электрохимическая поляризация (перенапряжение) обусловлена пониженной скоростью электрохимических реакций на электроде.
Скорость электрохимических реакций может быть повышена увеличением температуры и использованием катализатора, а также при повышении потенциала электрода по сравнению с его равновесным значением, т.е. при поляризации. Роль поляризации сводится к уменьшению энергии активации и величина этого снижения пропорциональна величине поляризации. Уменьшение энергии активации сопровождается увеличением скорости реакции, что в случае электрохимических процессов ведет к увеличению плотности тока
Корро́зия (от лат. corrosio — разъедание) — это самопроизвольное разрушение металлов в результате химического или физико-химического взаимодействия с окружающей средой. В общем случае это разрушение любого материала, будь то металл или керамика, дерево или полимер. Причиной коррозии служит термодинамическая неустойчивость конструкционных материалов к воздействию веществ, находящихся в контактирующей с ними среде. Пример — кислородная коррозия железа в воде: 4Fe + 6Н2О + ЗО2 = 4Fe(OH)3. Гидратированный оксид железа Fe(OН)3 и является тем, что называют ржавчиной.
Электрохимическая коррозия. Разрушение металла под воздействием возникающих в коррозионной среде гальванических элементов называют электрохимической коррозией. Не следует путать с электрохимической коррозией коррозию однородного материала, например, ржавление железа или т. п. При электрохимической коррозии (наиболее частая форма коррозии) всегда требуется наличие электролита (Конденсат, дождевая вода и т. д.), с которым соприкасаются электроды — либо различные элементы структуры материала, либо два различных соприкасающихся материала с различающимися окислительно-восстановительными потенциалами. Если в воде растворены ионы солей, кислот, или т. п., электропроводность её повышается, и скорость процесса увеличивается.
Коррозионный элемент.При соприкосновении двух металлов с различными окислительно-восстановительными потенциалами и погружении их в раствор электролита, например, дождевой воды с растворенным углекислым газом CO2, образуется гальванический элемент, так называемый коррозионный элемент. Он представляет собой не что иное, как замкнутую гальваническую ячейку. В ней происходит медленное растворение металлического материала с более низким окислительно-восстановительным потенциалом; второй электрод в паре, как правило, не корродирует. Этот вид коррозии особо присущ металлам с высокими отрицательными потенциалами. Так, совсем небольшого количества примеси на поверхности металла с большим редокспотенциалом уже достаточно для возникновения коррозионного элемента. Особо подвержены риску места соприкосновения металлов с различными потенциалами, например, сварочные швы или заклёпки.
Если растворяющийся электрод коррозионно-стоек, процесс коррозии замедляется. На этом основана, например, защита железных изделий от коррозии путём оцинковки — цинк имеет более отрицательный потенциал, чем железо, поэтому в такой паре железо восстанавливается, а цинк должен корродировать. Однако в связи с образованием на поверхности цинка оксидной плёнки процесс коррозии сильно замедляется.
